Clear Sky Science · sv
c-Myc/GRPEL1 upprätthåller fettsyrasyntes via FASN för att stödja PDAC-cellers proliferation
Varför cancercellers fettbehov spelar roll
Bukspottkörtelcancer är en av de dödligaste cancerformerna, delvis därför att dess celler är skickliga på att omprogrammera sin egen metabolism för att överleva och växa. Denna studie undersöker en överraskande del av den berättelsen: hur pankreastumörceller upptrappat sina interna ”fettfabriker” för att driva ohämmad tillväxt, och hur blockering av denna process kan öppna nya behandlingsmöjligheter för patienter.
En svår cancer med ett metabolt försprång
De flesta pankreascancerfallen är av typen pankreasductalt adenokarcinom (PDAC), som vanligtvis upptäcks sent och svarar dåligt på dagens behandlingar. PDAC-celler lever i en tuff miljö med lite syre och knappa näringsämnen, men de frodas genom att omkoppla hur de använder socker, fetter och andra bränslen. Deras mitokondrier — små kraftverk inuti cellerna — spelar en central roll i denna omkoppling. För att hålla dessa kraftverk igång övervakar och reparerar cellerna ständigt tusentals mitokondriella proteiner, en process som kallas mitokondriell protein-kvalitetskontroll. Hittills var det oklart hur denna kvalitetskontroll hänger ihop med hur pankreastumörer skaffar sig näring.
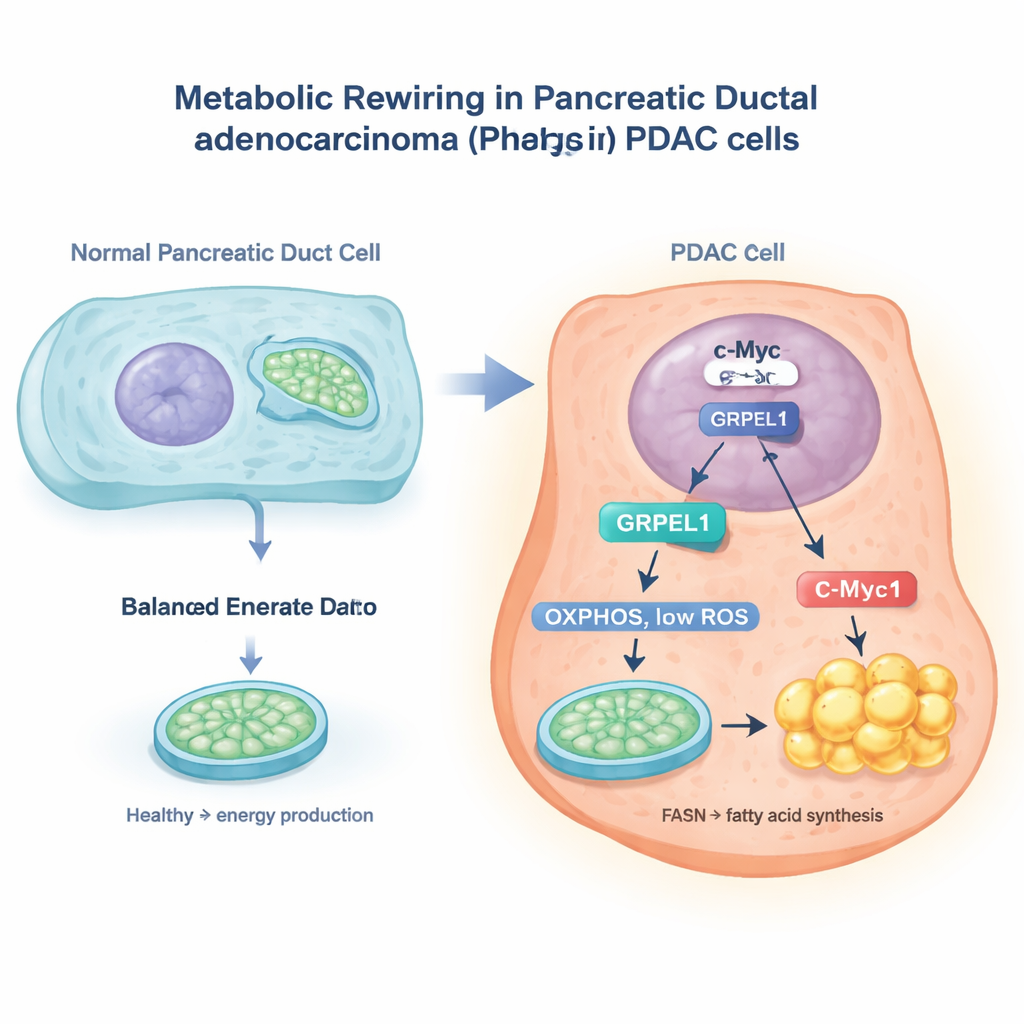
c-Myc-omkopplaren och en mitokondriell hjälpare
Forskarna använde stora cancer-databaser och experiment i pankreascellinjer för att rikta in sig på ett protein kallat GRPEL1, en hjälpare som deltar i hanteringen av mitokondriella proteiner. De upptäckte att den välkända cancergenen c-Myc fungerar som en molekylär omkopplare i cellkärnan som slår på GRPEL1-genen. När c-Myc-nivåerna minskade föll även GRPEL1-nivåerna; när c-Myc ökade steg GRPEL1. Patientprover visade också att c-Myc och GRPEL1 ofta är höga samtidigt, och båda var kopplade till sämre prognos. I odlingar av PDAC-celler saktade minskad GRPEL1 ner celldelning och koloniutveckling, medan extra GRPEL1 fick cellerna att proliferera snabbare, särskilt när c-Myc annars var blockerat.
Från mitokondrier till fettproduktion
Vid fördjupade studier fann teamet att GRPEL1 gör mer än att bara hålla ordning på mitokondriella proteiner. När GRPEL1 utarmades blev mitokondrierna i PDAC-celler mindre effektiva på att producera energi, förlorade sin normala form och släppte ut mer reaktiva syreföreningar (ROS) — kemiskt reaktiva biprodukter som ibland kallas cellulär ”rost”. Denna ökade mängd ROS fick en följdeffekt: nivåerna av fettsyrasyntas (FASN), ett nyckelenzym som bygger nya fettsyror i cellen, sjönk. Med FASN nedreglerat tillverkade cellerna färre fetter, lagrade mindre lipider och deras tillväxt bromsades upp. När forskarna tog bort ROS med en antioxidant återhämtade sig FASN-nivåerna, vilket visar att kopplingen mellan GRPEL1 och FASN drivs av ROS. Intressant nog verkade inte c-Myc direkt slå på FASN-genen i detta system, utan påverka FASN indirekt via GRPEL1 och mitokondriell stress.
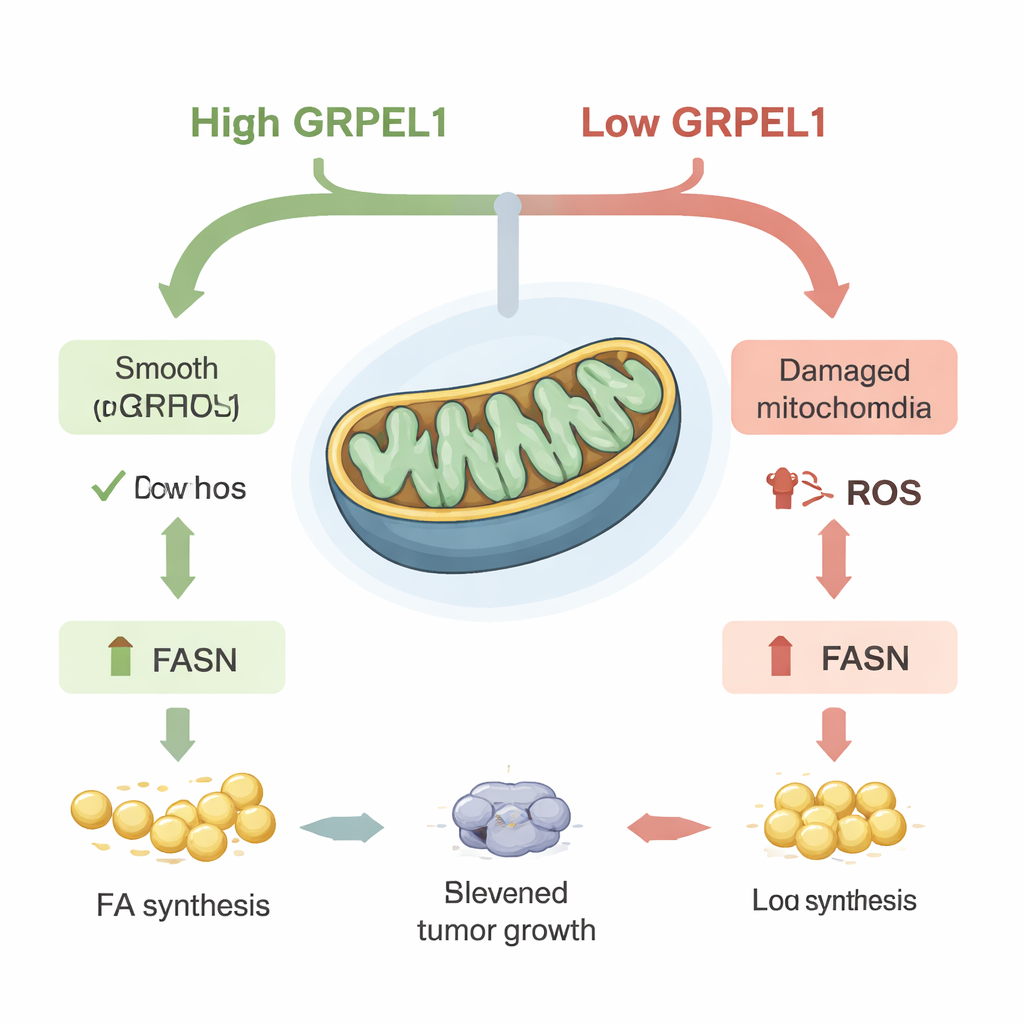
Fett som bränsle för tumörtillväxt
Där FASN står i centrum för fettbyggandet frågade sig forskarna om återinförande av FASN kunde rädda tumörcelltillväxten när GRPEL1 var låg. I cellodlingar vände tvingad överuttryck av FASN delvis den tillväxthämning och minskade koloniutveckling som orsakades av förlust av GRPEL1. Samma mönster sågs i möss: tumörer bildade av GRPEL1-utarmade celler växte långsammare, men återintroduktion av FASN återupplivade både tumörstorlek och fettinnehåll. Detaljerade analyser av metaboliter och lipider visade breda minskningar i många fettrelaterade molekyler när GRPEL1 eller c-Myc sänktes. Viktigt var att tillsats av extra fettsyror eller en lipidblandning utifrån delvis återställde tillväxten både i cancercellinjer och i patientderiverade pankreasorganoider — mini-tumörer odlade i 3D — vilket tyder på att huvudproblemet var förlusten av nyproducerade fetter.
Att förvandla en sårbarhet till terapi
Sammantaget ger arbetet en tydlig bild: i pankreascancer höjer c-Myc GRPEL1, vilket hjälper mitokondrierna att fungera smidigt och håller ROS i schack. Denna lugna mitokondriella miljö tillåter cellerna att upprätthålla höga nivåer av FASN, som pumpar ut nya fettsyror som fungerar som byggstenar för membraner, energilagring och tillväxtsignaler. När GRPEL1 blockeras sviktar mitokondrierna, ROS ökar, FASN sjunker och cancercellerna får svårt att växa — en effekt som delvis kan kringgås om fett tillförs utifrån. För lekmannen är slutsatsen att pankreastumörer är beroende av en intern ”fettfabrik”-krets, driven av c-Myc, GRPEL1 och FASN. Läkemedel som stör denna fettbyggande axel, särskilt i tumörer där den är mycket aktiv, kan erbjuda en lovande ny väg för att svälta ut pankreascancerceller samtidigt som normala vävnader påverkas mindre.
Citering: Wang, J., Zhang, L., Chen, K. et al. c-Myc/GRPEL1 maintains fatty acid synthesis via FASN to support PDAC cell proliferation. Cell Death Dis 17, 205 (2026). https://doi.org/10.1038/s41419-026-08439-0
Nyckelord: bukspottkörtelcancer, tumörmetabolism, fettsyrasyntes, mitokondrier, c-Myc