Clear Sky Science · sv
KDM5B samarbetar med CRL4B-komplexet för att främja tumörbildning hos ER+-bröstcancer genom att reglera kolesterolmetabolism
Varför denna forskning är viktig för vardagshälsa
Bröstcancer är den vanligaste cancern hos kvinnor, och många tumörer växer som svar på hormonet östrogen. Dessa cancerformer gör mer än att bara dela sig snabbt — de omprogrammerar också hur de använder fetter som kolesterol. I denna studie avslöjas hur ett genreglerande protein kallat KDM5B slår sig ihop med ett annat proteinkomplex, CRL4B, för att öka kolesterolnivåerna i östrogenreceptor‑positiva (ER+) bröstcancerceller. Genom att förstå detta dolda partnerskap hoppas forskare kunna hitta nya sätt att bromsa tumörtillväxt och förbättra befintliga behandlingar, såsom hormonbehandling och kolesterolsänkande läkemedel.
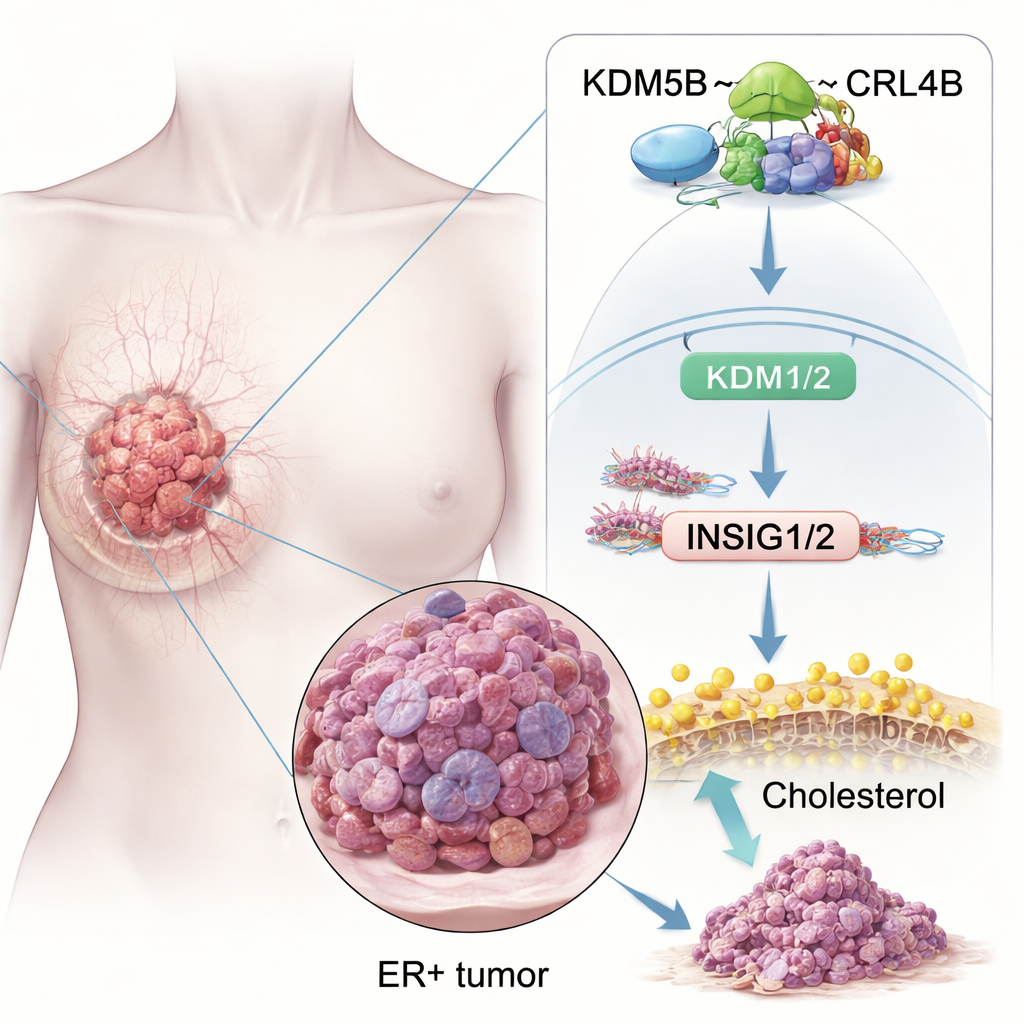
Ett protein som tippar balansen mot cancer
Forskarnas första fråga var om KDM5B bara finns närvarande i ER+ bröstcancer eller om det faktiskt bidrar till sjukdomen. Genom att analysera stora cancerregister och vävnadsprover fann de att KDM5B-nivåer är högre i brösttumörer än i normal bröstvävnad, och särskilt höga i ER+ tumörer. Patienter vars tumörer uttrycker mer KDM5B tenderar att ha sämre överlevnad, även när de får standard kemoterapi eller hormonbehandling. I cellkulturer ledde ökat KDM5B till att ER+ bröstcancerceller växte snabbare, invaderade omgivande vävnad lättare och bildade fler stamliknande kluster, vilka tros ge upphov till nya tumörer. Att minska KDM5B gav motsatt effekt och krympte kolonier i odlingsskålar och tumörer i möss.
Ett kraftfullt partnerskap inne i cancerceller
För att förstå hur KDM5B utövar sina effekter sökte teamet efter dess proteinpartners. De upptäckte att KDM5B fysiskt binder till delar av ett molekylärt maskineri kallat CRL4B‑komplexet, ett enzymatiskt system som märker proteiner och också förändrar hur DNA packas. Detaljerade biokemiska tester visade att KDM5B direkt interagerar med två CRL4B‑komponenter, CUL4B och DDB1, via specifika regioner i varje protein. I ER+ bröstcancerceller agerar detta KDM5B–CRL4B‑komplex på många gener vid deras av/på‑regleringsställen. Genom genomsnittlig kartläggning över hela genomet fann författarna att KDM5B och CUL4B ofta sitter tillsammans vid genpromotorer, där de ändrar kemiska märken på histonproteiner — spolarna som DNA är lindat runt — för att dämpa genuttryck.
Att släppa bromsen på kolesterol
Bland många påverkade vägar framträdde kolesterolmetabolism tydligt. Cancerceller behöver extra kolesterol för att bygga membran och klara stress, och ER+ tumörer använder också kolesterol‑deriverade molekyler för att efterlikna östrogen. Studien visar att KDM5B–CRL4B‑komplexet binder direkt till regleringsregionerna för två nyckel‑"broms"‑gener, INSIG1 och INSIG2. Dessa gener hjälper normalt till att hålla en huvudregulator av kolesterol, SREBP2, under kontroll. KDM5B–CRL4B tillför en repressiv markör (H2AK119ub1) och tar bort en aktiverande markör (H3K4me3) på histoner vid INSIG1/2‑promotorerna, vilket dämpar dessa gener. Med färre INSIG1/2‑proteiner frigörs SREBP2 för att slå på kolesterolproducerande gener, vilket höjer kolesterolnivåerna inne i ER+ bröstcancerceller och ökar deras invasiva beteende. När forskarna störde KDM5B eller CRL4B steg INSIG1/2, SREBP2‑aktiviteten föll och det totala kolesterolet i cellerna minskade.
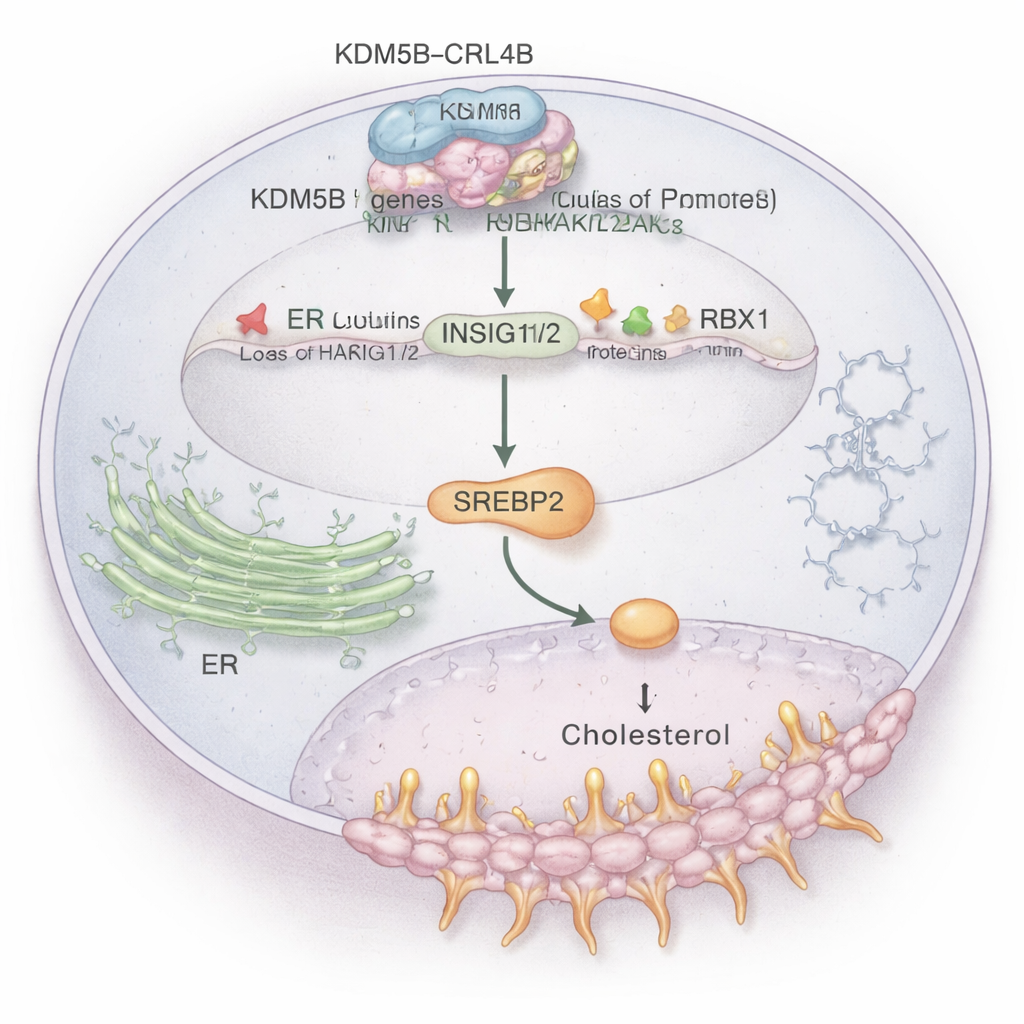
Kolesterolläkemedel och cancersignaler möts
Arbetet kopplar också denna bana till en kolesterol‑deriverad signal kallad 27‑hydroxykolesterol (27‑HC), en molekyl som redan är känd för att främja ER+ bröstcancer. Behandling av ER+ celler med 27‑HC ökade KDM5B‑nivåerna och undertryckte ytterligare INSIG1/2, vilket drev cellerna mot ökad tillväxt och invasion. Viktigt är att blockering av KDM5B eller CRL4B dämpade dessa aggressiva effekter, vilket tyder på att 27‑HC delvis verkar genom att mata in i KDM5B–CRL4B‑axeln. Separat visade forskarna att simvastatin, en allmänt använd kolesterolsänkande statin, bromsade bröstcancercellernas tillväxt, och när den kombinerades med en KDM5B‑hämmare blev antitumoreffekten starkare. Detta antyder att en kombination av läkemedel som riktar sig mot kolesterolproduktion och läkemedel som riktar KDM5B:s genreglerande aktivitet kan vara en lovande terapeutisk strategi.
Vad detta innebär för patienter och framtida behandlingar
Denna studie avslöjar en ny händelsekedja inne i ER+ bröstcancerceller: en kolesterolrelaterad signal (27‑HC) ökar KDM5B; KDM5B slår sig ihop med CRL4B‑komplexet för att stänga av INSIG1 och INSIG2; detta frigör SREBP2, ökar kolesterolproduktionen och hjälper tumörer att växa, invadera och upprätthålla stamliknande celler. Eftersom KDM5B också är förhöjt och kopplat till dålig överlevnad i flera andra cancerformer kan blockering av detta protein — eller återställande av INSIG1/2‑bromsarna — erbjuda nya sätt att kontrollera tumörtillväxt. Även om mer arbete krävs innan detta kan bli rutin i vården framhäver fynden hur tätt cancers beteende är knutet till vardagliga molekyler som kolesterol, och hur befintliga läkemedel som statiner en dag kan kombineras med epigenetiska terapier för att förbättra utfallen.
Citering: Yang, Y., Gao, T., Yuan, B. et al. KDM5B cooperates with CRL4B complex to promote the tumorigenesis of ER+ breast cancer via regulating cholesterol metabolism. Cell Death Dis 17, 207 (2026). https://doi.org/10.1038/s41419-026-08438-1
Nyckelord: ER-positiv bröstcancer, kolesterolmetabolism, KDM5B, INSIG1/INSIG2, epigenetisk terapi