Clear Sky Science · sv
LAP2α driver brösttumörbildning genom att dämpa replikationsstress
Varför detta är viktigt för bröstcancer
Brösttumörer växer delvis därför att cancerceller hittar sätt att överleva det konstanta trycket när de kopierar sitt DNA. Denna studie avslöjar hur ett mindre känt protein, kallat LAP2α, hjälper bröstcancerceller att skydda sitt DNA under replikationen, vilket främjar tumörtillväxt och gör cancer svårare att behandla. Att förstå detta dolda stödsystem öppnar för nya sätt att försvaga tumörer och förbättra effekten av befintliga läkemedel.
En dold hjälpare inne i tumörcellernas kärnor
Varje gång en cell delar sig måste den kopiera sitt DNA noggrant. I cancerceller är denna process särskilt ansträngd: tillväxtsignaler sitter fast i ett ”på”-läge och replikationsmaskineriet pressas till sina gränser. Det här trycket, känt som replikationsstress, lämnar segment av enkelsträngat DNA som snabbt måste täckas och stabiliseras av ett proteinkomplex kallat RPA. Författarna har tidigare visat att LAP2α, ett protein kopplat till cellkärnans interna stomme, kan binda RPA och hjälpa det att nå skadat DNA. I det här arbetet undersökte de om partnerskapet mellan LAP2α och RPA faktiskt driver brösttumörutveckling och påverkar hur tumörer svarar på behandling.
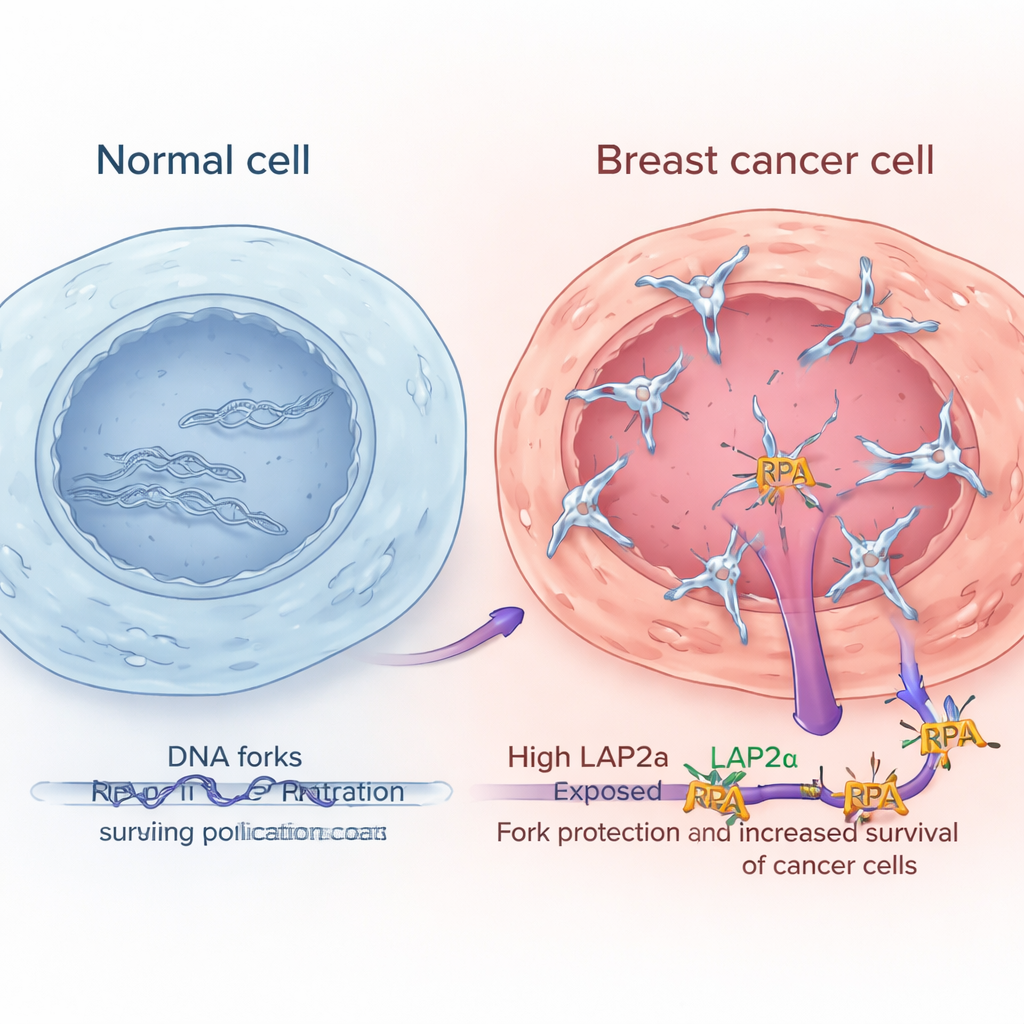
Höga nivåer av LAP2α kännetecknar mer aggressiva brösttumörer
Genom att analysera stora publika genuttrycksdatamängder och granska tumörprover i mikroskop visade forskarna att LAP2α konsekvent är högre i bröstcancervävnad än i närliggande normal bröstvävnad. Dess nivåer ökar med tumörgrad, vilket innebär att mer abnorma och aggressiva cancerformer tenderar att ha mer LAP2α. Detta mönster framträdde över flera stora bröstcancersubtyper, inklusive hormonreceptorpositiva, HER2-berikade och trippelnegativa tumörer. Viktigt för patienter var att de vars tumörer hade höga LAP2α-nivåer ofta hade sämre överlevnad. I kontrast visade inte RPA:s kärnkomponenter samma förändringar eller tydliga samband med utfall, vilket tyder på att det är LAP2α:s förstärkta funktion — snarare än enbart mer RPA — som hjälper cancerceller att bättre hantera replikationsstress.
Att stänga av LAP2α bromsar tumörer och blottar svagheter
För att gå bortom korrelationer använde teamet musmodeller för bröstcancer där LAP2α kunde väljas bort selektivt. När mammatumörer väl hade bildats ledde genetisk borttagning av LAP2α till att tumörerna växte långsammare och förlängd överlevnad hos djuren. Tumörceller utan LAP2α delade sig mindre och bar på fler tecken på DNA-skador, vilket visades av ökad färgning för markörer för DNA-brott och minskat RPA-skydd på DNA. När dessa LAP2α-bristfälliga tumörceller transplanterades till nya möss bildade de återigen mindre tumörer och visade förhöjd känslighet för DNA-skadande kemoterapi, inklusive platina-läkemedlet cisplatin och en PARP-hämmare. Liknande experiment i humana bröstcancercellinjer bekräftade att minskad LAP2α gjorde celler mer sårbara för flera genotoxiska läkemedel, medan återställande av normalt LAP2α — men inte en mutantform som inte kan binda RPA — räddade både DNA-skyddet och läkemedelsresistensen.
Hur LAP2α hjälper till att skydda sköra DNA-strängar
För att dissekera mekanismen återuppbyggde forskarna DNA-bindningsstegen i provrörsassay. De blandade renat RPA, enkelsträngat DNA och antingen normalt LAP2α eller en variant som inte kan interagera med RPA. De fann att LAP2α direkt ökade hur effektivt RPA täckte enkelsträngat DNA och hjälpte RPA att sträcka ut och stabilisera dessa ömtåliga regioner, fungerande som en slags lastningshjälpare eller chaperon. När DNA var närvarande tenderade RPA att lämna LAP2α och fullt ut binda den enkla strängen, vilket visar att LAP2α inte ingår i den slutliga skyddande beläggningen utan i stället överlämnar RPA till DNA. Utan en fungerande LAP2α–RPA-interaktion kollapsade fler replikationsgafflar, DNA-brott ackumulerades och cancerceller var mer benägna att dö, särskilt när ytterligare skada inducerades av kemoterapi.
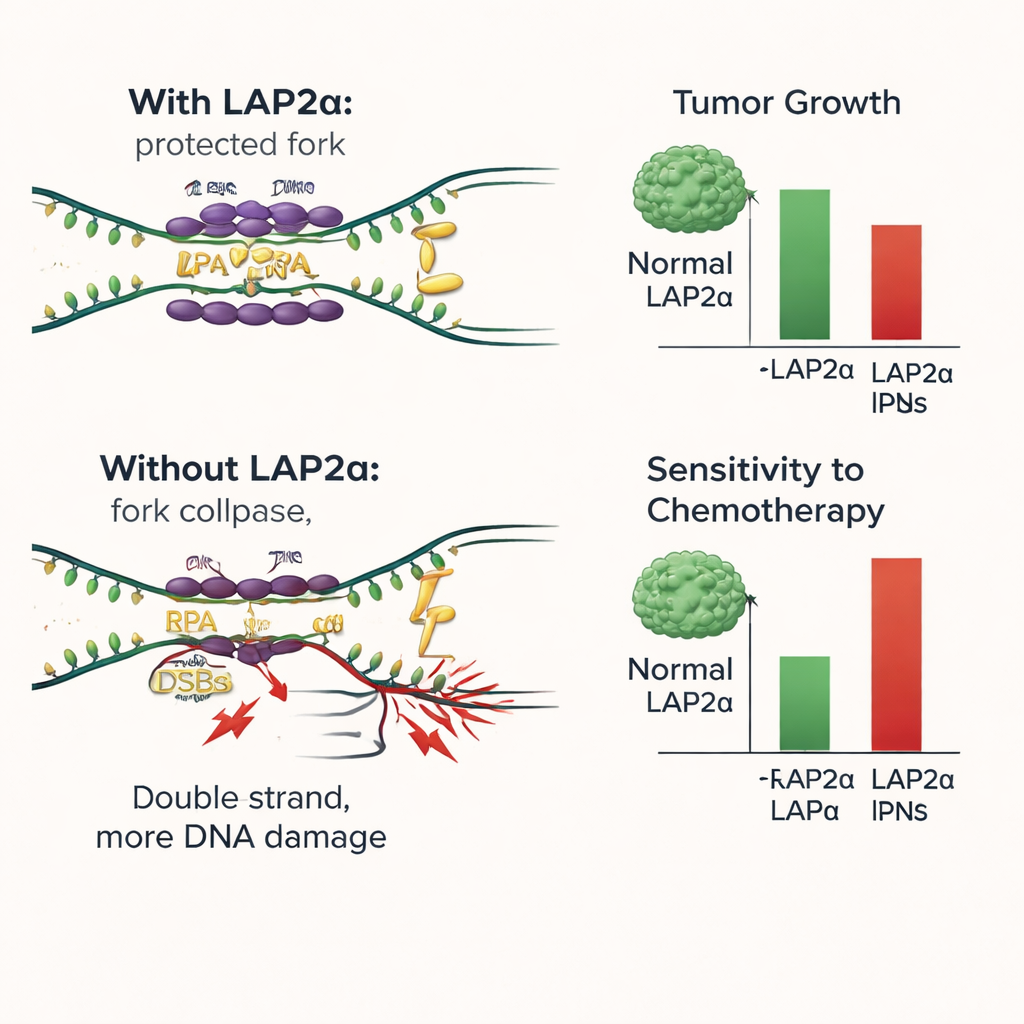
Vad detta betyder för framtida bröstcancerbehandling
Enkelt uttryckt visar denna studie att LAP2α fungerar som en kulissassistent som hjälper bröstcancerceller att överleva ansträngningen att kopiera sitt DNA. Genom att effektivt lasta RPA på sårbart DNA minskar LAP2α skador och stöder fortsatt tumörtillväxt. Att ta bort eller inaktivera LAP2α tippar balansen: DNA-skador hopar sig, cellerna slutar dela sig och konventionella läkemedel som angriper DNA blir mer effektiva. Dessa fynd tyder på att LAP2α kan användas som en markör för sämre prognos och som ett nytt terapeutiskt mål. Läkemedel som blockerar LAP2α eller dess grepp om RPA kan göra befintliga behandlingar såsom platinaagenter och PARP-hämmare mer verksamma, särskilt i tumörer som i hög grad förlitar sig på detta stressdämpande system.
Citering: Ma, Y., Qin, Y., Bao, P. et al. LAP2α drives breast tumorigenesis by mitigating replication stress. Cell Death Dis 17, 201 (2026). https://doi.org/10.1038/s41419-026-08433-6
Nyckelord: bröstcancer, DNA-replikationsstress, LAP2 alpha, replicationsprotein A, känslighet för kemoterapi