Clear Sky Science · sv
Att rikta in sig på glycerofosfolipid‑biosyntes övervinner kemoresistens orsakad av SLFN11‑förlust i Ewing‑sarkom
Varför denna forskning är viktig för barncancer
Ewing‑sarkom är en sällsynt men aggressiv cancer som främst drabbar barn och tonåringar. Många patienter svarar initialt väl på kemoterapi, men för dem vars cancer återkommer fungerar dagens behandlingar ofta dåligt. Denna studie ställer en angelägen fråga: när Ewing‑sarkomceller blir resistenta mot kemoterapi, vilka förändringar inom dem hjälper dem att överleva — och kan dessa förändringar bli nya svagheter som läkare kan rikta in sig på?
En gen som gör cancerceller lättare att döda
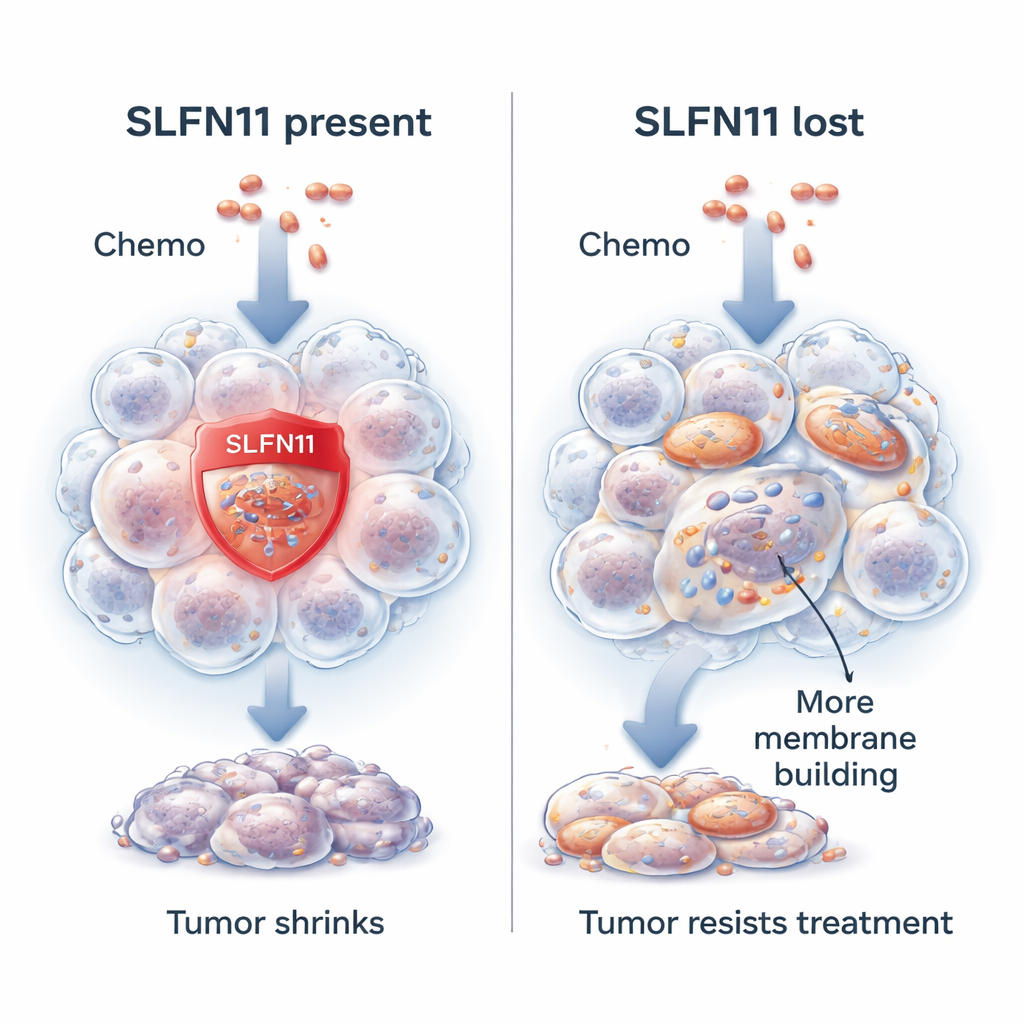
Forskarnas fokus ligger på en gen som heter SLFN11. I många Ewing‑sarkomtumörer är SLFN11 mycket aktiv och gör cancerceller betydligt mer känsliga för läkemedel som skadar DNA, cellens genetiska ritning. När dessa läkemedel ges hjälper SLFN11 till att stänga ner DNA‑reparation och driver cancercellen mot död. Patienter vars tumörer har högre nivåer av SLFN11 tenderar att leva längre och svara bättre på behandling. Men omkring en av tio tumörer har antingen lite eller inget SLFN11 från början eller förlorar det under behandlingens gång. När det händer blir samma kemoterapi mycket mindre effektiv, samtidigt som cancercellerna fortfarande kan växa normalt.
Hur cancerceller omkopplar sin användning av bränsle och fetter
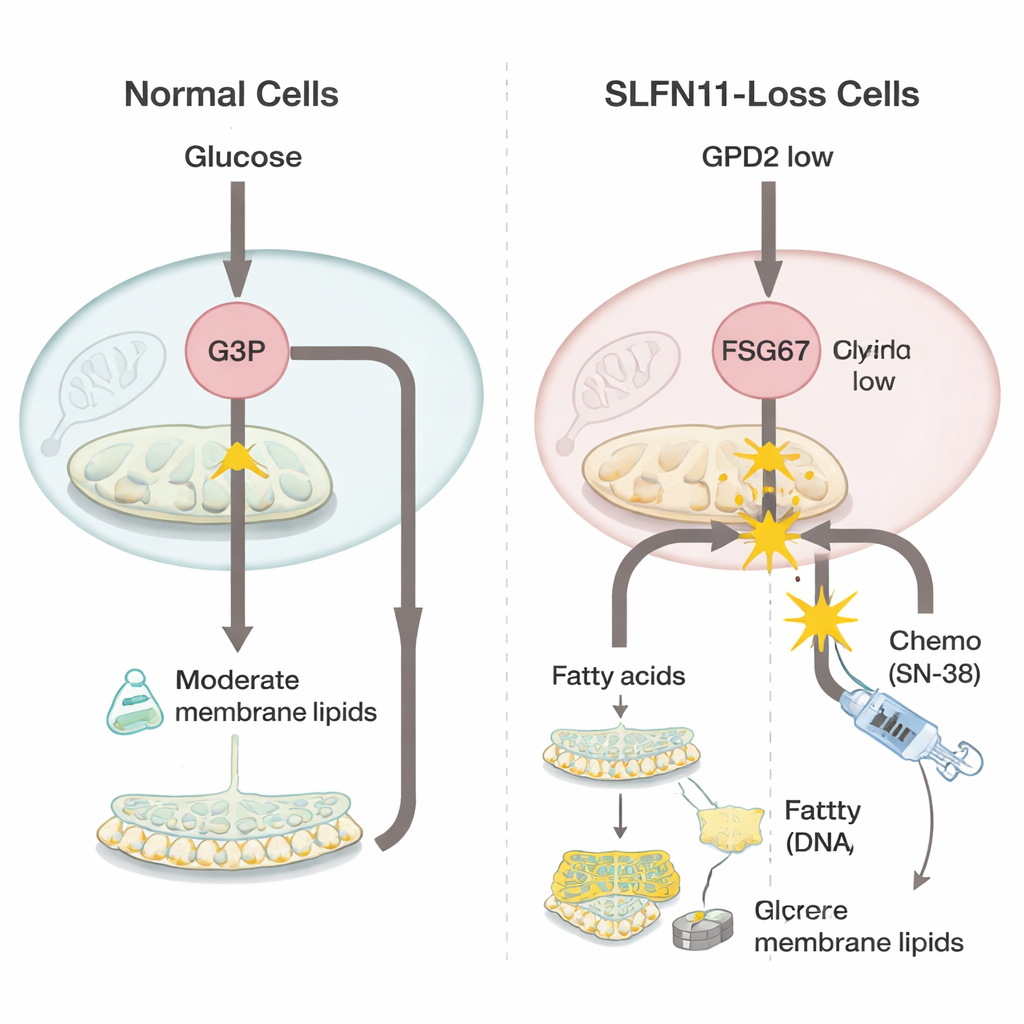
För att förstå vad som förändras när SLFN11 förloras jämförde teamet Ewing‑sarkomceller med och utan denna gen med kraftfulla ”omik”‑verktyg som mäter tusentals gener och små molekyler samtidigt. De upptäckte att celler utan SLFN11 nedreglerar ett enzym i sina mitokondrier som kallas GPD2, vilket normalt hjälper till att förbränna molekylen glycerol‑3‑fosfat som en del av energiproduktionen. När GPD2 minskar byggs glycerol‑3‑fosfat upp. Istället för att gå till spillo omdirigeras denna extra byggsten till att tillverka fler fetämnen som bildar cellmembran, en grupp som kallas glycerofosfolipider. Cellerna visade också tecken på att producera mer flexibla, omättade fetter, vilket kan hjälpa snabbt växande tumörer att anpassa sig till stress.
Att göra en överlevnadsstrategi till en svag punkt
Eftersom dessa SLFN11‑defekta celler lutar mer åt membranbygge testade forskarna om blockering av denna process kunde återställa känsligheten för kemoterapi. De använde en förening kallad FSG67, som hämmar ett nyckelsteg i produktionen av glycerofosfolipider. På egen hand hade det standardiserade DNA‑skadande läkemedlet SN‑38 blivit mycket mindre potent i SLFN11‑defekta celler, vilket speglar det kliniska problemet med resistens. Men när SN‑38 kombinerades med FSG67 drabbades de tidigare resistenta cellerna mycket hårdare, och de två läkemedlen samarbetade bättre än vad deras individuella effekter skulle förutsäga. I kontrast, i celler som fortfarande hade SLFN11 och redan var mycket känsliga för SN‑38, gav tillägg av FSG67 liten ytterligare nytta och kunde till och med vara något motproduktivt. Detta mönster tyder på att det nyfunna beroendet av fett‑ och membranproduktion är specifikt för det resistenta, SLFN11‑låga tillståndet.
En möjlig icke‑invasiv signal för svårbehandlade tumörer
Forskarna frågade sedan om denna metaboliska omkoppling kunde upptäckas i faktiska tumörer, inte bara i cellodling. De odlade Ewing‑sarkomtumörer i möss, med eller utan SLFN11, och använde kärnmagnetisk resonans (NMR) för att undersöka den kemiska sammansättningen i tumörextrakt. Tumörer utan SLFN11 visade en högre kvot av två kolin‑innehållande molekyler kopplade till membranomsättning: fosfocholin och glycerofosfocholin. En hög fosfocholin/glycerofosfocholin‑kvot har i andra cancerformer kopplats till mer aggressivt beteende och sämre behandlingssvar. Eftersom kolinsignaler kan mätas med avancerade bildtekniker kan denna typ av förändring en dag fungera som en icke‑invasiv markör för att flagga Ewing‑sarkomtumörer som antagit detta resistenta, membranbyggande läge.
Vad detta kan innebära för framtida behandlingar
Sammanfattningsvis visar studien att när Ewing‑sarkomceller förlorar SLFN11 och blir mindre känsliga för DNA‑skadande kemoterapi, kompenserar de genom att omkoppla sin metabolism mot att tillverka fler membranfetter. Denna förskjutning hjälper inte bara cellerna att överleva; den skapar också en ny akilleshäl. Att blockera glycerofosfolipidproduktion med ett läkemedel som FSG67 kan delvis återställa kemoterapins dödande effekt i dessa resistenta celler. Även om FSG67 i sig ännu inte är ett kliniskt godkänt läkemedel, pekar arbetet mot en strategi där läkare en dag kan matcha patienters tumörer efter SLFN11‑status och metabola egenskaper, och sedan kombinera DNA‑skadande terapier med riktade hämmare av fett‑ och membransyntes för att övervinna resistens.
Citering: Chakraborty, K., Burman, R., Satheesh, S. et al. Targeting glycerophospholipid biosynthesis overcomes chemoresistance driven by SLFN11 loss in Ewing sarcoma. Cell Death Dis 17, 190 (2026). https://doi.org/10.1038/s41419-026-08432-7
Nyckelord: Ewing‑sarkom, kemoresistens, SLFN11, cancermetabolism, lipidbiosyntes