Clear Sky Science · sv
Modulering av immunceller och metabol omprogrammering vid efferocytos
Hur våra kroppar tyst städar upp döende celler
Varje dag når miljarder av våra celler slutet på sin livstid. Ändå märker vi inte denna mikroskopiska omsättning, och vi blir inte sjuka av resterna. Denna tysta städning sköts av immunceller och vävnadsceller som känner igen och slukar döende celler, vilket förhindrar skadlig inflammation. Den granskade forskningen förklarar hur denna städprocess, kallad efferocytos, inte bara håller vävnader rena utan också omprogrammerar ämnesomsättningen i de celler som utför städningen, och därigenom påverkar om vårt immunsystem lugnar ned sig, bekämpar infektioner eller—om något går fel—bidrar till sjukdom.
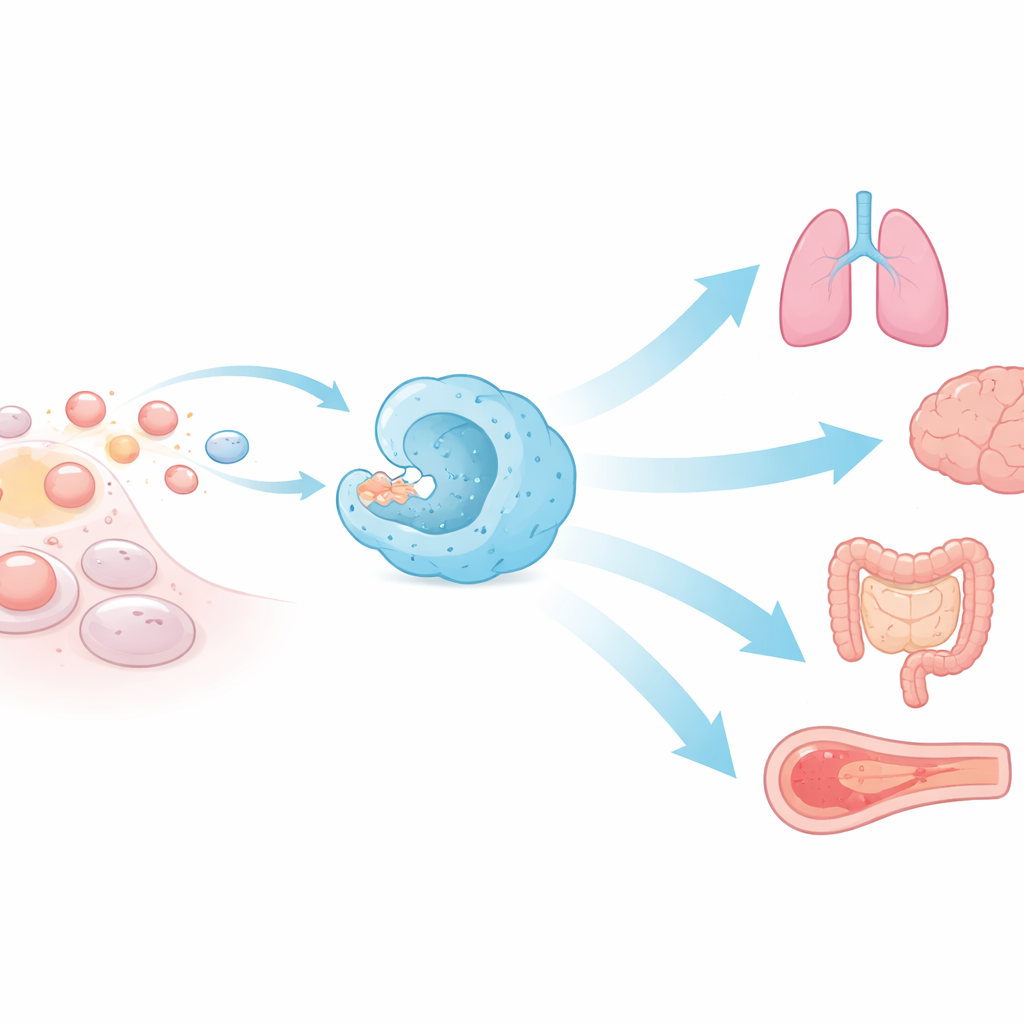
Kroppens tysta sophämtare
Efferocytos är namnet på upptag och borttagning av apoptotiska, det vill säga programmerat döende, celler. Specialiserade immunceller som makrofager och dendritiska celler utför det mesta av detta arbete, men många icke-immunceller—såsom epitelceller i tarm, lunga, öga och testiklar—kan också rycka in. Döende celler skickar ut kemiska "hitta mig"-signaler som attraherar närliggande städceller, och visar sedan "ät mig"-flaggor på ytan samtidigt som de stänger av "ät inte mig"-signaler. När de väl känns igen omsluts de i en membranficka, dras in och bryts ner i enzymfyllda compartment. Denna snabba, mångstegs-koreografi förklarar varför apoptotiska celler sällan ses i mikroskop trots den massiva dagliga cellförlusten.
Städning som skyddar organen
Effektiv efferocytos skyddar strukturen och funktionen hos många organ. I ögat leder underlåtenhet att rensa bort döende fotoreceptorfragment i näthinnan till synförlust. I testiklarna kan bristfällig borttagning av döende könsceller orsaka infertilitet. Under graviditet främjar efferocytos av placentaceller maternell tolerans genom att dämpa inflammatoriska molekyler och öka lugnande faktorer. I hjärnan beskär mikroglia överflödiga neuroner och stödjer en hälsosam anslutningsstruktur, medan i tarmen rensar Paneth-celler och andra fagocyter upp döende celler för att förhindra kronisk tarminflammation. I lungorna tar luftvägsmakrofager kontinuerligt bort döda celler och undviker utsläpp av fara-signaler som kan driva fram astma, kronisk obstruktiv lungsjukdom eller svåra virusskador.
När infektioner gör städningen till ett dubbelsidigt vapen
Vid infektioner blir efferocytos mer komplex. Patogener utlöser ofta celldöd, och den efterföljande upptagningen av infekterade lik kan antingen försvaga eller stärka värdförsvaret. Vissa virus och bakterier utnyttjar den antiinflammatoriska sidan av efferocytos för att gömma sig från immunangrepp eller för att spridas, genom att använda uppslukade vesiklar som "Trojanska hästar." I andra sammanhang levererar intag av infekterade döda celler mikrobiella fragment till makrofager och dendritiska celler, som sedan presenterar dessa fragment för T-celler och mobiliserar skyddande immunsvar. Beroende på mikroben och vävnaden kan efferocytos styra T-hjälparceller mot olika immunprofiler, vilket antingen stödjer bakteriell eliminering eller—om själv-molekyler presenteras tillsammans med mikrobiella—leder till uppkomsten av autoreaktiva T-celler som angriper kroppens egna vävnader.
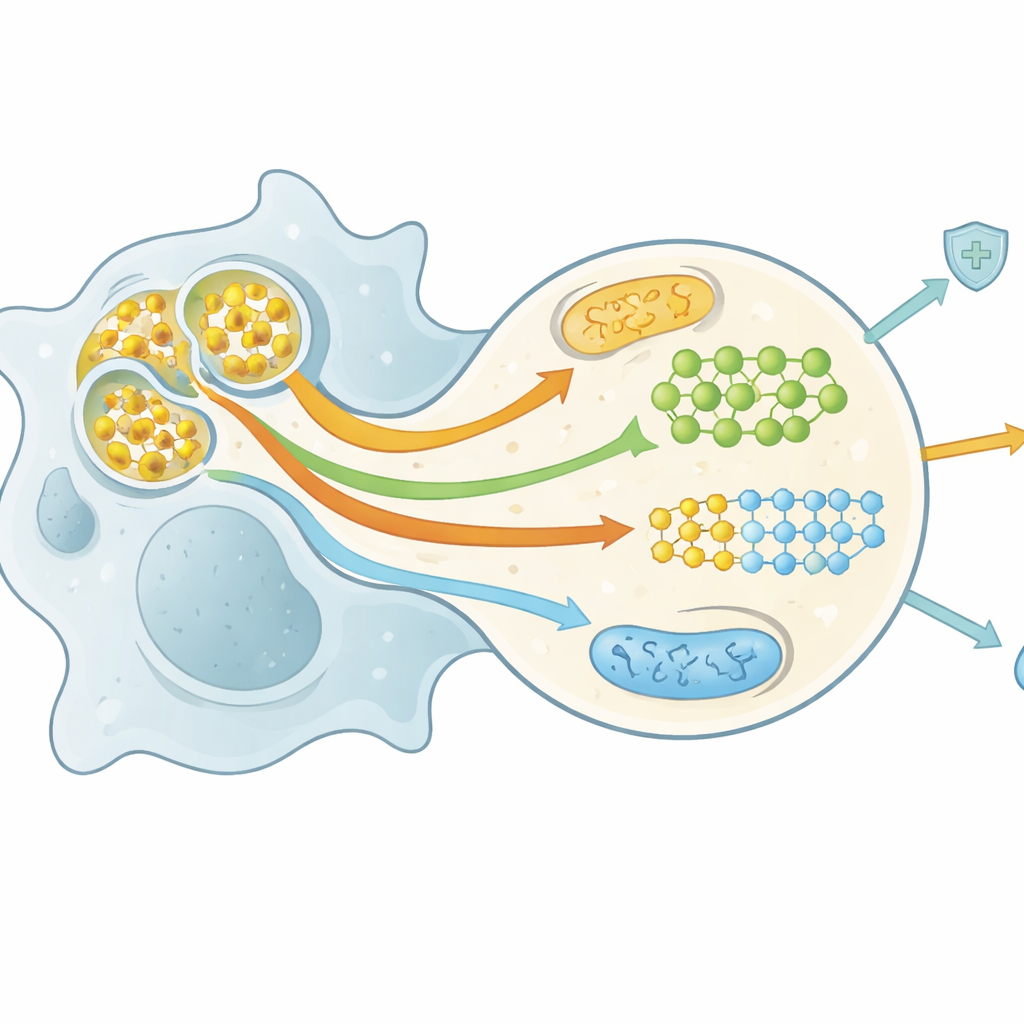
Näring från de fallna: hur ämnesomsättningen omprogrammeras
Att bryta ner en hel cell är metabolt krävande, men det översvämmar också städcellen med näringsämnen—lipider, sockerarter, aminosyror och nukleotider. Författarna beskriver ett växande fält, ibland kallat efferotabolism, som följer hur denna näringsökning omprogrammerar ämnesomsättningen hos makrofager och dendritiska celler. Lipider från döende celler aktiverar nukleära receptorer som ökar kolesterolexport, stödjer mitokondriell fettoxidation och främjar ett antiinflammatoriskt, vävnadsreparerande tillstånd. Aminosyror såsom arginin, metionin och tryptofan återvinns till molekyler som driver upprepade omgångar av upptag och utlöser pro-resolverande signaler. Korta utbrott av glukosnedbrytning och relaterade vägar förser med energi, upprätthåller redoxbalans och hjälper till att hålla receptorer och membran i rätt tillstånd för kontinuerlig städning. Dessa sammanflätade metaboliska förändringar avgör om de efferocytiska cellerna förblir toleranta, växlar till reparationsläge eller behåller stark antimikrobiell aktivitet.
Öppna frågor och framtida behandlingsvägar
Översikten betonar att inte alla efferocyter, eller cellätare, beter sig lika. Professionella immunceller och vävnadsceller kan förlita sig på skilda metaboliska program, och olika former av celldöd—såsom nekros eller ferroptos—lämnar sannolikt olika metabola och immunologiska spår. Centrala obesvarade frågor inkluderar hur blandade signaler från både själv- och mikrobiella komponenter inne i samma döende cell formar energivägar och långsiktig immunitet. Genom att kartlägga dessa länkar mellan städning, metabolism och immunöde hoppas forskare utforma terapier som försiktigt styr efferocytos: förbättra den för att lösa kronisk inflammation och stödja sårläkning, eller finjustera den för att bevara antimikrobiell styrka utan att övergå i autoimmunitet. I korthet kan förståelsen för hur kroppen "äter" sina egna cellulära rester öppna nya sätt att hålla inflammation, infektion och tolerans i hälsosam balans.
Citering: Oliveira, K.C., Marcos, C.M., Penteado, L.d.A. et al. Modulation of immune cells and metabolic reprogramming in efferocytosis. Cell Death Dis 17, 257 (2026). https://doi.org/10.1038/s41419-026-08431-8
Nyckelord: efferocytos, immunologisk tolerans, medfödd immunitet, immunometabolism, kronisk inflammation