Clear Sky Science · sv
HSPA5 främjar stabilitet hos YAP/TAZ oberoende av Hippo‑vägen och inducerar proneural‑till‑mesenkymal övergång i glioblastom
Varför denna hjärntumörstudie är viktig
Glioblastom är en av de dödligaste hjärntumörerna, delvis eftersom många tumörer över tid skiftar till ett tuffare, mer behandlingsresistent tillstånd. Denna studie avslöjar hur ett vanligt stressresponsprotein, HSPA5, bidrar till det skiftet och håller tumörfrämjande molekyler vid liv längre än de borde vara. Att förstå detta ”överlevnadstrick” pekar på nya sätt att göra glioblastom mindre aggressivt och mer mottagligt för befintliga behandlingar.
En tumör som ändrar personlighet
Läkare och forskare vet nu att glioblastom inte är en enda sjukdom utan en blandning av molekylära subtyper. Två huvudsakliga varianter är en ”proneural” form, som tenderar att vara något mindre aggressiv, och en ”mesenkymal” form, som är mer invasiv, behandlingsresistent och förknippad med tidigare återfall. Tumörer kan utvecklas från proneural till mesenkymal status, en process författarna kallar proneural‑till‑mesenkymal‑övergång, eller PMT. Teamet bestämde sig för att ta reda på vilka stressresponsproteiner som kan driva tumörer längs denna farliga väg.
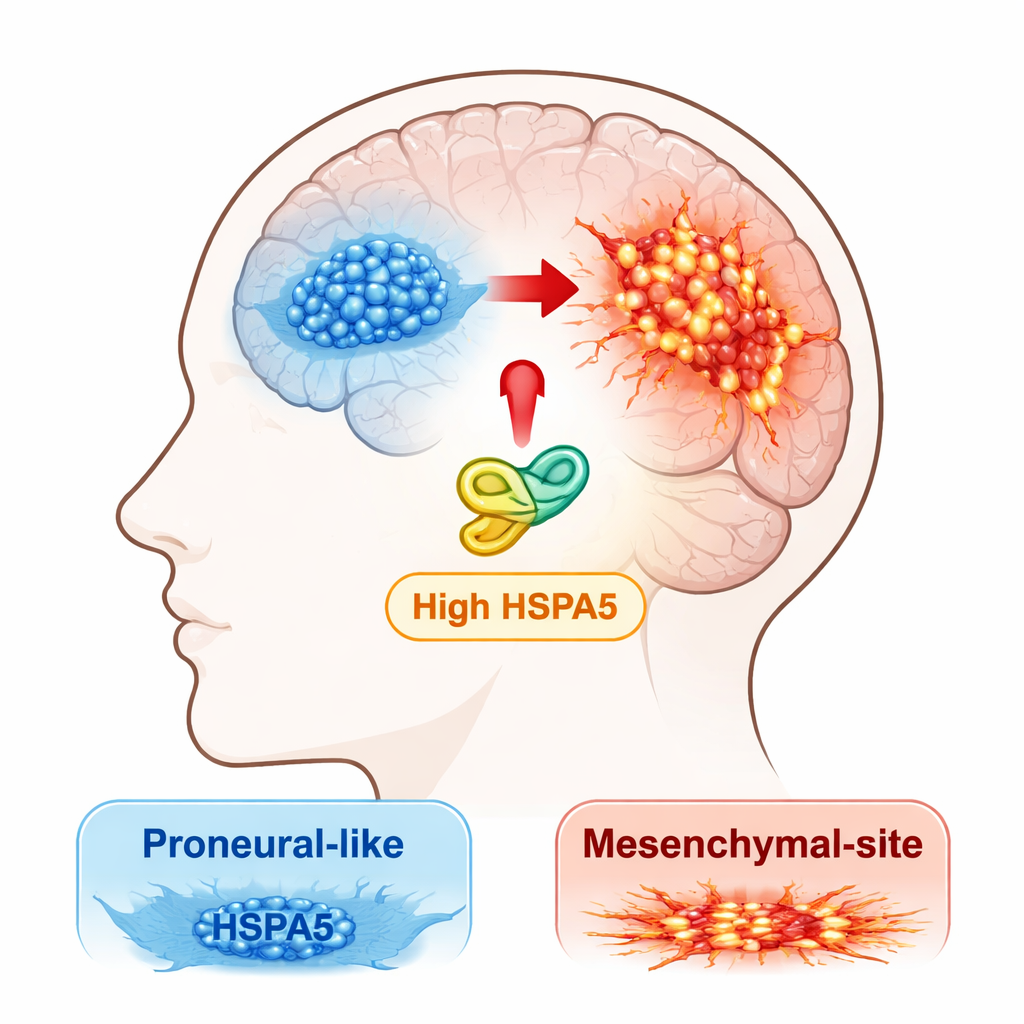
Ett stresshjälpprotein i rampljuset
Forskarna inledde med att genomsöka stora offentliga cancer‑databaser och sina egna patientprover efter medlemmar i HSP70‑familjen, en grupp ”chaperon”‑proteiner som hjälper andra proteiner att veckas rätt och överleva under stress. En chaperon, HSPA5, stack ut. Dess aktivitet var högst i den mesenkymala subtypen av glioblastom och markant högre i tumörer än i normal hjärnvävnad. Patienter vars tumörer hade högre HSPA5 tenderade att ha sämre total överlevnad, vilket framhåller proteinet som en möjlig drivkraft för aggressiv sjukdom snarare än en passiv åskådare.
Tvinga celler att bli mer aggressiva
För att undersöka vad HSPA5 faktiskt gör inne i tumörceller odlade teamet primära glioblastomceller som togs direkt från patienter och delade upp dem i proneural‑lika och mesenkymal‑lika grupper. När de tvingade proneurala celler att producera extra HSPA5 började dessa celler bete sig mer som mesenkymala celler: de delade sig snabbare, rörde sig och invaderade lättare samt slog på typiska mesenkymala markörer som CD44 och c‑MET, samtidigt som de sänkte proneurala markörer som SOX2 och OLIG2. Det motsatta gällde också — att minska HSPA5‑nivåerna i mesenkymala celler dämpade deras tillväxt och invasivitet och tryckte delvis tillbaka dem mot en mindre aggressiv profil.
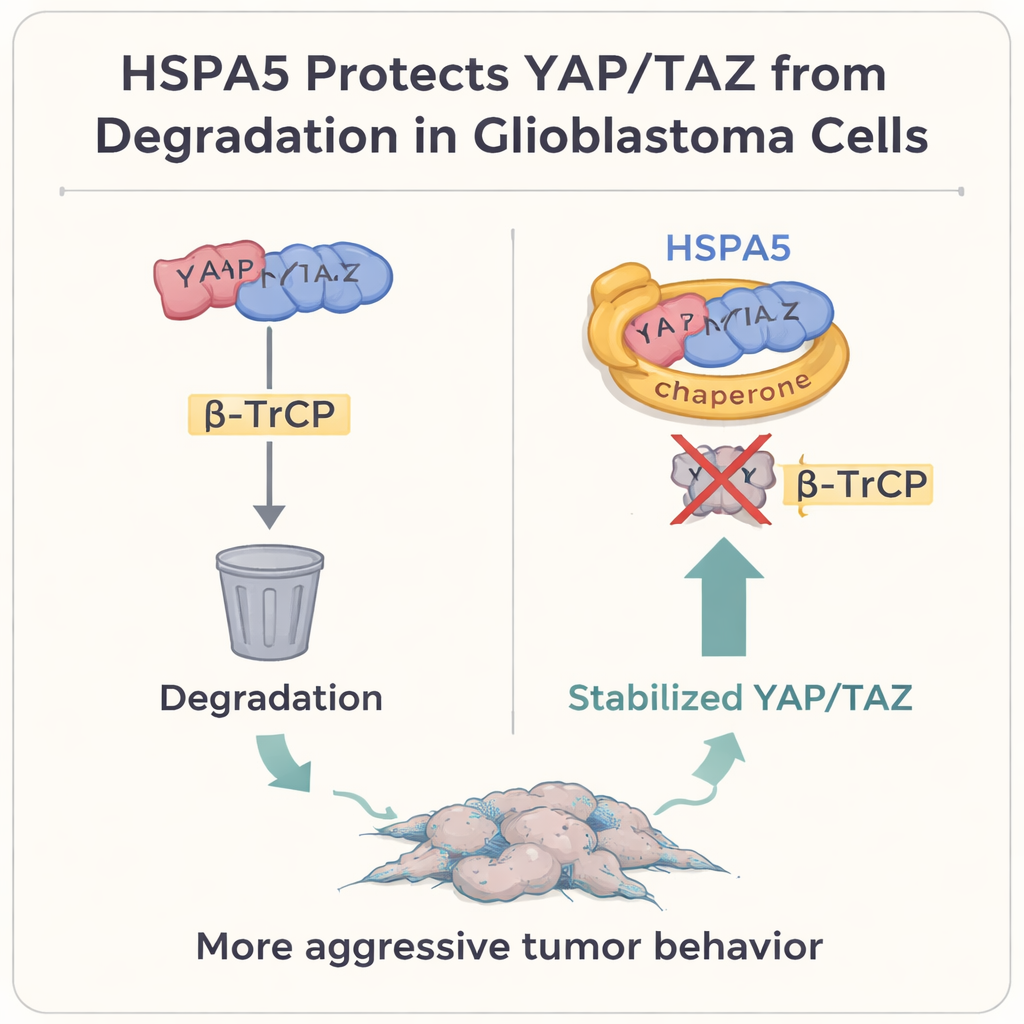
Skydda nyckelomkopplare från cellens sopnedkast
På djupet fokuserade författarna på två kraftfulla tillväxtregulatorer, YAP och TAZ, som ligger i centrum av Hippo‑signalvägen. I många solida tumörer, inklusive glioblastom, fungerar dessa proteiner som huvudomkopplare som främjar celltillväxt, plasticitet och den mesenkymala tillståndet. Normalt, när celler vill dämpa detta program, märker de YAP och TAZ för nedbrytning genom ett protein kallat β‑TrCP, som ledsagar dem till cellens ”soptunna”, proteasomen. Studien visar att HSPA5 fysiskt binder till YAP och TAZ, använder sin substratbindande domän som en skyddshandske. Genom detta blockerar den β‑TrCP från att fästa, hindrar YAP/TAZ från att ubiquitineras och brytas ner, och tillåter dem att ackumuleras i kärnan där de aktiverar mesenkymala gener, inklusive CD44 och c‑MET själva.
Från odlingsskålar och möss till patienttumörer
Teamet bekräftade denna mekanism på flera sätt. Att blockera HSPA5 gjorde att YAP‑ och TAZ‑proteiner försvann snabbare, såvida inte proteasomen kemiskt hämmades, och ökade deras ”sop‑tagg”‑signaler. Återaktivering av YAP och TAZ räddade den förlorade tillväxten och invasiviteten som uppstod när HSPA5 minskades, medan tystnad av YAP/TAZ utsläckte de tumörfrämjande effekterna av HSPA5‑överexponering. I musmodeller där mänskliga glioblastomceller implanterades i hjärnan växte tumörer med hög HSPA5 snabbare och dödade djuren tidigare; att sänka HSPA5 eller avbryta dess stöd för YAP/TAZ bromsade tillväxten och förlängde överlevnaden. Slutligen visade matchade mänskliga prover tagna från samma patienter före och efter återfall att återkommande, mer mesenkymala tumörer uppvisade högre nivåer av HSPA5, YAP, TAZ och mesenkymala markörer än de ursprungliga proneural‑lika tumörerna.
Vad detta innebär för framtida behandling av hjärncancer
Kort sagt tyder detta arbete på att glioblastomceller utnyttjar en stress‑respons‑hjälpare, HSPA5, för att skydda avgörande tillväxtomkopplare (YAP och TAZ) från nedbrytning. Det skyddet hjälper tumörer att skifta till och upprätthålla en mer aggressiv, behandlingsresistent identitet. Eftersom småmolekylära hämmare av HSPA5 redan finns och tumörceller kan vara mer beroende av denna chaperon än normala celler, erbjuder HSPA5–YAP/TAZ‑axeln ett lockande nytt mål. Terapier som försvagar denna skyddande sköld kan göra glioblastomceller mindre anpassningsbara, mindre invasiva och mer sårbara för standardbehandlingar såsom kemoterapi och strålbehandling.
Citering: Gui, S., Yu, W., Song, Z. et al. HSPA5 promotes YAP/TAZ stability independently of the Hippo pathway and induces proneural-to-mesenchymal transition in glioblastoma. Cell Death Dis 17, 208 (2026). https://doi.org/10.1038/s41419-026-08428-3
Nyckelord: glioblastom, HSPA5, YAP/TAZ, tumörplasticitet, mesenkymal övergång