Clear Sky Science · sv
p16-medierad G0/G1-cells cykelstopp leder till SASP och fibros i Fuchs endotelskörhet i hornhinnan
Varför denna ögonsjukdom är viktig
När människor blir äldre är ett av de mindre kända hoten mot synen en sjukdom kallad Fuchs endotelskörhet i hornhinnan (FECD), som gradvis gör ögats normalt klara främre fönster grumligt. Denna artikel undersöker varför vissa celler på hornhinnans inre yta slits ut och blir ärriga över tid, och varför kvinnor drabbas oftare. Att förstå dessa dolda förändringar kan öppna för läkemedel som fördröjer eller till och med förhindrar behovet av hornhinnetransplantationer.
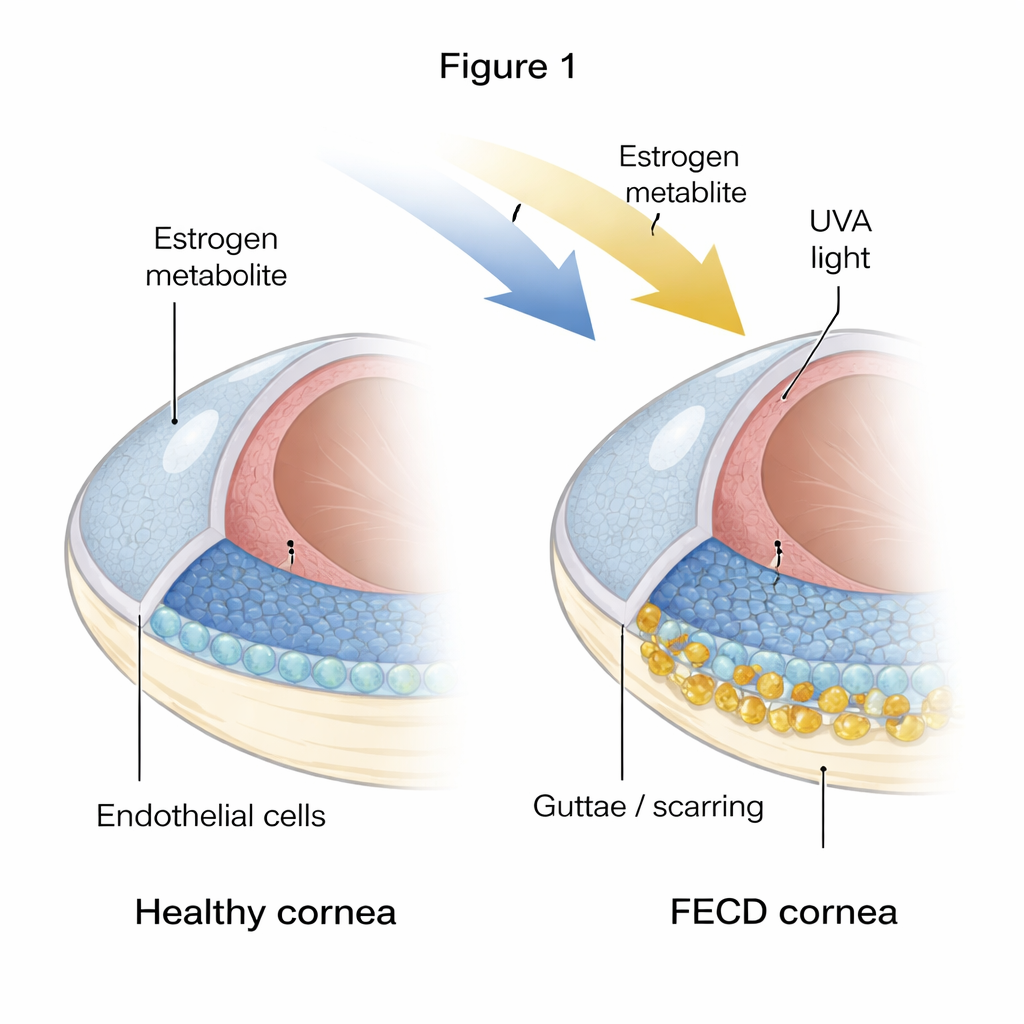
Hornhinnans sköra inre beklädnad
Hornhinnan måste hållas exakt avfuktad för att förbli genomskinlig, ett arbete som utförs av ett enkelt lager hexagonformade celler kallade korneala endotelceller. Vid FECD dör många av dessa celler och lagret blir fläckigt och oregelbundet. Samtidigt uppstår hårda knölar och förtjockat material, känt som guttae och överskott av extracellulär matrix, på den inre ytan. Författarna jämförde friska donatorhornhinnor med hornhinnor från FECD-patienter och fann starka tecken på att det sjuka vävnadsområdet både var ”åldrat” och fibrotiskt: cellerna visade markörer för senescens (ett permanent avstängt tillstånd) och för fibros (celler som beter sig mer som ärrbildande celler och lägger ner extra vävnad).
Kronisk ljus- och hormonstress driver celler mot ett återvändsgränd
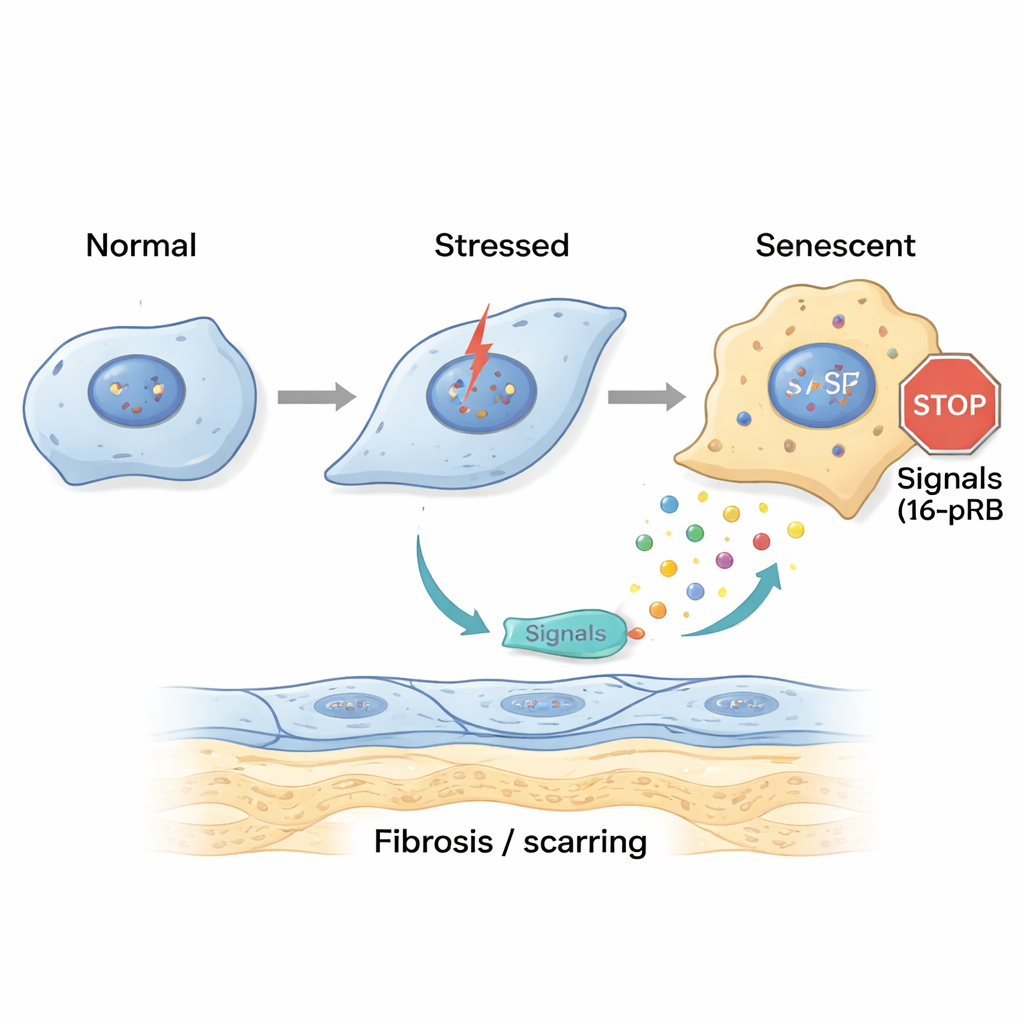
För att undersöka hur denna skada börjar reproducerade forskarna FECD-liknande stress i laboratoriet. De utsatte friska korneala endotelceller för UV-A-ljus och för 4-hydroxyestradiol, en oxiderad östrogenbiprodukt kopplad till DNA-skada. En kort, enkel påfrestning fick cellerna att tillfälligt stanna upp i ett sent stadium av cellcykeln och börja en tidig övergång mot ett mer fibroblastliknande tillstånd, men viss återhämtningsförmåga återstod. Däremot drev upprepad, kronisk exponering cellerna in i ett annat tillstånd: de samlades i ett tidigt cellcykelstadium kallat G0/G1 och slog på genen p16, som låser cellcykeln via sin partnerproteinet pRB. Dessa celler blev stora, platta och obestridligt senescenta, samtidigt som de starkt uttryckte fibrosmarkörer och proteiner som bygger upp de förtjockade guttae man ser i FECD.
Senescenta celler sänder skadliga signaler och sprider ärrbildning
Senescenta celler sitter inte bara stilla; de utsöndrar en blandning av signalsubstanser känd som det senescensassocierade sekretoriska fenomenet (SASP). Forskargruppen samlade vätska från stressade korneala celler och applicerade den på nya celler och på friska donatorhornhinnor. Den ”akuta” SASP orsakade tidiga tecken på formförändringar i cellerna, medan ”kronisk” SASP drev många celler in i senescens och ökade uttrycket av gener kopplade till fibros och extra matrixdeposition. Detaljtester visade att kronisk SASP var rik på inflammatoriska budbärare såsom IL-8 och IL-17, som är kända för att främja cellåldrande, fibrotisk ärrbildning och rekrytering av immunceller. När forskarna blockerade IL-17-vägen eller IL-8-receptorn CXCR2 visade celler exponerade för kronisk SASP färre senescensmarkörer och mindre fibros, vilket tyder på att dessa signaler är viktiga drivkrafter i sjukdomen.
Avlägsnande av utslitna celler för att skydda synen
Då p16-positiva senescenta celler var så starkt kopplade till ärrbildning testade författarna om eliminering av dem kunde skydda hornhinnan. I en musemodell där UV-A-ljus utlöser FECD-liknande förändringar behandlade de djuren med en senolytisk läkemedelskombination, Dasatinib plus Quercetin, som selektivt dödar senescenta celler. Jämfört med obehandlade möss behöll de senolytikabehandlade mössen ett mer regelbundet endotelcellenät, bevarade fler celler totalt och visade färre markörer för senescens, fibros och överskott av matrix. Med andra ord, att rensa ut de mest skadade cellerna minskade bördan av skadliga utsöndringar och bidrog till att bibehålla en friskare hornhinneyta.
Vad detta betyder för personer med FECD
För patienter leder FECD idag ofta till hornhinnetransplantation när synen blir för grumlig. Denna studie antyder en annan väg: sjukdomen kan drivas av en långsam ansamling av stressade, icke-delande celler som både misslyckas med att utföra sitt arbete och aktivt förgiftar sina grannar med inflammatoriska och fibrotiska signaler. Att rikta in sig på dessa signaler med läkemedel mot IL-17- eller IL-8-vägar, eller att använda senolytiska terapier för selektivt avlägsnande av de mest drabbade cellerna, skulle en dag kunna fördröja ärrbildning, bevara mer av ögats naturliga vävnad och skjuta upp eller minska behovet av kirurgi.
Citering: Parekh, M., Adhikari, Y., Deshpande, N. et al. p16-mediated G0/G1 cell cycle arrest leads to SASP and fibrosis in Fuchs endothelial corneal dystrophy. Cell Death Dis 17, 197 (2026). https://doi.org/10.1038/s41419-026-08425-6
Nyckelord: Fuchs-dystrofi, korneal endotel, cellulär senescens, fibros, senolytisk terapi