Clear Sky Science · sv
Mitochondriellt DNA driver aktivering av NLRP3–IL-1β-axeln i mikroglia genom bindning till NLRP3, vilket leder till neurodegeneration i Parkinsons sjukdomsmodeller
Varför detta är viktigt för Parkinsons sjukdom
Parkinsons sjukdom är mest känd för skakningar och fördröjd rörelse, men under dessa symtom pågår en komplex kamp inne i hjärnan. Denna studie avslöjar hur små fragment av genetiskt material från skadade mitokondrier i hjärnans immunceller kan antända inflammation som gradvis dödar de dopaminproducerande neuroner som behövs för smidig rörelse. Att förstå denna kedjereaktion öppnar möjligheter för nya, mycket specifika läkemedelsmål som kan bromsa eller förebygga Parkinsonliknande skador.
Hjärnans immunceller och kraftverk under stress
Hjärnan innehåller inte bara neuroner utan också mikroglia, dess lokala immunceller. Vid Parkinsons sjukdom blir dessa mikroglia ofta överaktiva och frisätter giftiga molekyler och inflammatoriska signaler som skadar närliggande neuroner. Författarna fokuserade på mitokondrierna, cellernas ”kraftverk”, som har eget DNA. När mitokondrier skadas—av toxiner, åldrande eller andra påfrestningar—kan deras DNA bli oxiderat, en sorts kemisk skada orsakad av reaktiva syreradikaler. Eftersom mitokondriellt DNA liknar bakteriellt DNA kan dessa skadade fragment fungera som larm i hjärnan, aktivera immunsystemet och potentiellt driva kronisk inflammation.
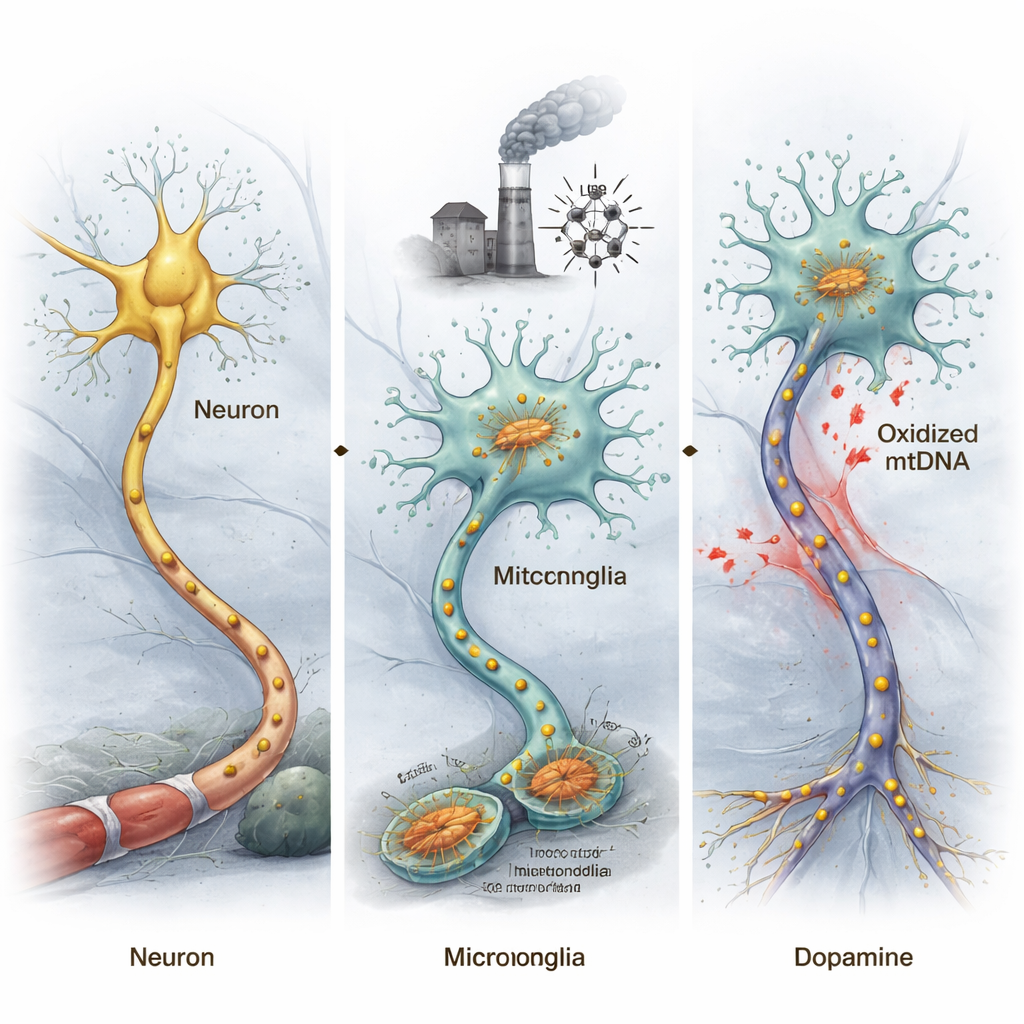
Skadat mitokondriellt DNA kan driva möss mot Parkinsonliknande sjukdom
För att testa om oxiderat mitokondriellt DNA (ox-mtDNA) faktiskt kan utlösa Parkinsonliknande förändringar, extraherade forskarna ox-mtDNA från stressade mikrogliala celler och injicerade det direkt i en hjärnregion som normalt innehåller dopaminproducerande neuroner viktiga för rörelse. Möss som exponerades för detta ox-mtDNA visade minskad rörlighet i beteendetester och en förlust av dessa dopaminneuroner, vilket speglade centrala drag hos Parkinsons sjukdom. Genom att separera neuroner och mikroglia från mitthjärnan och analysera deras genaktivitet fann teamet att gener kopplade till Parkinsons sjukdom blev mer avvikande i neuroner, medan inflammationsrelaterade gener var kraftigt aktiverade i mikroglia.
En molekylär alarmswitch inne i mikroglia
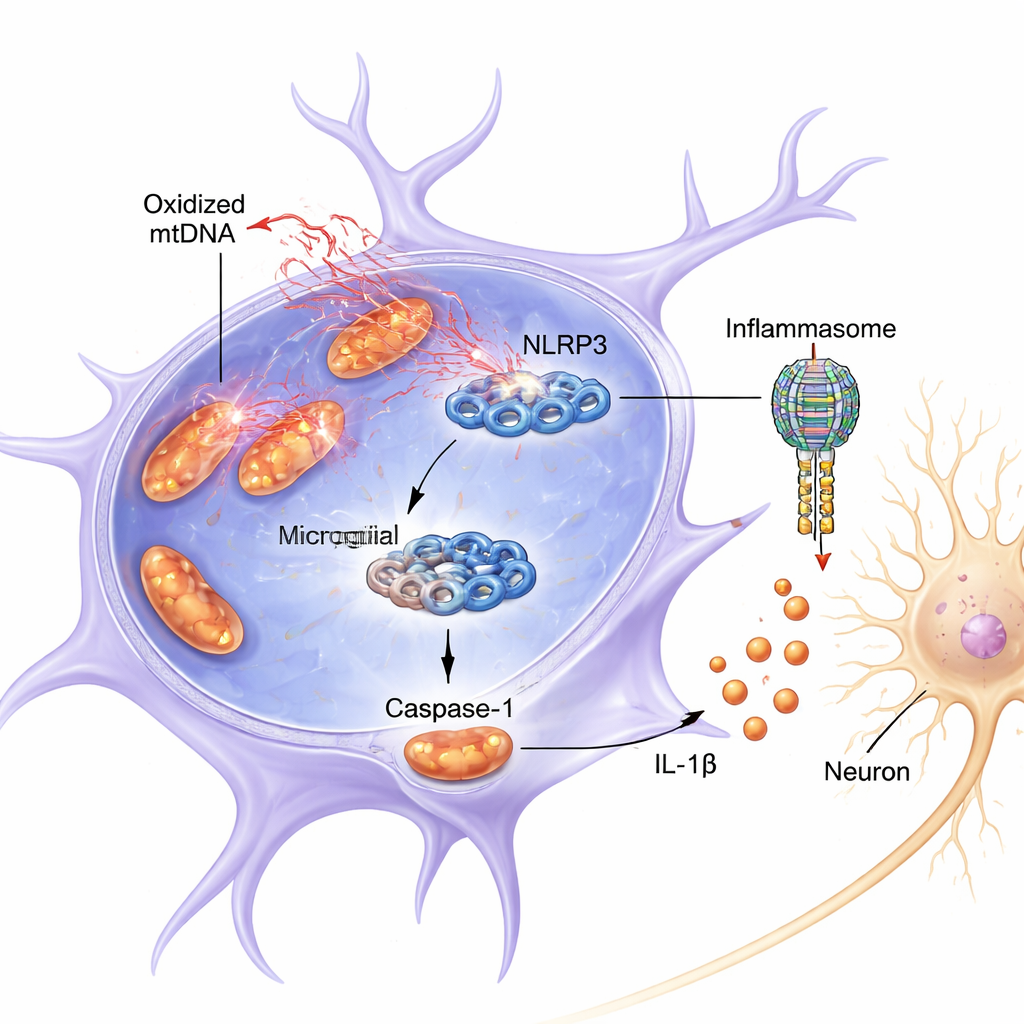
Studien fördjupade sig i ett proteinkomplex i mikroglia kallat NLRP3, en del av en större struktur som kallas inflammasom. När det aktiveras hjälper NLRP3 till att aktivera kaspas-1, ett enzym som klyver den inflammatoriska molekylen IL-1β till dess aktiva, skadliga form. Både i möss och i odlade celler orsakade kombinationen av ett inflammatoriskt primingsignal (LPS, en bakteriell komponent) och ett pesticidliknande toxin rotenon att mitokondrier i mikroglia släppte ut oxiderat mtDNA i cellvätskan. Denna frisättning sammanföll med starkare aktivering av NLRP3, mer klyvt (aktivt) kaspas-1 och högre nivåer av IL-1β. Medium taget från dessa överaktiverade mikroglia var direkt giftigt för dopaminlika neuroner odlade i petriskålar och minskade deras överlevnad samt nivån av deras nyckelmarkör tyrosinhydroxylas.
Direkt bindning: hur oxiderat DNA slår på NLRP3
Förutom enkel korrelation visade författarna att ox-mtDNA inte bara finns när inflammation pågår—det tycks binda fysiskt till NLRP3 och slå på det. När de blockerade frisättningen av mitokondriellt DNA med ett läkemedel sjönk aktiveringen av kaspas-1 och IL-1β. Omvänt gav direkt leverans av oxiderat mtDNA till mikroglia en stark förstärkning av NLRP3-signaleringen, mer än icke-oxiderat mtDNA. Med biokemiska pull-down-experiment detekterade de mtDNA, rikt på oxidativa skademarkörer, bundet till NLRP3. Datorbaserade modeller och protein-kemi visade att ox-mtDNA binder till ett positivt laddat, flexibelt segment av NLRP3 (en ”intrinsically disordered region”) som sträcker sig över aminosyrorna 180–187. När denna kritiska sekvens togs bort från NLRP3 minskade dess förmåga att binda ox-mtDNA och aktivera kaspas-1 kraftigt.
Att stänga av inflammasomet skonar neuroner
Forskarna frågade sedan om störning av NLRP3 kunde skydda neuroner. I odlade mikroglia sänkte genetisk reducering av NLRP3 kraftigt aktiveringen av kaspas-1 och IL-1β efter LPS- och rotenonbehandling, och det konditionerade mediet från dessa celler var betydligt mindre giftigt för dopaminlika neuroner. I möss minskade en selektiv NLRP3-hämmare (MCC950) mikroglial aktivering, bevarade dopaminneuroner och sänkte nivåerna av inflammasomrelaterade proteiner i modeller drivna antingen av LPS plus rotenon eller av injicerat mtDNA. Tillsammans visar dessa experiment att ox-mtDNA–NLRP3–IL-1β-kedjan inte bara är associerad med skada; den är nödvändig för mycket av den observerade neuronförlusten.
Vad detta betyder för framtida Parkinsonbehandlingar
För icke-specialister är huvudbudskapet att skadat mitokondriellt DNA som läcker från hjärnans immunceller kan fästa direkt vid en intern ”alarmswitch” (NLRP3), vilket orsakar en våg av inflammation som skadar dopaminneuroner och driver Parkinsonliknande sjukdom i modeller. Eftersom denna interaktion beror på en kort, definierad del av NLRP3-proteinet och på den oxiderade naturen hos mitokondriellt DNA, erbjuder den precisa nya läkemedelsmål. Terapier som förebygger mitokondriellt DNA-skada eller läckage, blockerar dess bindning till NLRP3 eller hämmar NLRP3 självt skulle i princip kunna dämpa denna inflammatoriska kaskad och bromsa utvecklingen av Parkinsons sjukdom.
Citering: Gan, Q., Fu, X., Zhou, T. et al. Mitochondrial DNA drives NLRP3-IL-1β axis activation in microglia by binding to NLRP3, leading to neurodegeneration in Parkinson’s disease models. Cell Death Dis 17, 213 (2026). https://doi.org/10.1038/s41419-026-08424-7
Nyckelord: Parkinsons sjukdom, mikroglia, mitokondriellt DNA, NLRP3-inflammasom, neuroinflammation