Clear Sky Science · sv
Laktylering av SLC26A3 i det sura tumörmikromiljön främjar malign progression av kolorektalt karcinom
Varför tumörens surhet spelar roll
Kolorektal cancer är fortfarande en av de dödligaste cancerformerna globalt, delvis därför att tumörer ofta återkommer, sprider sig eller slutar svara på läkemedel. Denna studie undersöker en underuppskattad orsak till detta beteende: den sura, mjölksyrarika miljön inne i tumörer. Genom att visa hur denna hårda miljö destablerar ett skyddande membranprotein kallat SLC26A3, avslöjar författarna en ny händelsekedja som gör att cancerceller blir mer stamcellsliknande, invasiva och läkemedelsresistenta — vilket ger nya idéer för behandling.
Ett hårt grannskap kring cancerceller
Snabbt växande tumörer förbrukar stora mängder socker och syre och frigör mjölksyra och vätejoner som gör deras omgivning sur. Genom att använda stora patientdatamängder och vävnadsprover visar forskarna att detta sura tillstånd, spårat med en markörprotein kallad CA9, går hand i hand med aggressiva kolorektala tumörer. I mer avancerade cancerformer är CA9-nivåerna höga, medan SLC26A3-nivåerna konsekvent är låga. SLC26A3 sitter normalt på ytan av colonceller och hjälper till att balansera salt och bikarbonat, vilket i sin tur hjälper till att reglera pH. I tumörprover, cancercellinjer och encellanalyser finner teamet att när surheten ökar sjunker SLC26A3-nivåerna — särskilt i maligna, stamcellsliknande cancerceller. 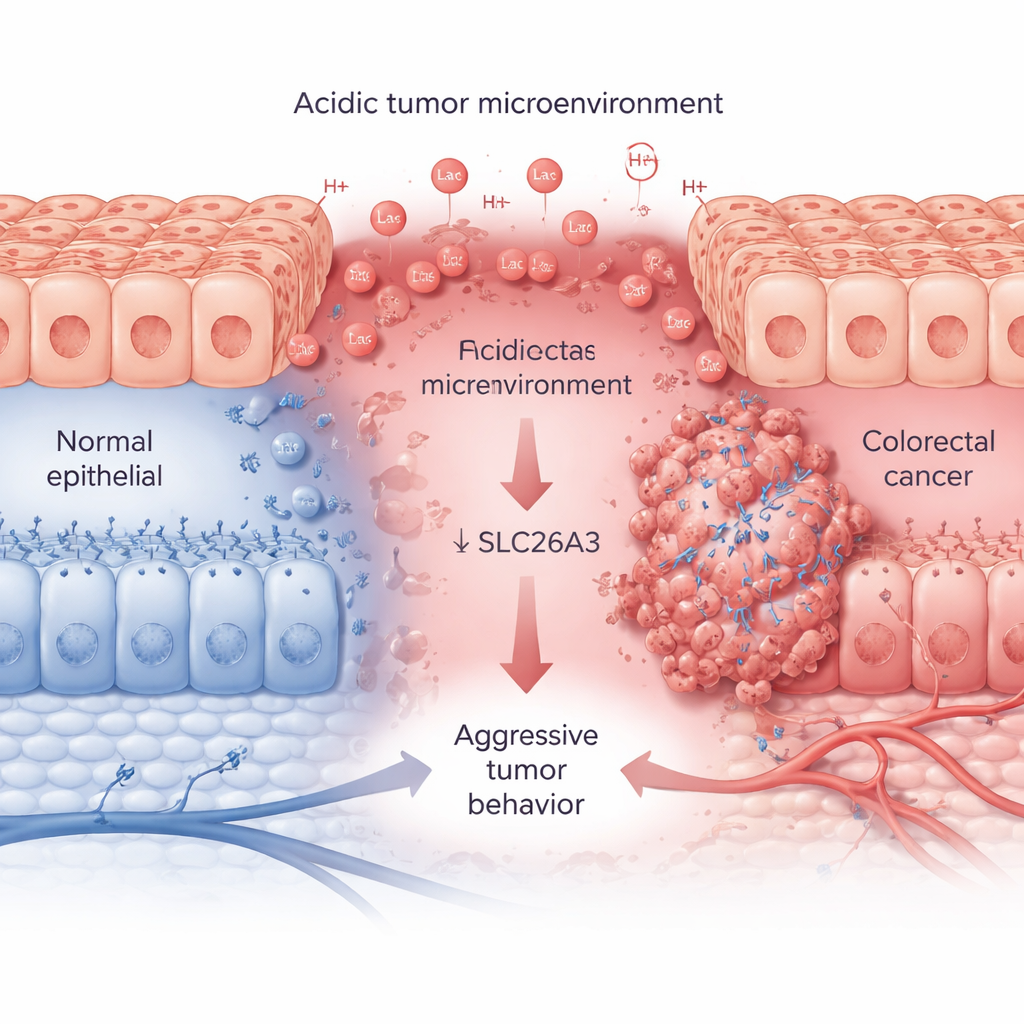
Hur mjölksyra märker ett mål för destruktion
Författarna frågar sig varför SLC26A3 minskar i sura tumörer. De fokuserar på laktylering, en nyligen upptäckt kemisk märkning som bildas från mjölksyra och kan fästas på proteiner. När kolorektala cancerceller exponeras för mjölksyra eller odlas i sura förhållanden blir SLC26A3 kraftigt laktylerat. Detaljerad proteinanalys identifierar en nyckelplats, en aminosyra kallad K536, där denna märkning läggs till. Laktylering vid K536 gör SLC26A3 mindre stabilt: proteinet löper större risk att märkas med ubiquitin, en cellulär ”släng bort detta”-signal, och skickas till cellens återvinningsmaskineri. Att blockera enzymet p300, som hjälper till att lägga till laktyleringsmärken, skyddar delvis SLC26A3 från nedbrytning. Som en följd etablerar surhet och laktat en skadlig återkopplingsloop — mer laktat leder till mer laktylering, vilket minskar SLC26A3, ytterligare rubbar pH-balansen och gynnar en ännu surare mikromiljö.
Att stänga av en broms på cancerstam-egenskaper och spridning
När SLC26A3 är utarmat beter sig cancerceller mer aggressivt. I cellodling uttrycker kolorektala cancerstamliknande celler naturligt mindre SLC26A3 än sina icke‑stamliknande motsvarigheter. När forskarna medvetet sänker SLC26A3-nivåerna bildar tumörceller fler sfärer (ett kännetecken för stamcellsegenskap), förnyar sig själva mer effektivt, invaderar genom artificiella membran och migrerar snabbare över skrapsår. De blir också mindre känsliga för vanliga cytostatika som oxaliplatin och 5‑fluorouracil. Omvänt minskar ökade nivåer av SLC26A3 markörer för stamcellsegenskaper och bromsar invasion och migration — men denna fördel dämpas när extra laktat tillsätts, vilket understryker hur surhet kan övervinna den skyddande effekten.
En dold koppling till genreglering
Förutom att hjälpa till att reglera surhet fungerar SLC26A3 också som en ställning som binder två RNA‑bindande proteiner, HuR och CUGBP1. Dessa proteiner kontrollerar livslängden hos många budbärar‑RNA som kodar för cancerrelevanta proteiner. När SLC26A3 är rikligt förekommande fångar det upp en del HuR och CUGBP1, vilket begränsar hur starkt de kan stabilisera eller destabilisera vissa cancerrelaterade budskap. När SLC26A3 förloras genom laktylering och nedbrytning är HuR och CUGBP1 friare att binda onkogena mRNA som främjar stamcellsegenskaper, epitelial‑mesenkymal transition (EMT), invasion och överlevnad. Experiment visar att HuR hjälper till att stabilisera mRNA för stamcellsmärken och cellförbindelseproteiner, medan CUGBP1 kan motsätta sig HuR för vissa mål, vilket minskar junction‑integritet och uppmuntrar EMT — båda gynnar tumörspridning.
Ombalansera miljön för att bekämpa cancer
För att testa om dessa insikter kan omvandlas till behandlingsstrategier använder forskarna musemodeller för kolorektal cancer. Neutralisering av tumörens surhet med natriumbikarbonat, blockering av laktattransport med en MCT1‑hämmare eller överuttryck av SLC26A3 saktar alla tumörtillväxt. Att kombinera återställning av SLC26A3 med kemoterapi krymper tumörer ytterligare. I patientdata korrelerar högre SLC26A3‑nivåer med bättre överlevnad, mindre återfall, färre metastaser och bättre svar på kemoterapi, vilket tyder på att detta protein både kan fungera som en biomarkör och ett terapeutiskt mål. 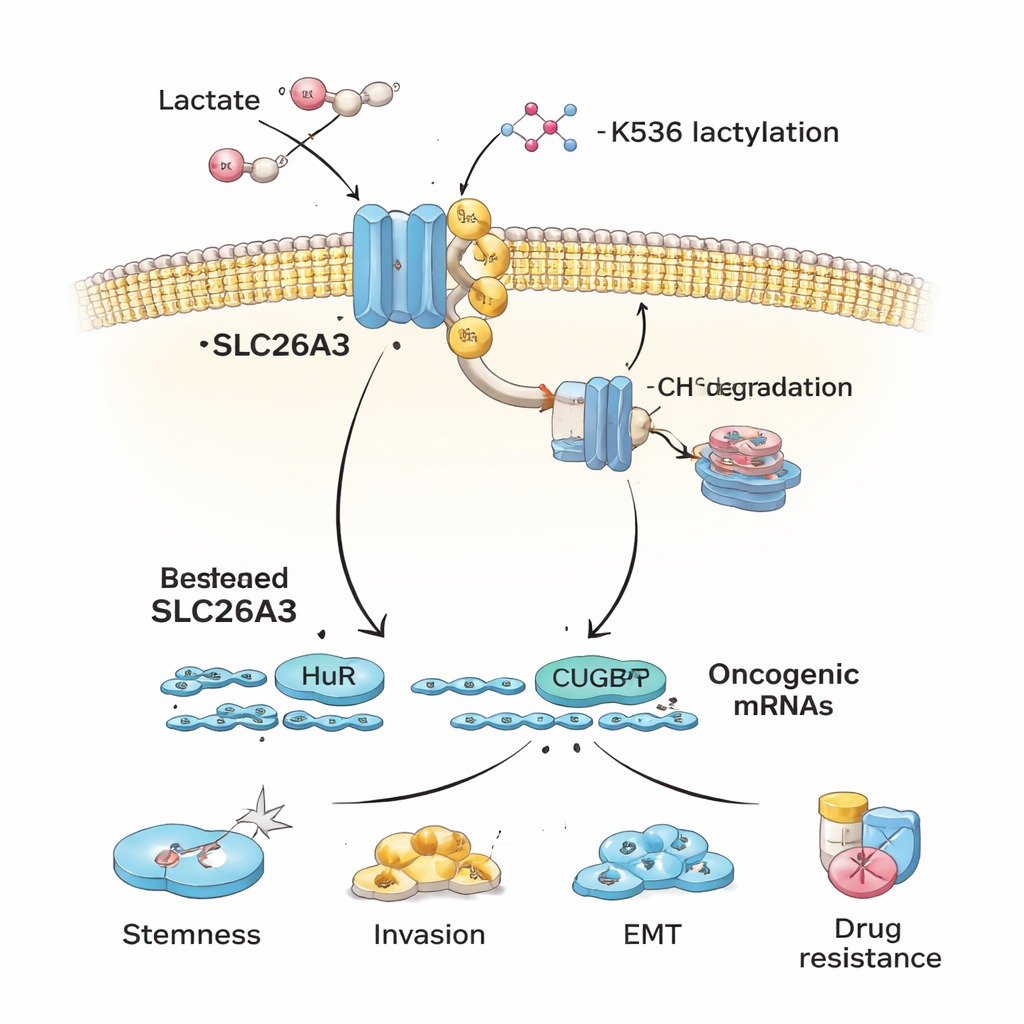
Vad detta betyder för patienter
I vardagliga termer visar denna studie att kolorektala tumörer trivs i ett surt, mjölksyra‑rikt bad som kemiskt ”märker” och förstör en skyddande grindvakt, SLC26A3. När denna grindvakt är borta antar cancerceller lättare stamcellsliknande egenskaper, sprider sig och blir behandlingsresistenta, understödda av kraftfulla RNA‑regulatorer inuti cellen. Genom att buffra tumörens surhet, blockera laktathantering eller återställa SLC26A3 kan man möjligen försvaga den maligna återkopplingsloopen och få standardbehandlingar att fungera bättre. Även om sådana tillvägagångssätt fortfarande kräver rigorösa kliniska prövningar öppnar de en lovande ny vinkel på hur hantering av tumörens kemiska omgivning skulle kunna hjälpa till att kontrollera kolorektal cancer.
Citering: Chen, C., Cai, D., Liu, X. et al. Lactylation of SLC26A3 in the acidic tumor microenvironment promotes malignant progression of colorectal carcinoma. Cell Death Dis 17, 164 (2026). https://doi.org/10.1038/s41419-026-08422-9
Nyckelord: kolorektal cancer, tumörmikromiljö, laktylering, cancerstamceller, kemoterapiresistens