Clear Sky Science · sv
Att rikta in sig på GNG4 hämmar tumörprogression och återställer känslighet för enzalutamid vid prostatacancer genom att undertrycka autofagi
Varför denna forskning är viktig
För många män med avancerad prostatacancer fungerar kraftfulla hormonblockerande läkemedel som enzalutamid bra till en början, men deras effekt avtar så småningom. Denna studie avslöjar ett dolt överlevnadstrick som tumörceller använder och pekar ut ett specifikt protein, GNG4, som hjälper cancer att fortsätta växa och stå emot behandling. Att förstå denna mekanism kan leda till kombinationsbehandlingar som får nuvarande läkemedel att fungera bättre och längre.
En proteinknapp som gömmer sig avtäckt
Prostatacancerceller styrs i hög grad av manliga hormoner, så standardbehandlingen för avancerad sjukdom avskärmar dessa signaler. Ändå blir de flesta tumörer så småningom ”kastrationsresistenta” och börjar växa igen. Författarna sökte efter gener som var mycket mer aktiva i tumörvävnad än i närliggande normal prostatavävnad från samma patienter. Bland flera kandidater utmärkte sig GNG4: när de minskade dess nivåer i prostatacancerceller sjönk tumörcellernas tillväxt markant. Analys av hundratals patientprover bekräftade att GNG4 är högre i primära prostatatumörer än i normal vävnad och är särskilt förhöjt i mer aggressiva, högre gradtumörer.
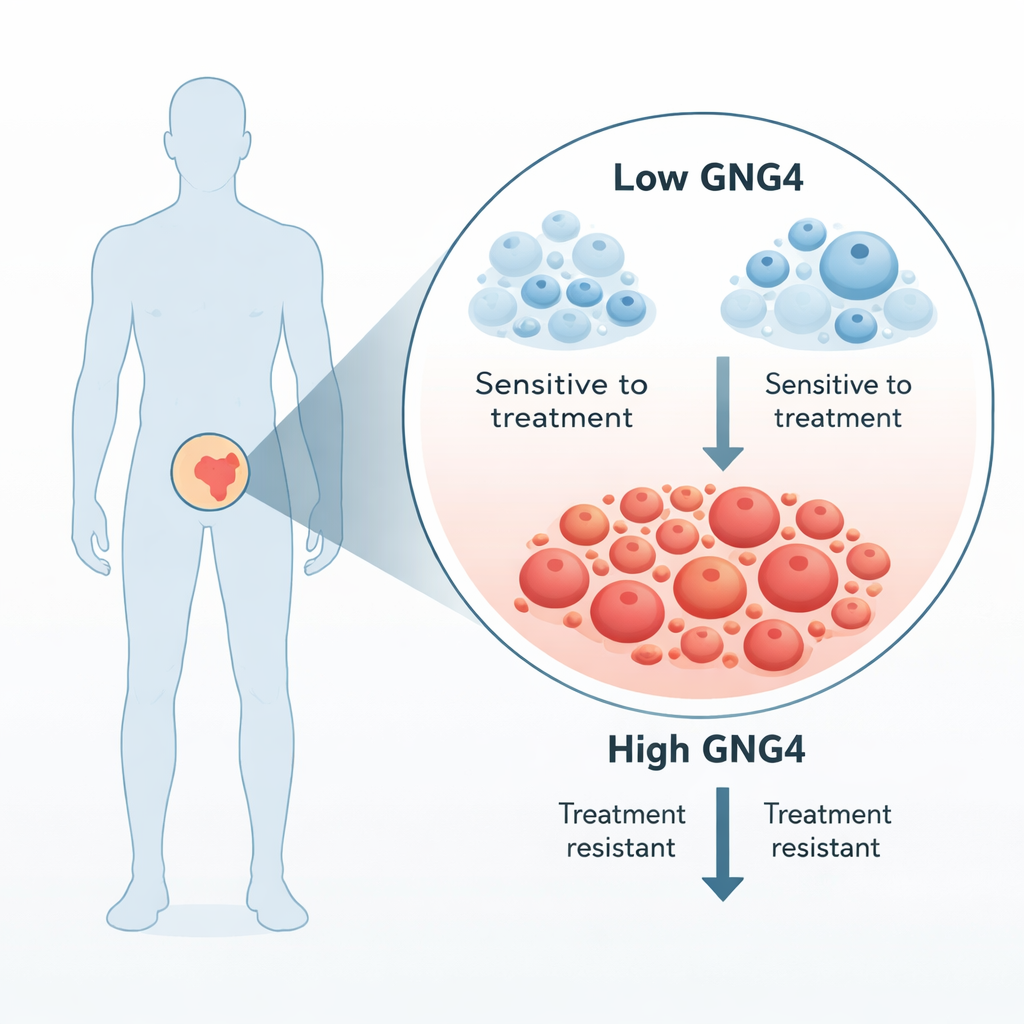
Hur GNG4 hjälper tumörer att frodas
GNG4 är en del av en större signalfamilj som kallas G‑proteiner, vilka sitter i cellmembranet och förmedlar signaler från utsidan till cellens inre. Teamet visade att nedreglering av GNG4 i prostatacancercellinjer saktade ner celldelningen, fick cellerna att stanna upp i en kontrollpunkt i cellcykeln och ökade programmerad celldöd. Dessa förändringar minskade också cancercellernas förmåga att migrera och sluta sår i laboratorietester, och tumörer som bildades av GNG4‑defekta celler växte långsammare i möss. Tillsammans tyder fynden på att GNG4 fungerar som en gaspedal för prostatacancertillväxt och spridning.
Autofagi: cancercellens nödskafferi
Forskarna fokuserade sedan på en process som kallas autofagi, där celler bryter ner och återvinner sina egna komponenter för att överleva stress, som svält eller läkemedelsbehandling. I många avancerade cancerformer fungerar autofagi som ett nödskafferi som hjälper tumörceller att klara svåra förhållanden. I denna studie visade prostatacancerceller med hög GNG4‑aktivitet fler tecken på aktiv autofagi, medan celler med nedslagen GNG4 hade färre återvinningsstrukturer och lägre nivåer av centrala autofagimarkörer. När GNG4 överproducerades tolererade cellerna enzalutamid bättre och genomgick mindre celldöd. Att blockera autofagi med en kemisk hämmare utplånade mycket av detta skydd, vilket indikerar att GNG4 hjälper tumörer att uthärda behandling i hög grad genom att uppreglera detta återvinningssystem.
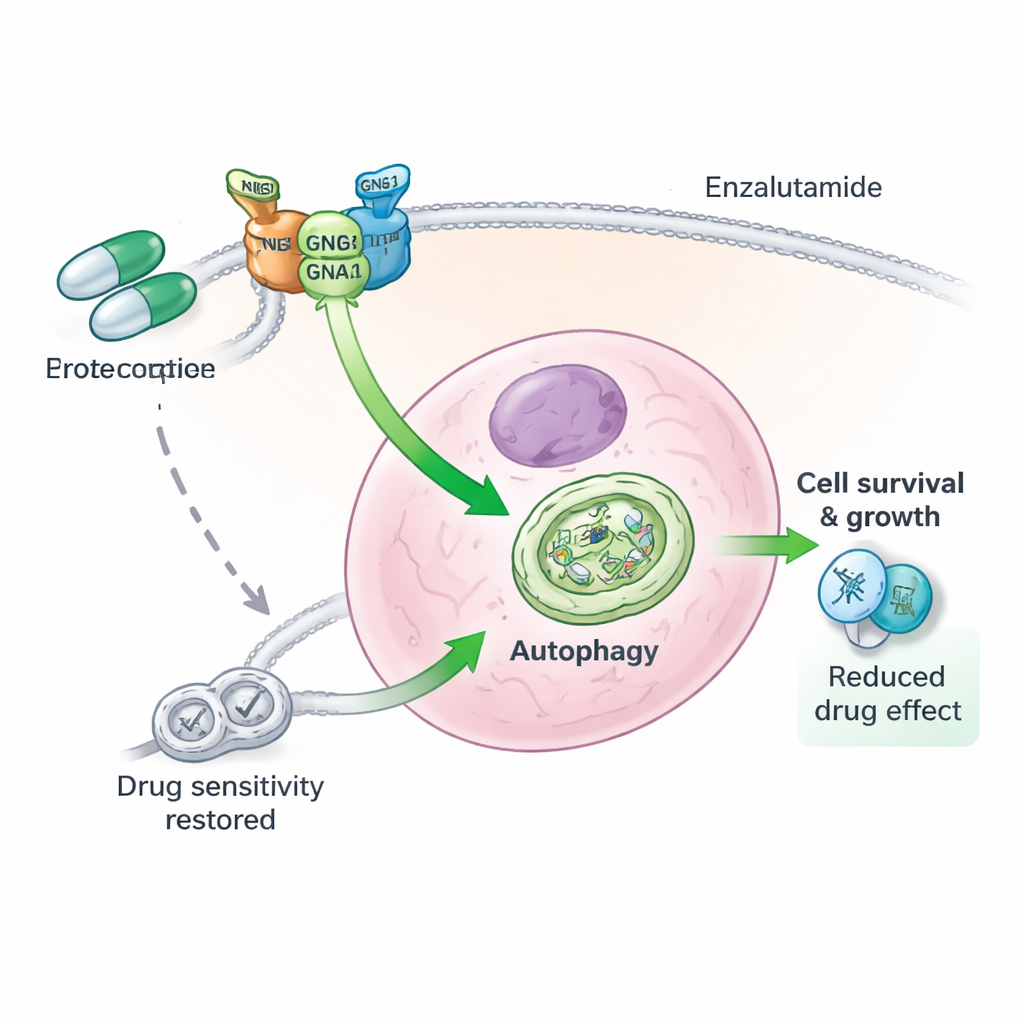
En tredelad proteintrojka bakom läkemedelsresistens
Vid en närmare granskning upptäckte författarna att GNG4 inte verkar ensam. Det binds fysiskt till en annan G‑proteinkomponent, GNB1, för att stabilisera ett tredje protein, GNAI3. Tillsammans bildar dessa tre subenheter ett funktionellt komplex som ökar autofagi i prostatacancerceller. När GNG4 minskades blev GNAI3‑proteinet snabbare märkt för nedbrytning och bröts ner av cellens sopmaskineri, vilket slog av autofagisignalen. Att ta bort GNAI3 i sig upphävde de tillväxt‑ och överlevnadsfördelar som extra GNG4 gav, både i odlingar och i musstumörer. Med andra ord driver GNG4 malignitet och stresstolerans i hög grad genom denna GNG4–GNB1–GNAI3‑axel.
Få nuvarande läkemedel att arbeta hårdare
Slutligen undersökte teamet vad som händer när GNG4‑inriktning kombineras med enzalutamid, ett ledande läkemedel för avancerad prostatacancer. I laboratoriet gjorde GNG4‑nedreglering cancerceller markant mer känsliga för enzalutamid och minskade deras förmåga att bilda kolonier efter behandling. I möss krympte tumörer med sänkt GNG4 mer vid behandling med enzalutamid än tumörer med normala GNG4‑nivåer, utan synbar ökad toxicitet. Direkt blockering av autofagi gav liknande förbättringar. Dessa resultat tyder på att störning av GNG4‑driven autofagi kan beröva tumörceller ett viktigt coping‑verktyg, vilket gör att befintliga hormonblockerande terapier kan ge ett starkare och mer långvarigt slag.
Vad detta betyder för patienter
För en icke‑specialist är huvudbudskapet att vissa prostatatumörer överlever behandling genom att slå på ett internt återvinningssystem som fungerar som ett reservkraftverk. Denna studie identifierar GNG4 som huvudströmbrytaren som slår på det systemet, tillsammans med partnerproteiner som skyddar cancerceller från enzalutamid. Genom att slå av denna brytare—antingen genom att direkt rikta in sig på GNG4 eller genom att säkert dämpa autofagi—kan framtida behandlingar eventuellt bromsa tumörtillväxt och återställa läkemedelskänslighet hos män vars cancer blivit svår att behandla.
Citering: Chen, L., Zhang, J., Hu, Y. et al. Targeting GNG4 inhibits tumor progression and restores enzalutamide sensitivity in prostate cancer by suppressing autophagy. Cell Death Dis 17, 160 (2026). https://doi.org/10.1038/s41419-026-08421-w
Nyckelord: prostatacancer, läkemedelsresistens, autofagi, G-proteiner, enzalutamid