Clear Sky Science · sv
Preklinisk profilering av antikropps–läkemedelskonjugat som riktar sig mot onkofetal kondroitinsulfat
Varför denna forskning är viktig för framtida cancerbehandling
Cancerläkemedel fungerar ofta som kartbombning: de träffar snabbt delande celler i hela kroppen, inte bara i tumörer, vilket ger svåra biverkningar och ibland misslyckas med att nå alla cancerceller. Denna studie utforskar ett smartare tillvägagångssätt som kombinerar antikroppars precision med cytostatikaers kraft och som riktar sig mot en struktur som förekommer i många tumörer men knappt i friska vävnader. För en lekmannaläsare ger den en bild av hur framtidens cancerterapier kan bli både mer effektiva och mindre skadliga.
En särskild cancer‑endast ”flagga” på tumörvävnad
Forskarna fokuserar på ett molekylärt mål som kallas onkofetal kondroitinsulfat, eller ofCS. Detta är ett sockerliknande ytlager som syns under fosterutveckling, försvinner i de flesta friska vuxna vävnader och sedan återkommer i många cancerformer. Det finns inte bara på cancercellerna själva utan även i den omgivande tumörstommen och stödjecellerna. Det gör ofCS till ett ovanligt attraktivt mål: att slå mot ofCS kan innebära att man angriper både tumören och dess ”jordmån” samtidigt som normala organ till största delen skonas. Gruppen upptäckte tidigare ett antikroppsfragment, kallat Vartumab, som känner igen ofCS i en bred variation av solida tumörer med mycket liten bindning till normal vävnad.
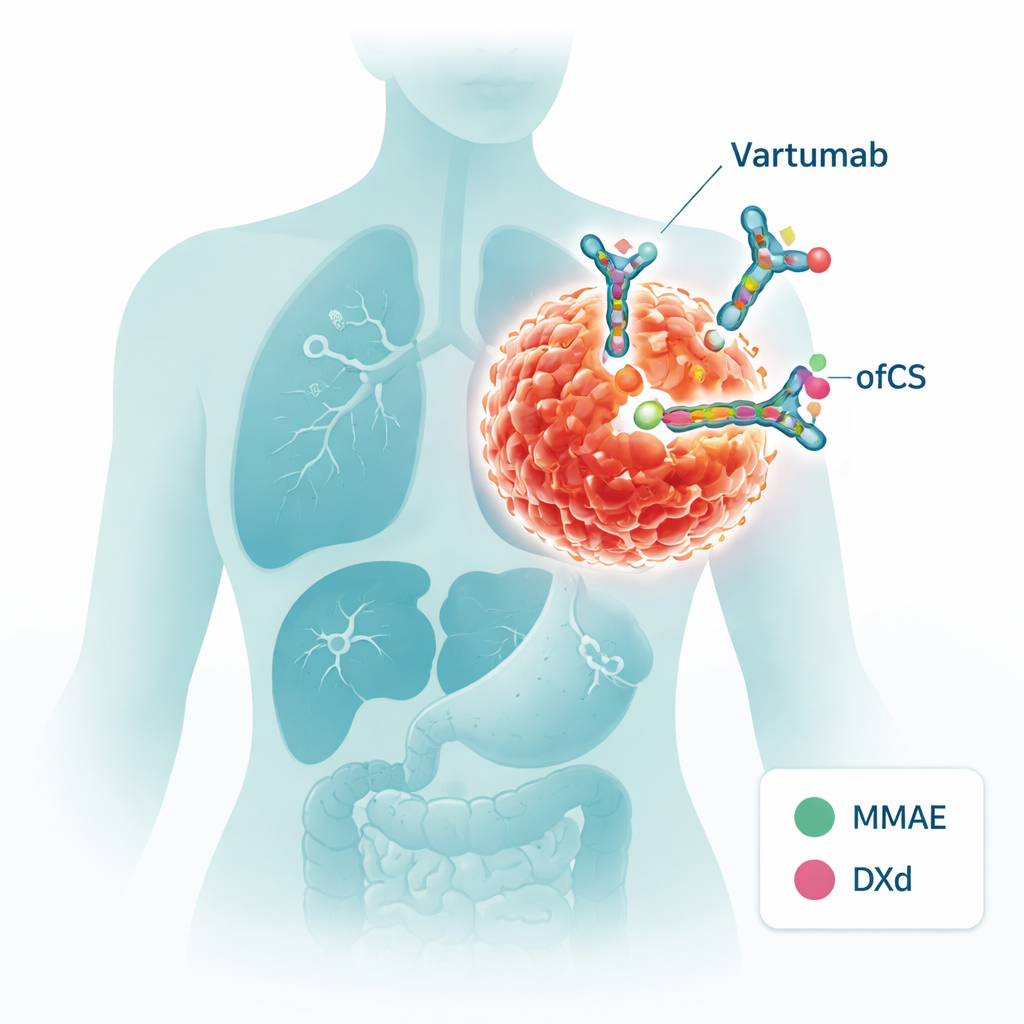
Att konstruera en styrd missil mot tumörer
I detta arbete omvandlas Vartumab till ett antikropps–läkemedelskonjugat (ADC) — i praktiken en styrd missil som bär ett giftigt stridsladdning. Forskarna kopplade två olika cytostatikapayloads, MMAE och DXd, vardera via en kemisk ”länk” som kan klippas av enzymer som ofta finns i tumörmiljön. När Vartumab binder till ofCS kan dessa länkar klyvas och frigöra läkemedlet exakt där det behövs. Gruppen verifierade noggrant att de modifierade antikropparna förblev stabila i blodliknande förhållanden, frigjorde payloaden vid exponering för tumörrelaterade enzymer och, avgörande, fortfarande kände igen ofCS lika bra som ursprungliga Vartumab.
Att slå mot cancerceller och deras grannar
En central egenskap hos de valda payloads är så kallad bystandereffekt. När MMAE och DXd väl frigörs kan de diffundera ut ur den första cellen de dödar och tränga in i närliggande celler, även om dessa grannar inte visar målet ofCS. Forskarna testade detta genom att blanda ofCS-positiva melanomceller med genetiskt konstruerade ofCS-negativa celler. ADC:er med MMAE eller DXd dödade inte bara de riktade cellerna utan även de målnegativa grannarna i en grad som berodde på hur många ofCS-positiva celler som fanns. Som jämförelse dödade en kontroll‑ADC med en mindre permeabel payload (MMAF) endast de direkt riktade cellerna och gav ingen stark bystandereffekt.
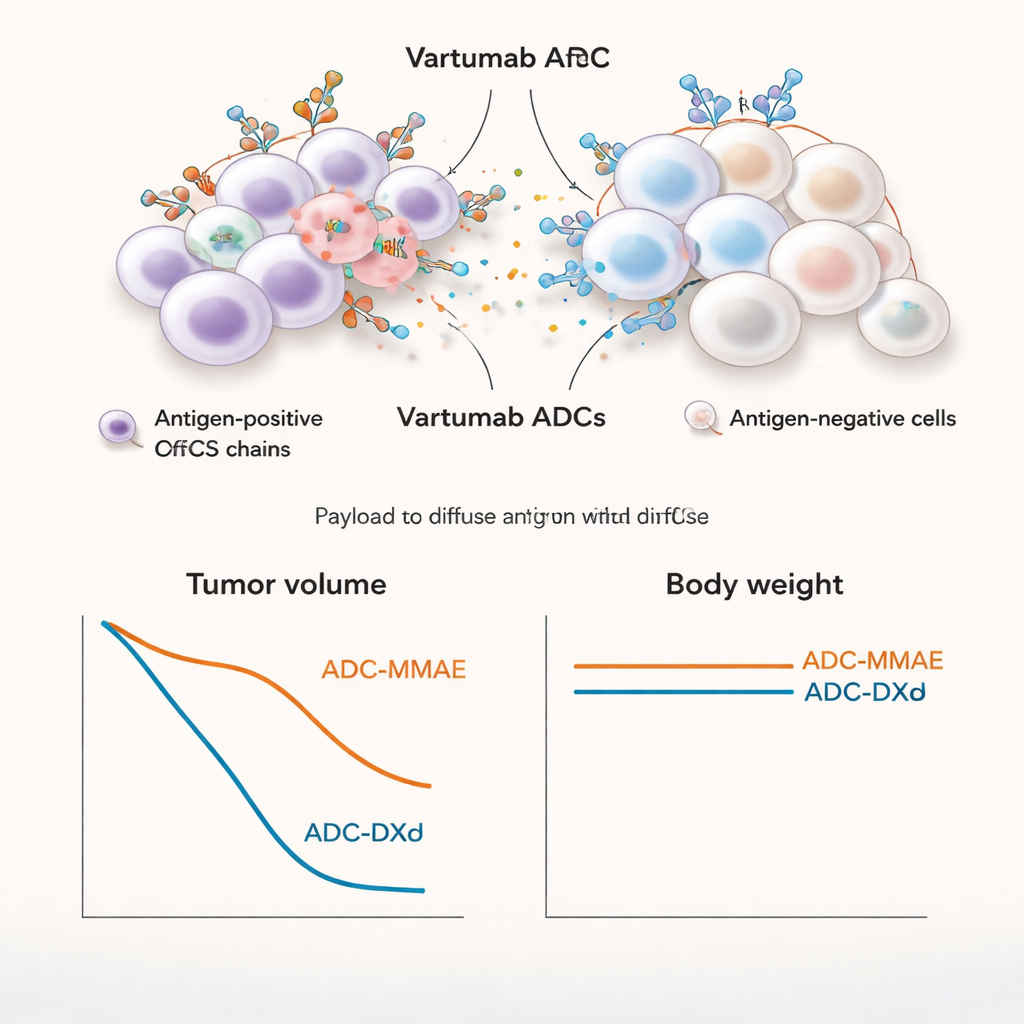
Stark tumörminskning med begränsad utanför‑mål‑skada
I musmodeller för melanom och lungcancer ackumulerades Vartumab‑ADC:erna starkt i tumörer medan nivåerna i andra organ var mycket lägre. MMAE‑varianten var särskilt potent: vid relativt låga doser krympte etablerade tumörer helt, även i en lungcancermodell med lägre ofCS‑nivåer. DXd‑varianten gav också stark tumörregression, men krävde generellt högre doser. När gruppen jämförde MMAE med den icke‑bystander‑kapabla MMAF i möss uppnådde endast den bystander‑kapabla MMAE‑ADC fullständig och varaktig tumörutrotning, vilket understryker vikten av att döda både cancerceller och stödjande stromaceller. I råttor tolererades upprepad dosering av MMAE‑ADC upp till 5 mg/kg väl, med vikt, blodprover och vävnadsundersökningar som visade endast milda, reversibla förändringar liknande kända effekter av relaterade godkända läkemedel.
Vad detta kan betyda för patienter
För icke‑specialister är budskapet att denna studie förfinar en lovande ”sök‑och‑förgör”‑strategi mot cancer. Genom att rikta in sig på ofCS — en markör som är vitt spridd i tumörer men sällsynt i frisk vävnad — och använda payloads som kan spridas till närliggande celler, angriper Vartumab‑ADC:erna inte bara den synliga tumörmassan utan även dess stödjande miljö och dolda cancerceller som annars skulle kunna undkomma. Arbetet är fortfarande prekliniskt, men det pekar på en väg mot framtida läkemedel som är mer tumörfokuserade, fungerar över många cancertyper och kan undvika några av de allvarligaste biverkningarna av konventionell cytostatikabehandling.
Citering: Skafte, A., Vidal-Calvo, E.E., Choudhary, S. et al. Preclinical profiling of antibody drug conjugates targeting oncofetal chondroitin sulfate. Cell Death Dis 17, 162 (2026). https://doi.org/10.1038/s41419-026-08420-x
Nyckelord: antikropps-läkemedelskonjugat, onkofetal kondroitinsulfat, bystandereffekt, riktad cancerterapi, tumörmikromiljö