Clear Sky Science · sv
DNA-PKcs orkestrerar CTLA-4‑depletion‑inducerad senescens i cancerceller
Att vända cancerns tillväxtknapp till en stoppignal
Immunbaserade cancerläkemedel fokuserar ofta på en molekyl som heter CTLA-4, som finns på immunceller, för att hjälpa kroppen att angripa tumörer. Denna studie avslöjar en överraskande vändning: CTLA-4 återfinns även inne i cancercellerna själva och kan fungera som en dold tillväxthjälpare. När forskarna medvetet avlägsnade detta interna CTLA-4 från melanomceller upphörde cancercellerna att föröka sig och gled in i ett långsiktigt "pensionsläge" känt som cellulär senescens. Att förstå denna oväntade roll öppnar nya sätt att bromsa eller till och med krympa tumörer genom att rikta in sig på CTLA-4 inne i cancerceller, inte bara på immunceller.
När celler väljer pension framför okontrollerad tillväxt
Celler delar sig normalt, reparerar och—när de är skadade bortom reparationsförmåga—antingen dör eller går in i senescens, ett permanent stopp i deras tillväxt. Senescenta celler blir typiskt större, ändrar form och producerar specifika markörer som forskare kan upptäcka i labbet. Forskarna fann att när de reducerade CTLA-4 inne i mus- och humana melanomceller blev cellerna större, deras tillväxt sjönk kraftigt och klassiska senescens‑signaler ökade, inklusive enzymer som kan påvisas med speciella färgningstester och proteiner som p16 och p21 som blockerar cellcykeln. Dessa förändringar sågs både när CTLA-4 tillfälligt tystades och när det permanent slogs ut med hjälp av genredigering.
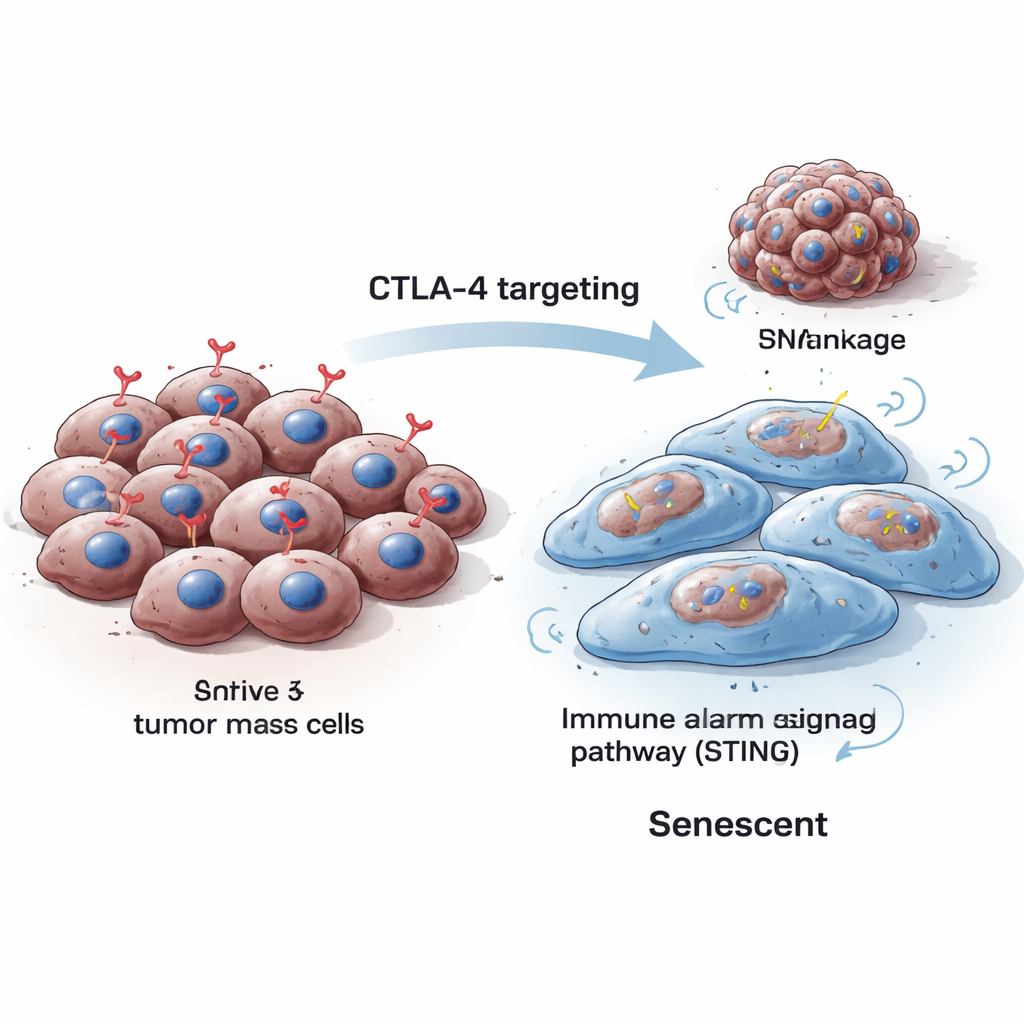
Sprickor i den genetiska ritningen leder till stopp
För att förstå varför CTLA-4‑bortfall pressar cancerceller mot senescens undersökte teamet hur dessa celler hanterar sitt DNA under celldelning. De upptäckte att CTLA-4‑depletion minskade nivåerna av Aurora B, ett protein som hjälper kromosomerna att separera rent när celler delar sig. När Aurora B sjönk utvecklade cellerna genomisk instabilitet: små extra DNA‑innehållande kroppar kallade mikronuclei uppträdde och markörer för DNA‑skada ökade. Denna typ av DNA‑stress är känd för att driva celler mot senescens snarare än okontrollerad tillväxt. Viktigt var att återställande av Aurora B hjälpte till att minska dessa mikronuclei, vilket knöt CTLA-4‑bortfallet direkt till felaktig kromosomhantering och DNA‑skada.
DNA‑skada sätter igång ett internt larmsystem
Det trasiga och felplacerade DNA:t i CTLA-4‑depleterade celler förblev inte oupptäckt. Det aktiverade DNA‑PKcs, en sensor för DNA‑skada, vilket i sin tur utlöste STING‑vägen, ett inbyggt larmsystem som svarar på löst DNA inne i celler. När STING slogs på signalerade det vidare till molekyler inklusive TBK1 och IRF3, och förstärkte även en annan viktig tillväxtkontrollväg, AKT‑vägen. Istället för att främja tillväxt ökade denna kombinerade signalering slutligen p21, en stark broms på cellcykeln, vilket befäste det senescenta tillståndet. När forskarna blockerade DNA‑PKcs minskade STING‑aktivering och senescensdragen kraftigt, vilket visar att DNA‑PKcs sitter i kärnan av denna larmsignalering.
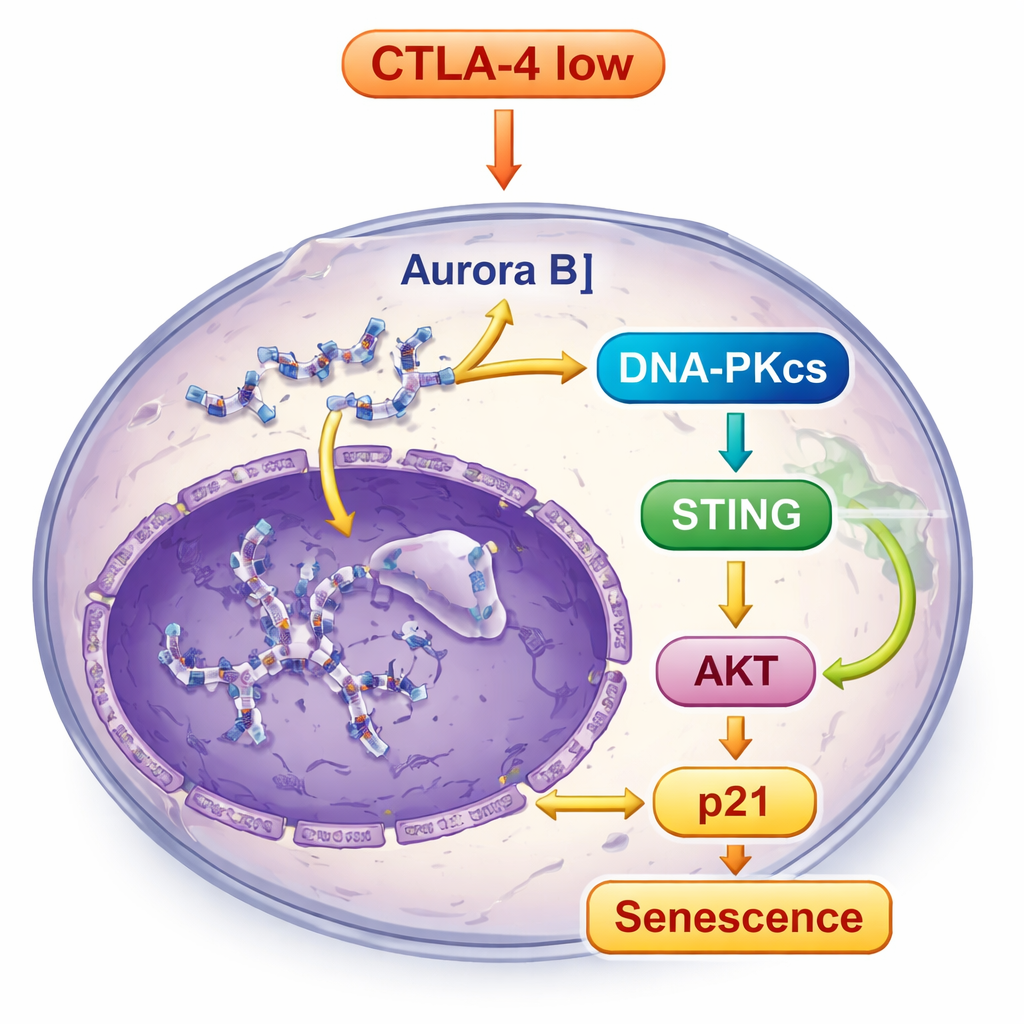
Från cellkultur till tumörer i levande djur
Laboratoriediskar berättar bara en del av historien, så forskarna testade om CTLA-4‑bortfall skulle påverka verkliga tumörer i möss. De implanterade melanomceller med eller utan CTLA-4 på motsatta sidor av samma djur. Tumörer utan CTLA-4 växte långsammare, vägde mindre och var mindre i volym än sina CTLA-4‑innehållande motsvarigheter. Dessa CTLA-4‑defekta tumörer visade också starkare senescensfärgning och högre nivåer av DNA‑skada och STING‑vägsaktivering. Analys av patientdata från stora offentliga databaser stödde ytterligare sambandet: över flera cancertyper var CTLA-4‑uttryck ofta omvänt relaterat till DNA‑PKcs och andra DNA‑reparationskomponenter, vilket speglade laboratoriumfynden i mänsklig sjukdom.
Vad detta betyder för framtida cancerbehandlingar
Sammanfattningsvis visar studien att CTLA-4 inne i cancerceller hjälper dem att bibehålla genetisk stabilitet och fortsätta dela sig. När CTLA-4 tas bort blir kromosomerna instabila, DNA‑brott ackumuleras och ett internt larmsystem—centrerat kring DNA‑PKcs och STING—driver cellerna in i permanent tillväxthämning. För en lekman betyder detta att avstängning av CTLA-4 i tumörceller skjuter cancer bort från farligt, snabbväxande beteende och mot ett säkrare, "pensionerat" tillstånd. Dessa insikter tyder på att framtida cancerterapier skulle kunna utformas inte bara för att frigöra immunsystemet genom att blockera CTLA-4 på immunceller, utan också för att direkt oskadliggöra tumörer genom att rikta CTLA-4 inne i cancerceller och utnyttja senescens som en inbyggd broms mot cancerstillväxt.
Citering: Lee, JJ., Rhee, W.J., Kim, S.Y. et al. DNA-PKcs orchestrates CTLA-4 depletion-induced senescence in cancer cells. Cell Death Dis 17, 204 (2026). https://doi.org/10.1038/s41419-026-08419-4
Nyckelord: cellulär senescens, melanom, CTLA-4, DNA‑skada, STING‑vägen