Clear Sky Science · sv
Cytoplasma‑kärnshuttling av TET2: en inre broms i kolorektalcancerprogression
Hur cancerceller bär sin egen broms
Kolorektalcancer är en av de vanligaste cancerformerna i världen och blir ofta dödlig när tumörceller lär sig att invadera intilliggande vävnad och sprida sig till andra organ. Denna studie visar att många av dessa cancerceller faktiskt bär på ett internt "bromssystem" — ett protein som heter TET2 — som kan sakta deras framfart när det förflyttas in i cellens kärna. Att förstå hur denna inbyggda broms slås på och av skulle kunna öppna nya vägar för att hålla tumörtillväxt i schack, istället för att enbart försöka döda cancercellerna direkt.
Att iaktta ett nyckelprotein röra sig inne i tumörceller
Forskarnas fokus låg på TET2, ett protein som hjälper till att styra vilka gener som är aktiva genom att ta bort vissa kemiska markörer från DNA. I vävnadsprover från hundratals patienter med kolorektalcancer spårade de var TET2 befann sig i tumörcellerna. De fann fyra huvudsakliga mönster: mestadels i kärnan, mestadels i cytoplasman, eller starkt förskjutet åt ena eller andra hållet. Patienter vars tumörer hade mer TET2 i kärnan tenderade att leva längre, medan de som hade TET2 kvar i cytoplasman hade sämre prognos. När cancer framskred till senare kliniska stadier blev nukleärt TET2 mer sällsynt, vilket tyder på att förlusten av detta nukleära skydd är en del i hur tumörer blir mer aggressiva.
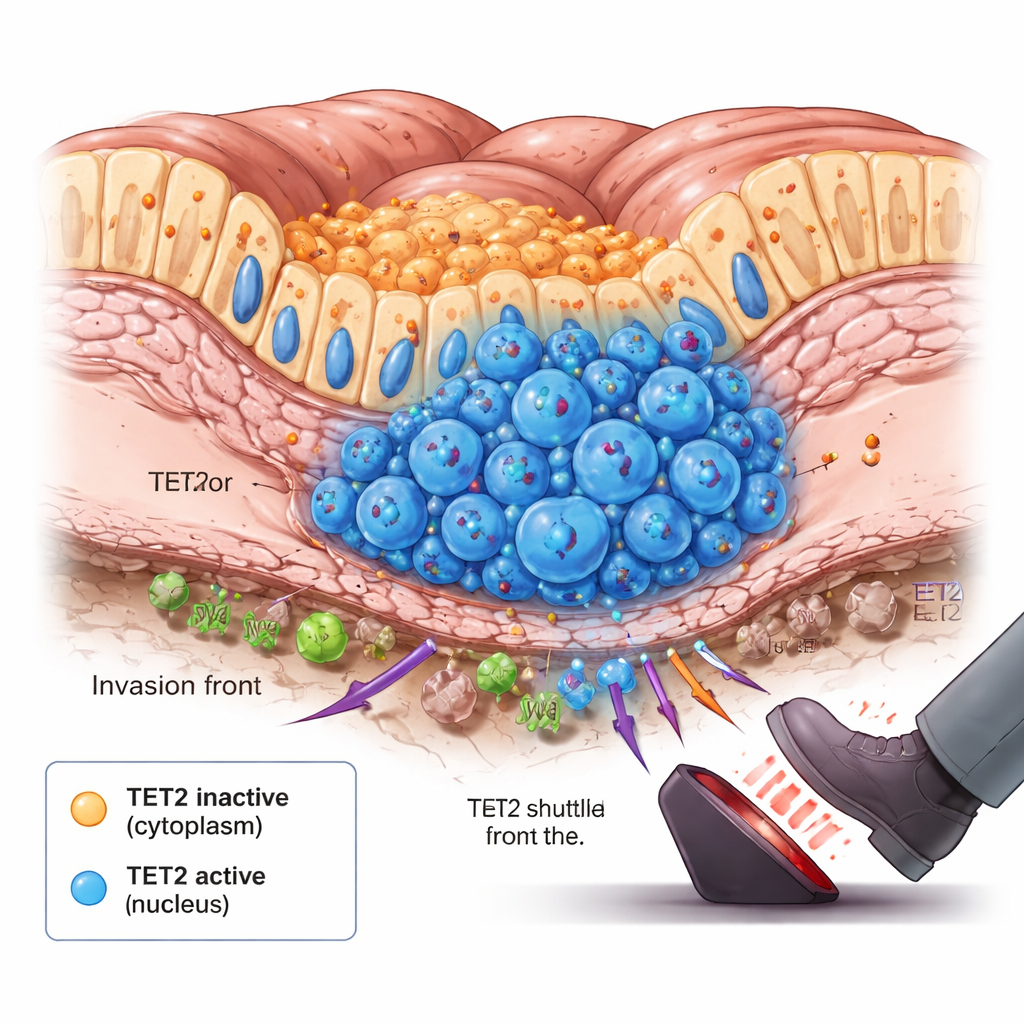
Tumörens frontlinje och ögonblicket för förändring
När teamet grävde djupare noterade de något överraskande: i tumörer som just börjat sprida sig fanns en liten ökning av celler där TET2 flyttat in i kärnan. Dessa celler klustrade sig vid botten av tarmens slemhinna, invasionsfronten där cancerceller först tränger in i djupare vävnad. Djurförsök och långvariga cellkulturmodeller som efterliknar tumörtillväxt visade ett liknande mönster över tid. I början stannade TET2 i cytoplasman och var i stort sett inaktivt. När tumörerna växte och inre regioner blev utsatta för syre‑ och näringsbrist utlöste signaler i cellerna att TET2 skulle shuttla in i kärnan i särskilda subpopulationer. Väl där började TET2 avlägsna DNA‑metyleringsmarkörer och bromsa tumörtillväxten, och fungerade som en nödbroms när cancern korsade en farlig tröskel.
När "kör"‑signaler också utlöser en broms
Kolorektala tumörer förlitar sig ofta på två kraftfulla "kör"‑program: en formskiftande process kallad epitelial–mesenkymal övergång (EMT), som hjälper celler att bli mer rörliga och invasiva, och WNT‑signalvägen, som främjar tillväxt och överlevnad. Dessa vägar ses vanligtvis som rent skadliga vid cancer. Studien visar dock att när EMT och WNT aktiveras kraftigt hjälper de också till att driva TET2 in i kärnan. Med läkemedel och genetiska verktyg i cellkulturer visade forskarna att aktivering av EMT eller WNT ökade andelen celler som flyttade TET2 till sina kärnor, medan blockering av dessa vägar gjorde motsatsen. När TET2 väl var i kärnan dämpade det genuttryck kopplat till EMT och WNT, minskade cellmigration och bromsade proliferation. Med andra ord väcker samma signaler som hjälper tumörer att växa också en intern motkraft.
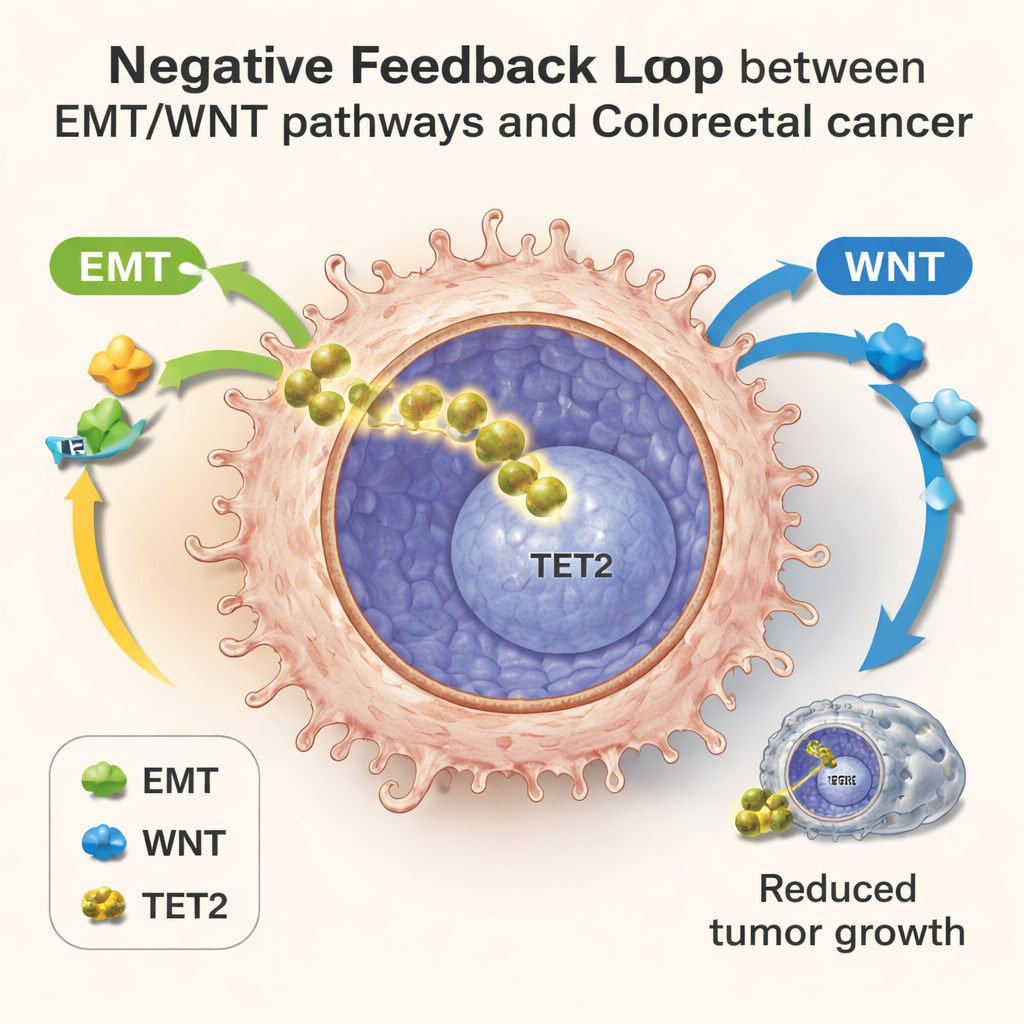
Encelliga analyser avslöjar en dold återkopplingsslinga
För att kartlägga detta dragkamp i detalj använde teamet encellig RNA‑sekvensering, som läser av vilka gener som är aktiva i tusentals individuella celler samtidigt. I laboratorieodlade kolonier, i musstumörer och i prover från patienter med kolorektalcancer såg de celler sprida sig längs en progresstidslinje. Tidiga celler visade normal energianvändning och svag EMT/WNT‑aktivitet; senare celler uppvisade omställning av metabolismen, starka EMT/WNT‑signaler och därefter stigande uttryck av TET2‑målgener. I dessa senare steg hade celler med högre TET2‑aktivitet lägre nivåer av invasionsrelaterade gener och var kopplade till bättre patientutfall, även bland tumörer som redan börjat sprida sig. Detta mönster stödjer idén om en negativ återkopplingsslinga: metabol stress och EMT/WNT‑aktivering driver TET2 in i kärnan, och nukleärt TET2 begränsar i sin tur dessa aggressiva program.
Vad detta betyder för framtida cancerbehandlingar
För icke‑specialister är huvudbudskapet att kolorektalcancerprogression inte är en enkel "på/av"‑omkopplare mellan gott och ont beteende. Istället finns en inbyggd, fördröjd säkerhetsmekanism: när tumörceller blir mer invasiva aktiverar de också TET2 i sina kärnor, vilket delvis hejdar dem. Med tiden lyckas många tumörer undkomma genom att förlora nukleärt TET2 eller överväldiga dess effekter. Genom att hitta sätt att hålla TET2 i kärnan eller öka dess aktivitet — möjligen i kombination med läkemedel som modulerar EMT eller WNT — skulle läkare kunna stärka denna naturliga broms och bromsa cancerutbredning. Istället för att enbart angripa cancerceller utifrån skulle framtida behandlingar kunna verka genom att återställa och förstärka detta interna kontrollsystem.
Citering: Li, C., Meng, F., He, J. et al. Cytoplasm-nucleus shuttling of TET2: an intrinsic brake in colorectal cancer progression. Cell Death Dis 17, 163 (2026). https://doi.org/10.1038/s41419-026-08418-5
Nyckelord: kolorektalcancer, TET2, epigenetik, EMT WNT‑signalering, cancerprogression