Clear Sky Science · sv
Avvikande bibehållande av utvecklingsfaktorn PAX6 främjar nervcellsdöd via JNK3-signalering
Varför denna forskning är viktig för synen
Glaukom är en ledande orsak till permanent blindhet, till stor del därför att de nervceller som för syninformation från ögat till hjärnan långsamt dör. Många behandlingar sänker ögontrycket, men människor kan ändå förlora synen även när trycket är väl kontrollerat. Den här studien ställer en djupare fråga: vad får dessa retinala nervceller att bestämma sig för att dö när de är utsatta för stress, och kan vi stänga av det beslutet på nivån för genreglering inne i cellkärnan?
En stressad näthinna under attack
I centrum för glaukom och närliggande ögonsjukdomar ligger den långsamma förlusten av retinala ganglieceller (RGC), ögats utgående neuroner. Dessa celler är känsliga för många typer av stress, inklusive toxiska nivåer av hjärnans budbärare glutamat, som överaktiverar NMDA-receptorer och utlöser skadlig kalciumöverbelastning. Forskarna använde en väletablerad musemodell där en liten mängd NMDA injiceras i ögat, vilket selektivt skadar RGC samtidigt som andra retinala lager i stort sett lämnas intakta. De bekräftade att denna behandling inte förändrade ögontrycket, men gav typiska tecken på programmerad celldöd i RGC, såsom frisättning av cytokrom c från mitokondrier och förekomst av TUNEL-positiva kärnor.
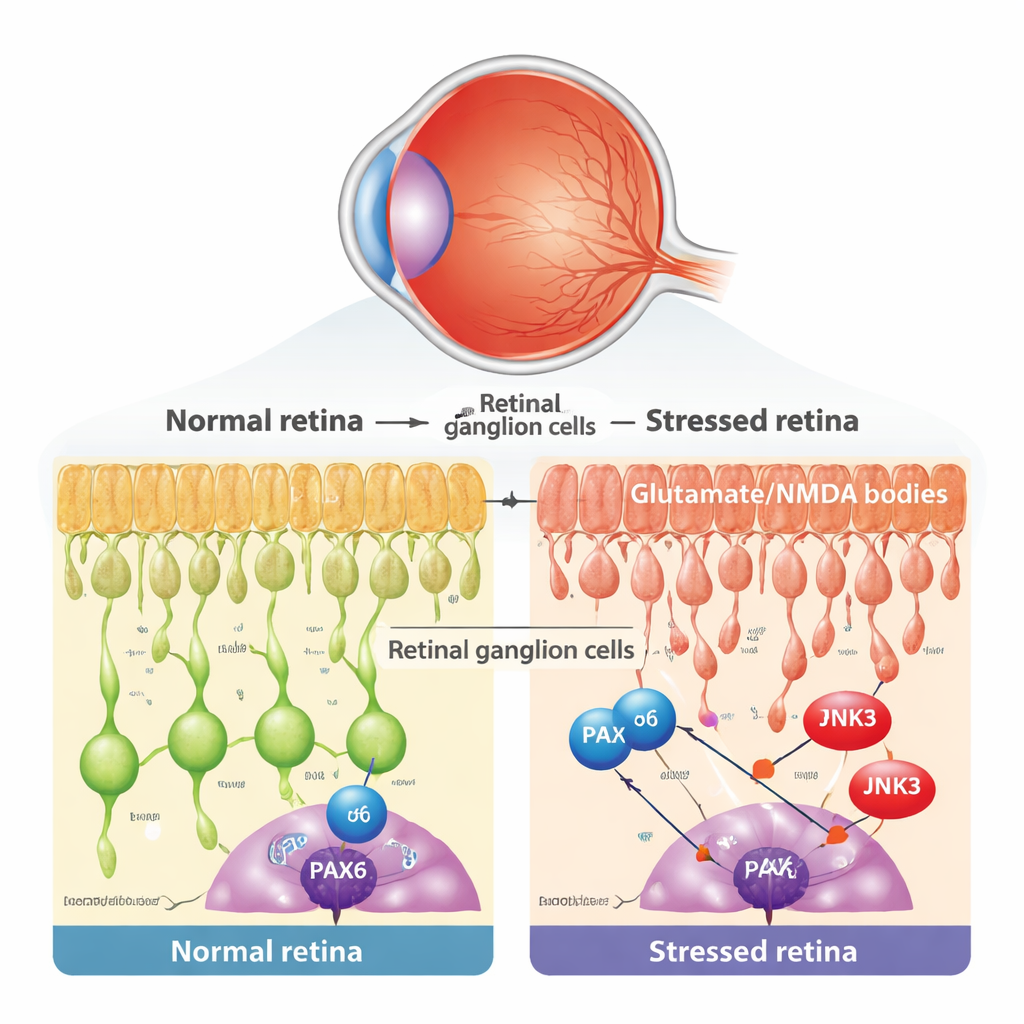
En utvecklingsgen som vägrar gå i pension
Under tidig utveckling fungerar en genregulator kallad PAX6 som en huvudarkitekt för ögat och styr hur olika retinala celler föds och kopplas ihop. Konventionell visdom säger att sådana utvecklingsprogram till största delen stängs av i vuxen ålder. Genom att omanalyssera enkelcells-RNA-sekvenseringsdata från både mus- och människoretina fann teamet att PAX6 faktiskt är starkt och selektivt bibehållen i mogna RGC och vissa interneuroner. Med mikroskopisk färgning visade de att i lagret där RGC finns är PAX6 till största delen närvarande i ganglieceller snarare än i närliggande amakrinceller. Detta väckte en intressant möjlighet: i vuxensjukdom kan ett gammalt utvecklingsprogram bli kapat och förvandlas till en drivkraft för degeneration.
Från väktare till bödel: PAX6 byter roll
För att testa om PAX6 hjälper RGC att överleva eller dö under stress använde forskarna ett genterapiliknande tillvägagångssätt. De levererade en viral vektor som bar en liten RNA som specifikt slår ned PAX6 i näthinnan, och utsatte sedan ögonen för NMDA. Jämfört med kontrollbehandlade ögon visade PAX6-nedslagna retina betydligt färre apoptotiska RGC och mycket mindre mitokondrieskada, vilket indikerar att PAX6 krävs för fullskalig celldöd i denna modell. Genom genomeomfattande RNA-sekvensering avslöjades att många dödsfrämjande gener, särskilt de som är involverade i mitokondrieskada och kaspaskaktivering, starkt inducerades av NMDA i normala möss men dämpades när PAX6 tystades. Med andra ord hjälper PAX6 till att slå på ett nätverk av gener som pushar RGC över stupet.
Stresskinasen som vänder PAX6-omkopplaren
Hur aktiverar stress PAX6 utan att öka dess mängd? Teamet fokuserade på JNK3, ett stressresponsivt enzym som främst återfinns i neuroner. Vid NMDA-skada flyttade JNK3 in i RGC-kärnan och associerade fysiskt med PAX6. Biokemiska "provrörsexperiment" med renade proteiner visade att JNK3 direkt kan lägga till fosfatgrupper på PAX6, och denna reaktion blockerades av en JNK-hämmare. I möss som saknar Jnk3-genen gav NMDA inte längre samma mönster av PAX6-fosforylering. Kromatinmappning (ChIP-seq) och riktade DNA-bindningsanalyser visade att fosforylerad PAX6, tillsammans med JNK3, under stress bindet starkare vid kontrollregioner för nyckelgener som främjar apoptos såsom Bax och Gadd45a, vilket ökar deras aktivitet. När antingen PAX6 slog ned eller JNK3 genetiskt togs bort minskade denna bindning och motsvarande aktivering av dödsfrämjande gener kraftigt.
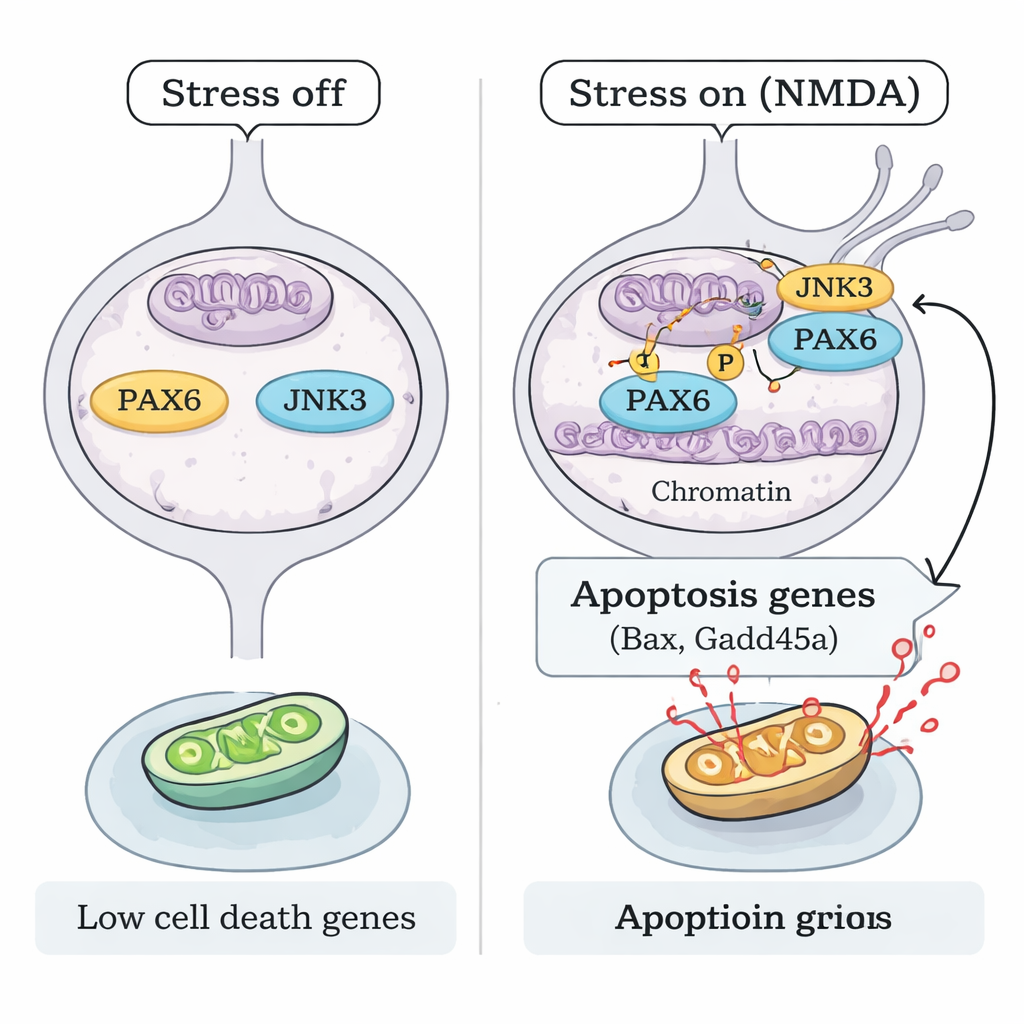
Stäng av dödsprogrammet för att skydda synen
Slutligen undersökte forskarna om blockering av denna JNK3–PAX6-axel räcker för att skydda synkritiska celler. Både i PAX6-nedslagna möss och i JNK3-defektiva möss bevarades RGC signifikant efter NMDA-exponering, med färre döende celler och en friskare retinal struktur. Detta pekar på en tydlig mekanistisk modell: under excitotoxisk stress fosforylerar JNK3 den persistenta PAX6, vilket omvandlar den från en utvecklingsbyggare till en potent aktivator av ett celldödsgenprogram i vuxna RGC. Att avbryta den länken — genom att tysta PAX6 eller inaktivera JNK3 — håller många av dessa neuroner vid liv. För patienter antyder detta arbete att framtida glaukombehandlingar kan gå bortom att sänka ögontrycket och istället rikta in sig direkt på de genetiska omkopplare som avgör om retinala neuroner lever eller dör.
Citering: Kim, JY., An, MJ., Kim, J. et al. Aberrant maintenance of developmental transcription factor PAX6 promotes neuronal cell death via JNK3 signaling. Cell Death Dis 17, 161 (2026). https://doi.org/10.1038/s41419-026-08417-6
Nyckelord: glaukom, retinala ganglieceller, PAX6, JNK3, neurodegeneration