Clear Sky Science · sv
Målinriktning av ENO1 omprogrammerar makrofagpolarisation för att utlösa antitumörimmunitet och förbättrar radioterapins terapeutiska effekt
Göra tumörernas sköldar till mål
Cancer överlever ofta inte bara genom snabb tillväxt utan också genom att tyst slå ut kroppens försvar. Denna studie undersöker en dold molekyl på cancerceller, kallad ENO1, som hjälper tumörer att undvika immunsystemet och motstå strålbehandling. Genom att utveckla ett nytt antikroppsbaserat läkemedel som riktar sig mot ENO1 visar forskarna att det är möjligt att tömma tumören på dess skyddande kemikalier, väcka immunceller och få strålbehandling att fungera bättre i modeller av kolorektal cancer och trippelnegativ bröstcancer. 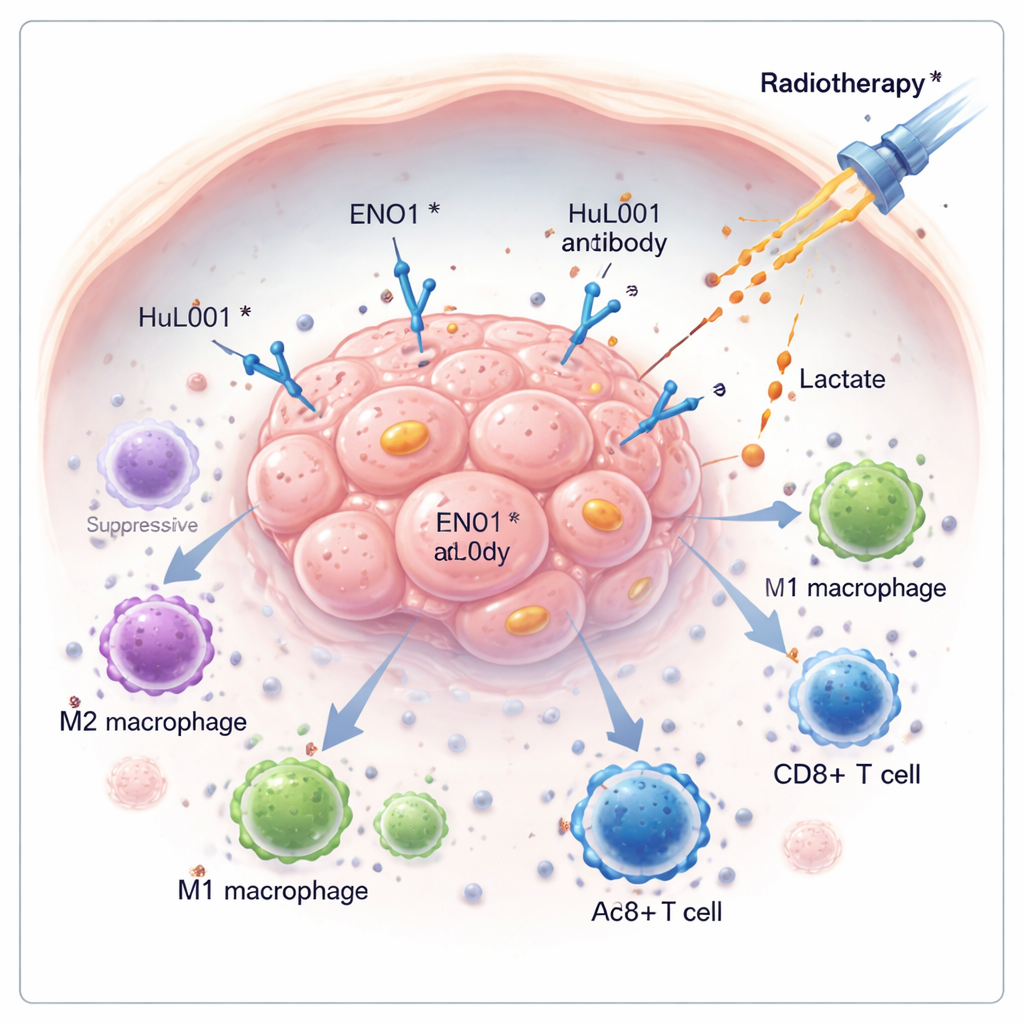
En metabolisk fälla som tystar immuniteten
Många tumörer omprogrammerar sin energianvändning och bryter ner socker på ett sätt som producerar stora mängder mjölksyra även när syre finns tillgängligt. Denna mjölksyra pumpas ut från cancercellerna och samlas runt tumören, vilket omvandlar omgivningen till en sur nisch som försvagar immunsvaret. I detta arbete fokuserar författarna på ENO1, ett enzym som deltar i sockeromsättningen och som också kan förekomma på cancercellens yta. När ENO1 sitter på cellytan samarbetar det med ett annat protein, transportören MCT4, för att hjälpa till att exportera laktat—vilket driver fram en miljö som gynnar tumörtillväxt och undertrycker immunceller.
Hur strålning kan slå fel
Strålbehandling är avsedd att skada tumörens DNA och utlösa immunsvar, men den har också biverkningar inne i tumörmikromiljön. Teamet upptäckte att signaler drivna av en molekyl kallad TGFβ1, som förstärks av strålning, aktiverar ett enzym (PRMT5) som kemiskt modifierar ENO1 och flyttar det till cancercellens yta. När ENO1 väl finns där interagerar det fysiskt med MCT4 för att stabilisera det och främja laktatexport. Högre nivåer av ytbundet ENO1 hittades hos patienter med avancerad kolorektal cancer och trippelnegativ bröstcancer och kopplades till fler metastaser och sämre överlevnad, vilket antyder att strålning ofrivilligt kan stärka en laktatdriven, immunhämmande sköld runt tumörer.
Omprogrammering av både vänliga och fientliga immunceller
I den sura zonen runt tumörer pressas immunceller som kallas makrofager in i ett "läknings"-tillstånd (ofta kallat M2) som faktiskt hjälper tumörer genom att dämpa inflammation och bistå reparation, i stället för att döda cancerceller. Forskarna skapade en humaniserad antikropp, HuL001, som känner igen ENO1 på både mus- och människocancerceller. I cellodlingar och musmodeller störde HuL001 ENO1:s stöd för MCT4, minskade laktatutsläpp och förskjöt makrofager från det tumörfrämjande M2-tillståndet mot ett M1-tillstånd, vilket är mer aggressivt mot cancer och bättre på att äta upp tumörceller. Viktigt är att HuL001 inte helt enkelt dödade makrofager; snarare omutbildade den dem samtidigt som den direkt ökade cancercellsdöd.
Få strålterapi att fungera bättre
När HuL001 kombinerades med strålbehandling i musmodeller av kolorektal cancer och trippelnegativ bröstcancer krympte tumörerna mer, växte tillbaka långsammare och försvann i många djur helt. 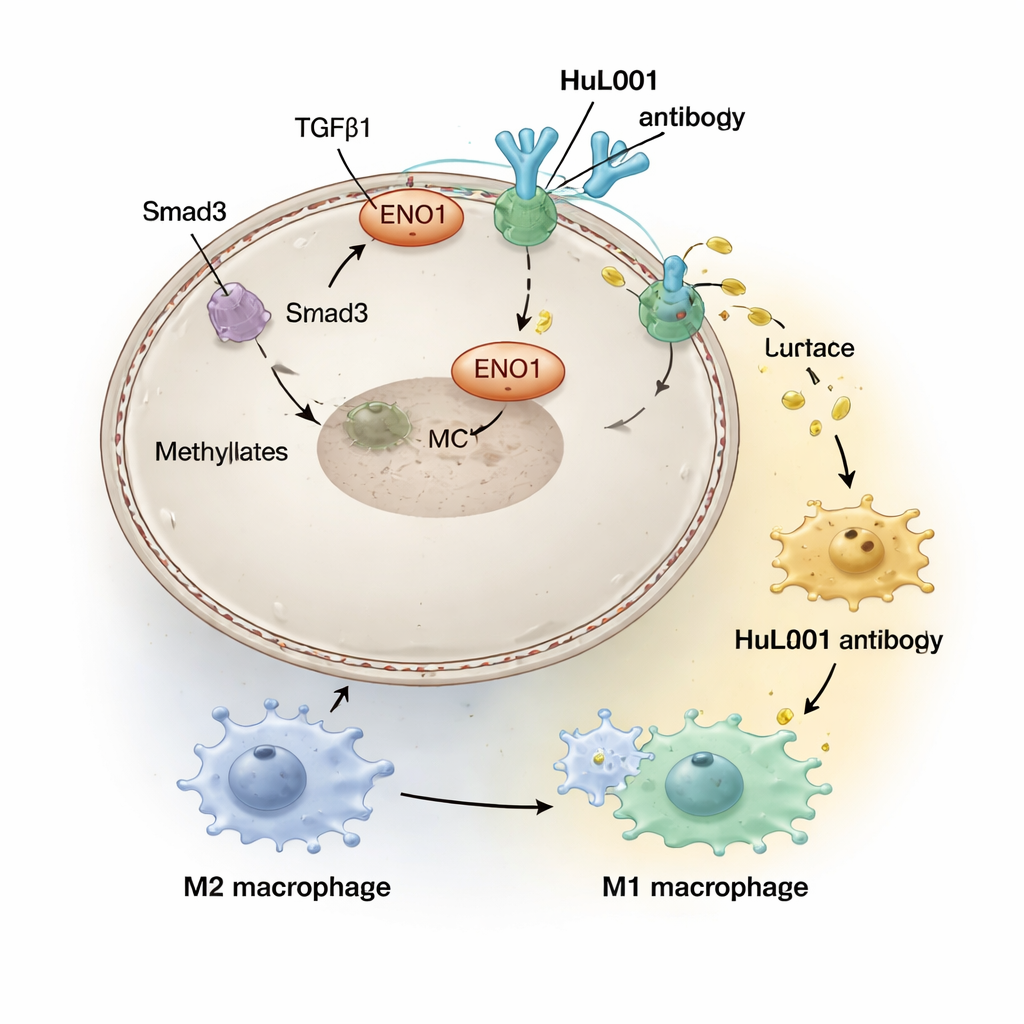
Från komplexa vägar till praktiskt löfte
För icke-specialister är budskapet i denna studie att en tumörs kemi och dess grannskap av immunceller är djupt sammanflätade. ENO1 sitter vid ett vägskäl: det hjälper tumörer att bränna socker, exportera mjölksyra och rekrytera fel sorts immunsvar. Genom att blockera ytbundet ENO1 med en riktad antikropp kunde forskarna minska skadlig laktatansamling, vända makrofager från tumörhjälpare till tumörbekämpare och göra strålbehandlingen mer effektiv i svårbehandlade cancertyper. Även om HuL001 ännu inte är ett kliniskt läkemedel tyder arbetet på att inriktning mot metabola grindvakter som ENO1 kan bli ett kraftfullt sätt att vända tumörens egna försvar mot den och förbättra befintliga terapier som radioterapi.
Citering: Lin, YS., Chang, HY., Hong, WZ. et al. Targeting ENO1 reprograms macrophage polarization to trigger antitumor immunity and improves the therapeutic effect of radiotherapy. Cell Death Dis 17, 194 (2026). https://doi.org/10.1038/s41419-026-08416-7
Nyckelord: tumörmetabolism, makrofagpolarisation, strålbehandling, immunoterapi, laktat