Clear Sky Science · sv
Sec8: en ny positiv regulator av RIG-I i försvaret mot RNA‑virus
Hur våra celler upptäcker listiga virus
Många farliga virus, inklusive influensa och nydanande zoonotiska virus, bär sitt genetiska material som RNA. Våra celler förlitar sig på interna larm för att snabbt upptäcka dessa inkräktare och utlösa ett antiviralt svar. Denna studie undersöker ett relativt okänt cellprotein kallat Sec8 och visar att det diskret spelar en central roll för att hålla en av våra viktiga virussensorer, RIG‑I, vid liv och aktiv tillräckligt länge för att skydda oss.
Ett cellulärt inbrottslarm hotas
RIG‑I är ett molekylärt ”inbrottslarm” som patrullerar inne i cellerna efter tecken på viralt RNA. När det upptäcker misstänkt RNA ändrar det form, aktiveras och skickar signaler som i slutändan utlöser typ I‑interferoner—potenta varningsmolekyler som hjälper närliggande celler att stå emot infektion och aktivera immunförsvaret. Eftersom ett överaktivt larm kan orsaka skadlig inflammation eller autoimmunitet reglerar cellerna RIG‑I‑nivåerna noggrant. Flera andra proteiner kan märka RIG‑I för destruktion genom att fästa små ubikvitinkedjor, vilket leder det till cellens ”papperskvarn” — proteasomen. Fram till nu var det oklart vilka ytterligare cellulära faktorer som skyddar RIG‑I från att bli förtidigt nedbrutet, särskilt under aktiv RNA‑virusinfektion.
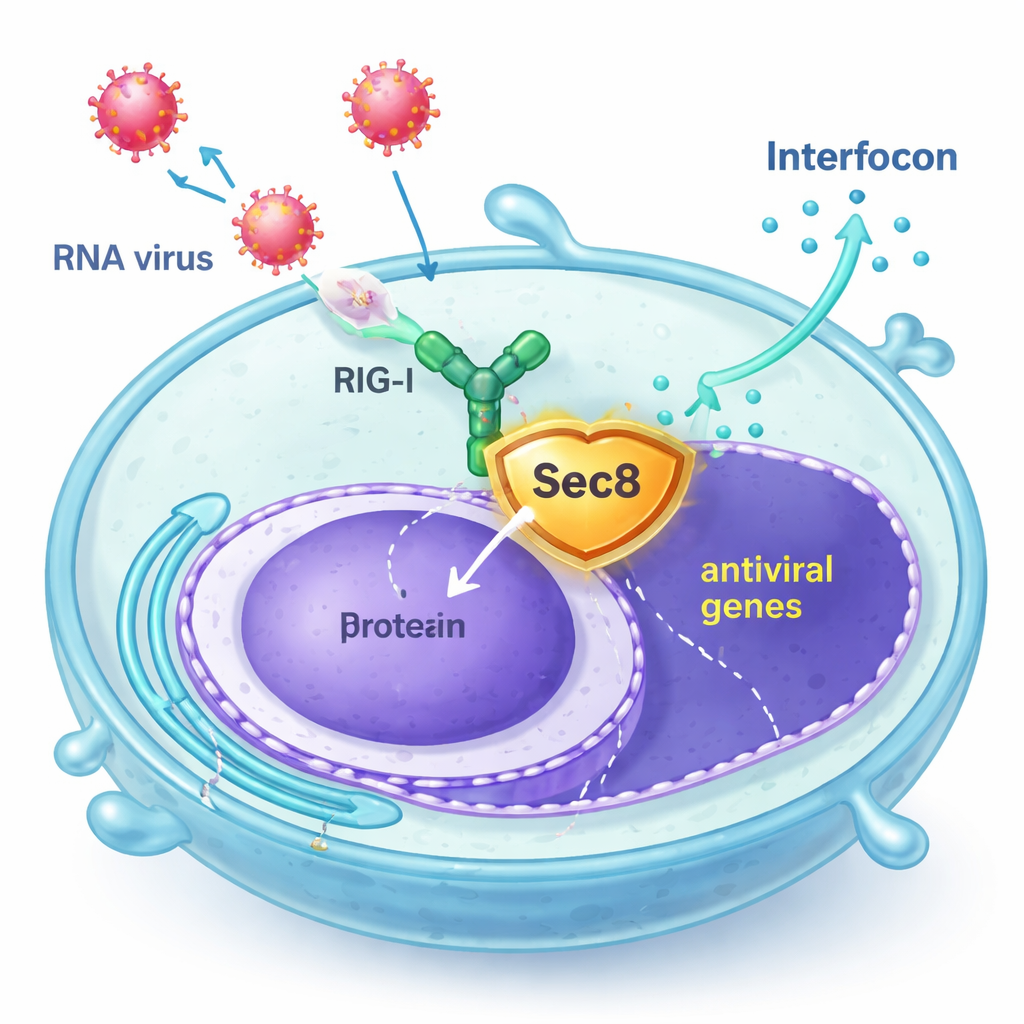
Sec8 kliver in som livvakt
Författarna upptäckte att Sec8, mest känt som en del av ett åttondeligt proteincomplex som hjälper sekretoriska vesiklar att fusera med cellens yta, faktiskt förstärker antiviralsignaleringen. I humana cellinjer och i primära immunceller från mus ledde ökade Sec8‑nivåer till starkare aktivering av interferonrelaterade gener efter infektion med RNA‑virus som vesikulärt stomatitvirus (VSV) och Sendai‑virus, eller efter exponering för syntetiskt viralt RNA. Omvänt minskade interferonproduktionen och uttrycket av interferonstimulerade gener när Sec8 reducerades, vilket lämnade cellerna sämre rustade att motstå virusreplikation. Dessa fynd tyder på att Sec8 inte bara deltar i sekretion utan fungerar som en positiv regulator inom det antivirala larmsystemet.
Blockering av den cellulära papperskvarnen
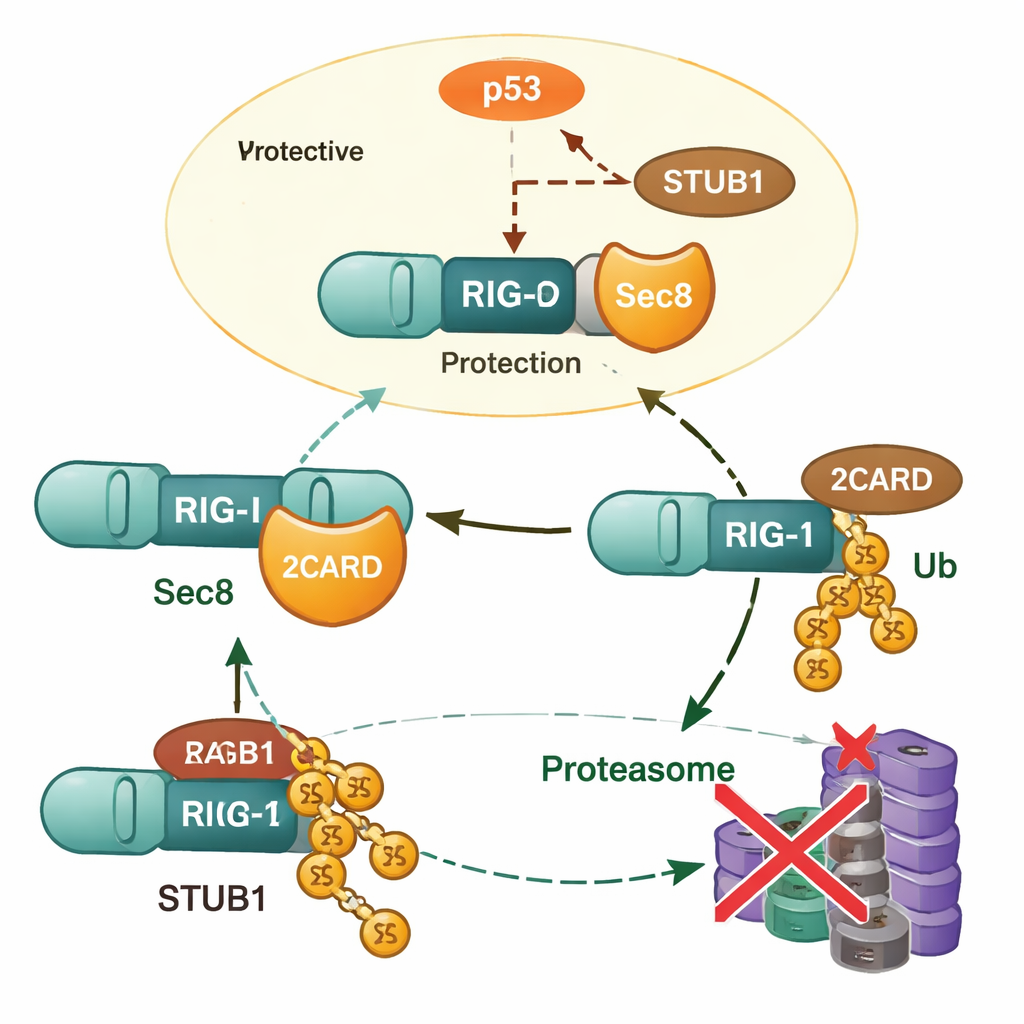
Vid djupare analys fann forskarna att Sec8 inte ökar RIG‑I:s genuttryck; istället förhindrar det att RIG‑I‑proteinet bryts ned. När Sec8 togs bort sjönk RIG‑I‑nivåerna snabbare, och denna förlust kunde förhindras av läkemedel som blockerar proteasomen, vilket pekar på cellens proteinåtervinningsmaskineri. Teamet identifierade ett annat protein, STUB1, som en nyckelaktör som fäster en specifik typ av ubikvitinkedja (K48‑kopplad) på RIG‑I vid aminosyran lysin 190. Denna märkning riktar RIG‑I för destruktion. Sec8 stör denna process på två sätt: det konkurrerar fysiskt med STUB1 om bindning till samma aktiveringsregion på RIG‑I, och det sänker mängden STUB1 som cellen producerar från början.
Sec8, p53 och kontrollen av märkaren
För att förklara hur Sec8 minskar STUB1‑produktionen vände författarna sig till genreglering. De lokaliserade ett kort DNA‑stycke som fungerar som kärn‑på/av‑knapp (promotor) för STUB1‑genen och visade att den välkända tumörsuppressorn p53 binder detta område och ökar STUB1‑nivåerna. Sec8 dämpade både mängden p53 och dess aktiverande fosforylering, så att p53 inte längre kunde driva STUB1‑produktionen lika effektivt. När p53 blockerades eller STUB1 tystades ner återställdes till stor del de skadliga effekterna av Sec8‑bortfallet på interferonproduktionen och virusväxten. Detta placerar Sec8 högst upp i en regleringskedja som går från p53 till STUB1 och slutligen till RIG‑I‑stabilitet.
Från petriskål till levande djur
Teamet testade sedan Sec8:s betydelse i möss som genetiskt modifierats för att sakna Sec8‑genen specifikt i vissa immunceller. Efter infektion med VSV producerade dessa djur mindre interferon, hade högre virusmängder i organ som mjälte, lever och lungor, och uppvisade allvarligare lungskador, större viktminskning och lägre överlevnad än kontrollmössen. Dessa in vivo‑resultat bekräftade att Sec8 inte är en obetydlig aktör utan en betydande skyddare mot RNA‑virusinfektion i en hel organism.
Varför detta betyder något för framtida terapier
Enkelt uttryckt visar denna studie att Sec8 fungerar som en livvakt för den antivirala sensorn RIG‑I. Genom att hålla den ”märkande” proteinen STUB1 i schack och direkt skydda RIG‑I från att skickas till den cellulära papperskvarnen tillåter Sec8 celler att snabbt ge ett interferonsvar och bättre kontrollera RNA‑virus. Förståelsen av den nydeskriva p53–STUB1–RIG‑I‑axeln öppnar dörren för framtida antivirala strategier som stabiliserar RIG‑I eller efterliknar Sec8:s skyddande funktioner, vilket potentiellt kan stärka vårt försvar mot ett brett spektrum av RNA‑baserade virusinfektioner.
Citering: Wang, L., Ma, W., Hou, P. et al. Sec8: a novel positive regulator of RIG-I in anti-RNA viral defense. Cell Death Dis 17, 165 (2026). https://doi.org/10.1038/s41419-026-08414-9
Nyckelord: medfödd immunitet, RNA‑virus, RIG-I, ubikvitinering, interferon‑signalering