Clear Sky Science · sv
Överföring av laktat från hypoxiska tumörceller främjar makrofagsenescens och M2‑polarisation via DNMT1‑NHE7‑axeln och accelererar endometriecancerprogression
Varför det spelar roll att svälta tumörer på syre
Endometriecancer, som uppstår i livmoderslemhinnan, blir allt vanligare globalt. Många avancerade tumörer är svåra att behandla eftersom de återkommer, sprider sig eller är resistenta mot standardbehandlingar. Denna studie undersöker vad som händer inuti dessa tumörer när de får för lite syre — en vanlig egenskap hos snabbt växande cancerformer — och visar hur en enkel avfallsprodukt, laktat, kan omprogrammera närliggande immunceller så att de hjälper cancern att växa istället för att bekämpa den.
Lågt syre förvandlar tumörer till laktatfabriker
När endometriecancerceller förökar sig hinner inte blodförsörjningen med, vilket skapar områden med lågt syre, eller hypoxi. Cellerna svarar genom att slå på en huvudregulator kallad HIF1A som omställer deras energiproduktion. Istället för att förlita sig främst på effektiv energiproduktion ökar cellerna glykolysen, en snabb men ineffektiv process som producerar stora mängder laktat. Forskarna analyserade tumördata från hundratals patienter och fann att högre nivåer av HIF1A korrelerade med ökad aktivitet i många gener och transportörer kopplade till glykolys och utsöndring av laktat från cancercellerna. Patienter med tumörer som hade mer HIF1A tenderade att ha sämre utfall, vilket tyder på att detta metaboliska skifte är nära kopplat till aggressiv sjukdom.
Hur tumöravfall formar om hjälpsamma immunceller
Makrofager är immunceller som antingen kan attackera tumörer eller stödja dem, beroende på sitt tillstånd. I detta arbete visade teamet att under hypoxi frisätter endometriecancerceller mycket mer laktat i sin omgivning. Detta laktat exporteras via en transportör kallad MCT3 på tumörcellerna och importeras sedan in i makrofager via en annan transportör, MCT1. När laktatet väl är inne får det makrofagerna att avvika från ett försvarande läge och istället anta den så kallade M2‑staten, som är förknippad med vävnadsreparation, dämpning av inflammation och, olyckligtvis, stöd för tumörtillväxt. I laboratorieexperiment visade makrofager som exponerats för laktatrik tumörvätska fler markörer för M2‑typen, och den vätska de i sin tur sekreterade ökade cancercellernas tillväxt, rörlighet och invasion. 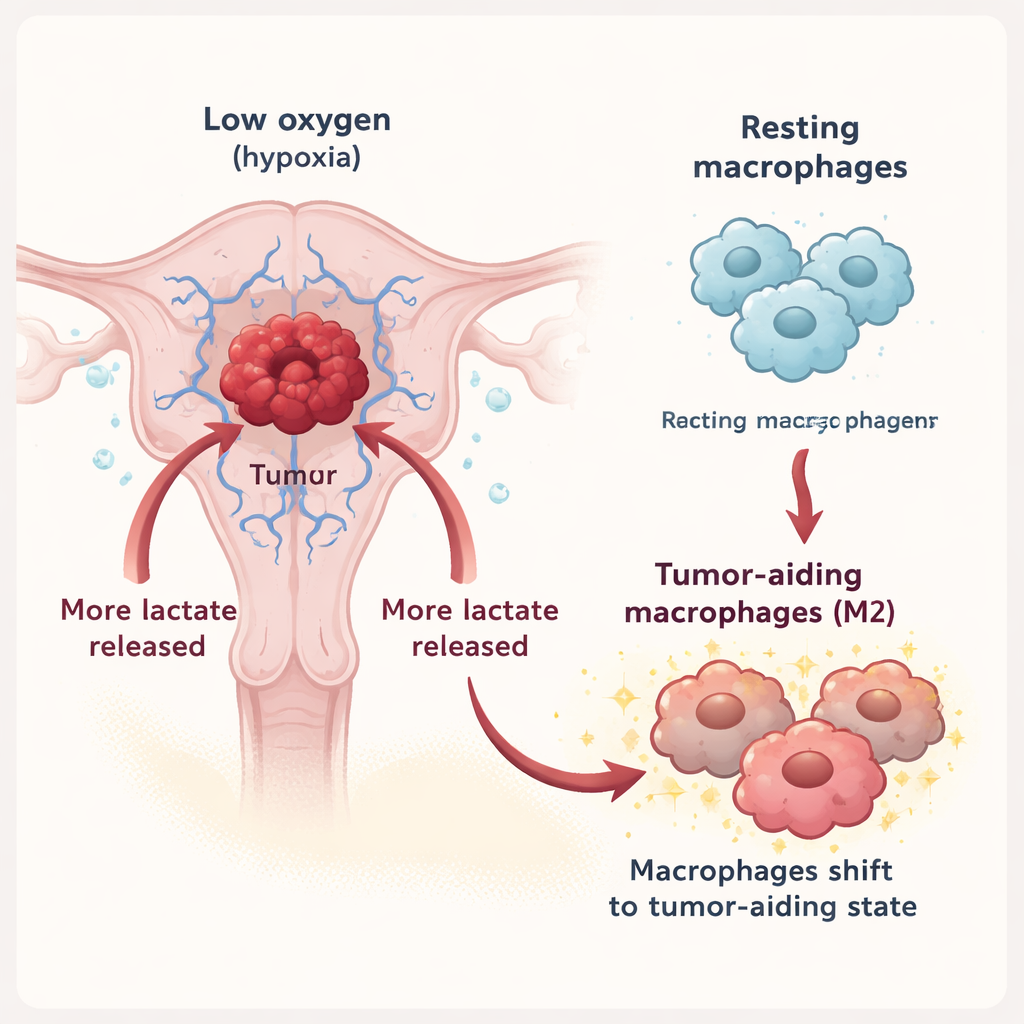
En epigenetisk strömbrytare som tystar en cellulär ”pH‑ventil”
Studien går ett steg längre genom att avslöja den molekylära strömbrytaren inne i makrofager som kopplar tumör‑härlett laktat till detta skadliga beteende. Laktat flyter inte bara omkring; det kan dekorera histonproteiner i cellkärnan — en kemisk märkning kallad laktatylering — som påverkar vilka gener som är aktiva eller tysta. Forskarna fann att laktat ökar en specifik histonmarkör i kontrollregionen för DNMT1‑genen och därigenom höjer dess aktivitet. DNMT1 är ett enzym som lägger till metylgrupper på DNA och kan tysta gener. Ett av dess mål här är NHE7, ett protein som hjälper till att kontrollera surhetsgraden i vissa cellkompartiment. När DNMT1 ökar leder det till ökad metylering av NHE7‑genen och minskad uttryck. Minskad NHE7 stör det interna pH‑balanssystemet och aktiverar en signalväg känd som MAPK‑banan. Denna bana driver i sin tur makrofager mot den tumörvänliga M2‑staten och en form av åldrande kallad senescens, vilket låser dem i ett kroniskt, tumörfrämjande läge.
Från molekylär kedjereaktion till snabbare växande tumörer
För att avgöra om denna händelsekedja spelar roll i levande organismer skapade forskarna musmodeller där mänskliga endometriecancerceller odlades tillsammans med mänskliknande makrofager. När extra laktat tillfördes växte tumörerna större, visade fler delande celler och innehöll fler M2‑typ‑senescenta makrofager med högt DNMT1 och lågt NHE7. Slående nog dämpade överuttryck av NHE7 i makrofager den tumörfrämjande effekten av laktat: tumörerna blev mindre, hade fler döende celler och innehöll färre M2‑ och senescenta makrofager. Att blockera DNMT1‑enzymet eller MAPK‑vägen försvagade också laktatets förmåga att omprogrammera makrofager och stärker idén att dessa molekyler bildar en sammanhängande axel. 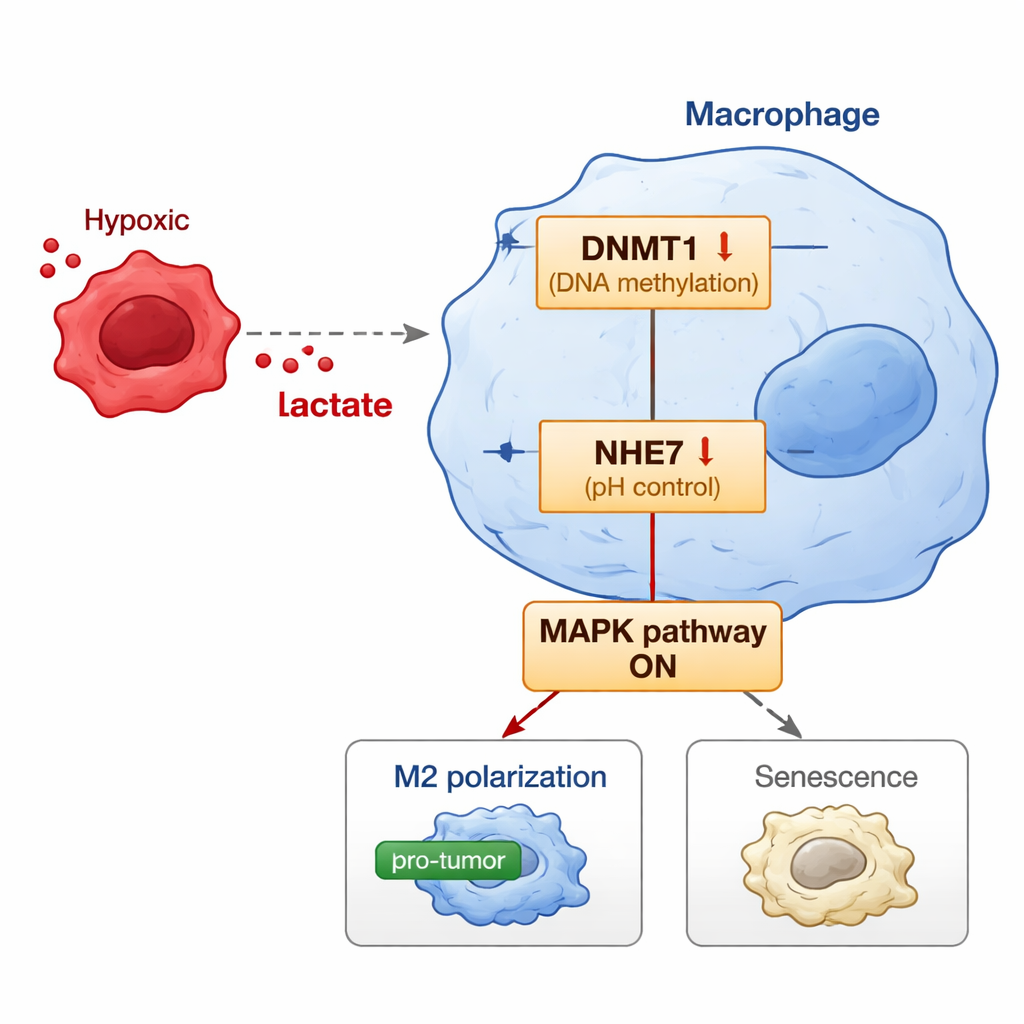
Göra tumörens egna knep till behandlingsmål
För icke‑specialister är huvudbudskapet att endometrietumörer kan utnyttja lågt syre och laktat — förr betraktat som rena cellulära restprodukter — för att ”hjärntvätta” närliggande immunceller till att hjälpa cancern. De gör detta genom ett epigenetiskt relä: laktat ökar DNMT1, vilket tystar NHE7, som i sin tur aktiverar signalering som fixerar makrofager i ett tumörvänligt, åldrande tillstånd. Genom att störa något steg i denna laktat–DNMT1–NHE7–MAPK‑kedja kan det vara möjligt att återställa mer anti‑tumöraktivitet i immunförsvaret och bromsa cancerutvecklingen. Detta arbete pekar mot framtida terapier som inte bara riktar sig direkt mot cancercellerna utan också omutbildar de omgivande immunceller som tumören har vänt till sin fördel.
Citering: Yang, S., Ma, Y., Wu, T. et al. Lactate transmission from hypoxic tumor cells promotes macrophage senescence and M2 polarization via the DNMT1-NHE7 axis to accelerate endometrial cancer progression. Cell Death Dis 17, 185 (2026). https://doi.org/10.1038/s41419-026-08411-y
Nyckelord: endometriecancer, tumörmikromiljö, laktatmetabolism, makrofagpolarisation, epigenetisk reglering