Clear Sky Science · sv
Bortom ämnesomsättningen: att utforska de reglerande och terapeutiska följderna av laktat och laktlylering vid cancerreglerad celldöd
Varför en ”avfallsprodukt” från socker spelar roll för cancer
I årtionden avfärdades laktat — ämnet som får överansträngda muskler att bränna — som cellulärt skräp. Denna översiktsartikel visar att laktat vid cancer inte är något avfall. Det fungerar som bränsle, som en kemisk signal och till och med som en strömbrytare som kan avgöra om tumörceller lever eller dör. Att förstå denna dolda roll kan öppna nya vägar för att få cancerceller att självförstöra medan friska vävnader skonas.
Sockrets genväg som omprogrammerar cancerceller
Cancerceller är ökända för sin ”söta tand.” Även när syre finns i överflöd föredrar de att snabbt bryta ned glukos till laktat istället för att fullständigt förbränna det i mitokondrierna — en förskjutning känd som Warburg-effekten. Denna strategi låter tumörer generera energi och byggstenar i hög takt. Den resulterande floden av laktat pumpas ut genom särskilda transportörer och skapar en sur, näringsrik tumörmikromiljö som stödjer tillväxt och hjälper tumörer att anpassa sig till stress, såsom låg syrehalt eller kemoterapi.
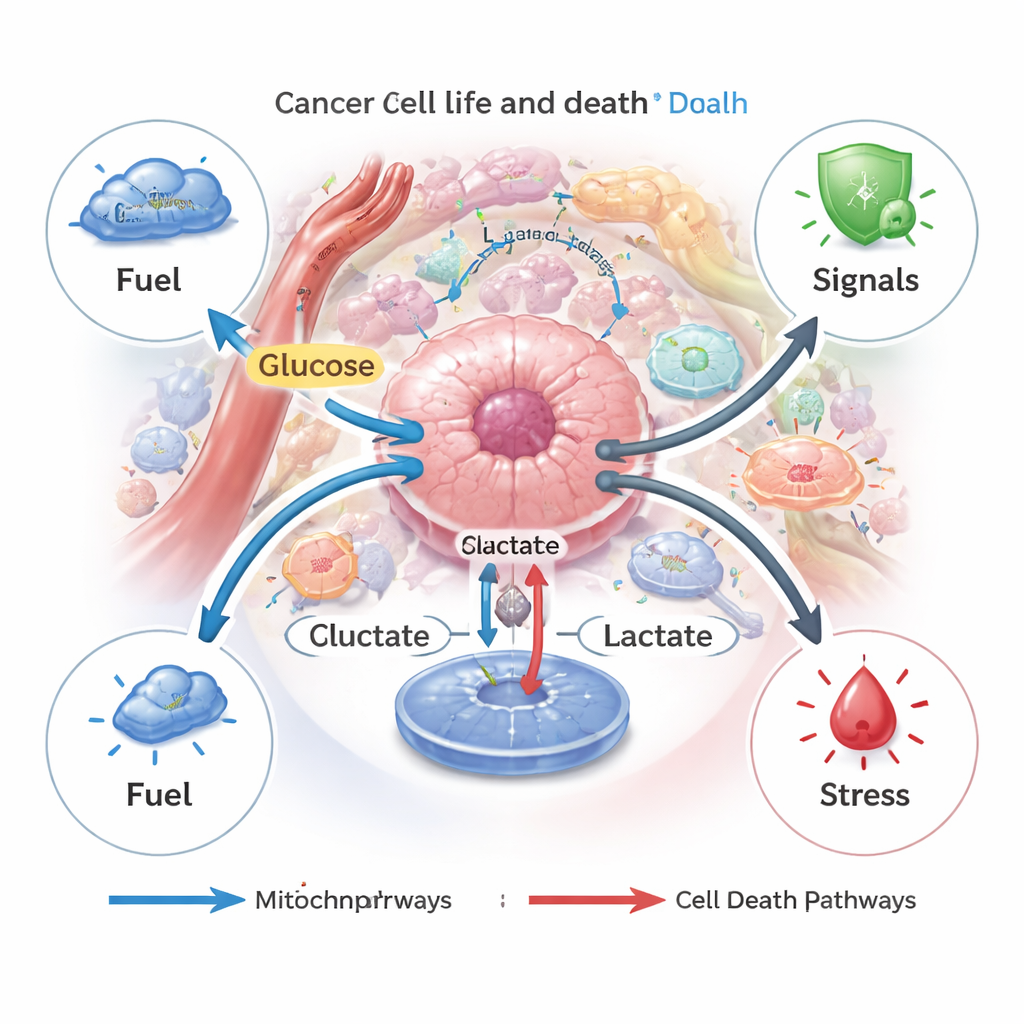
Laktat som reglage för olika typer av celldöd
Celldöd i våra kroppar är vanligtvis noggrant kontrollerad och hjälper till att avlägsna skadade eller farliga celler. Cancerceller undkommer ofta dessa program. Författarna beskriver hur laktat både kan blockera och utlösa flera reglerade dödsvägar — apoptos (cellens ”självmord”), autophagi (självnedbrytning), ferroptos (järndriven membranskada), pyroptos (inflammatorisk sprängning) och cuproptos (koppar‑driven kollaps). När cancerceller själva producerar eller importerar måttliga mängder laktat tenderar de att använda det som bränsle och som en överlevnadssignal, genom att slå på vägar som skyddar dem från kemoterapi, näringsbrist eller riktade läkemedel. Men när laktat byggs upp inuti celler — till exempel om dess export blockeras — kan den resulterande syrastressen och mitokondrieskadan vända spaken och driva cellerna mot apoptos eller ferroptos istället.
Laktlylering: när laktat skriver på proteiner
En iögonfallande ny upptäckt är att laktat kan omvandlas till en liten kemisk märkning och fästas på lysinrester i proteiner, en modifiering som kallas laktlylering. Enzymer fungerar som ”skrivare” och ”raderare” av dessa märkningar och dekorerar både DNA‑associerade histoner och många andra proteiner. Dessa markörer ändrar vilka gener som är aktiva, hur enzymer beter sig och hur stabila nyckelregulatorer är. I cancer finjusterar laktlylering balansen mellan överlevnad och självförstörelse. Den kan till exempel öka nivåerna av proteiner som blockerar apoptos, trappa upp återvinning via autophagi, skydda celler från ferroptos genom att strama åt järnkontrollen och öka antioxidanter, eller förändra nyare dödsformer som cuproptos genom att påverka hur celler hanterar kopparkänsliga proteiner.
En tvåvägskommunikation mellan metabolism och dödsprogram
Relationen är inte ensidig: celldödsprogram omformar också hur tumörer använder socker och producerar laktat. När mitokondrier skadas under tidig apoptos eller mitofagi (selektiv borttagning av mitokondrier) faller celler ofta tillbaka på snabb glykolys, vilket ökar laktatproduktionen. Omgivande stödjeceller, såsom cancerassocierade fibroblaster, kan genomgå liknande omprogrammering och bli laktatfabriker som matar närliggande tumörceller. Andra typer av död, som ferroptos, tenderar att undertrycka glykolys och därmed sänka laktatnivåerna. Resultatet är en dynamisk återkopplingsslinga där metabolism och dödsmekanismer ständigt anpassar sig till varandra i takt med att tumören utvecklas och svarar på behandling.
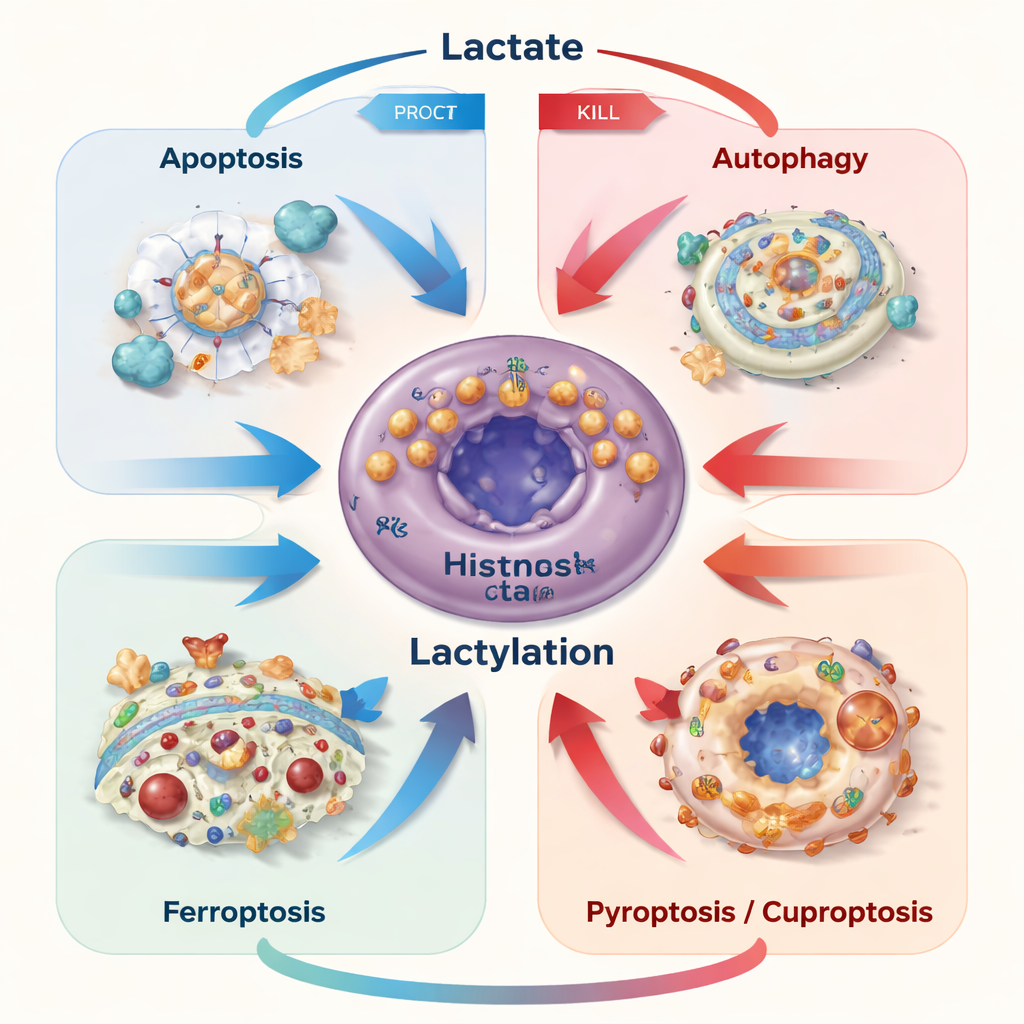
Att vända en svaghet till en behandlingsstrategi
Eftersom laktat och laktlylering beroende på sammanhang kan skydda eller döda cancerceller argumenterar författarna för att terapier måste göra mer än att bara blockera laktatproduktionen. Istället kan framtida behandlingar selektivt leda om laktatflöden, justera dess transportörer eller rikta in sig på specifika laktlyleringsmärken för att få cancerceller att gå över kanten samtidigt som antitumöra immunceller återaktiveras som för närvarande paralyserats av den sura miljön. Smart läkemedelsleverans och nanomediciner som reagerar på lokala laktat‑ eller pH‑nivåer framträder som sätt att tillämpa denna precision. I enkla termer är artikelns budskap att det som en gång såg ut som metabolt skräp faktiskt är en kraftfull kontrollknapp för cancercellernas öde — och att lära sig vrida den åt rätt håll skulle kunna göra befintliga terapier mycket mer effektiva.
Citering: Chen, C., Lin, A., Zhao, J. et al. Beyond metabolism: exploring the regulatory and therapeutic implications of lactate and lactylation in cancer-regulated cell death. Cell Death Dis 17, 184 (2026). https://doi.org/10.1038/s41419-026-08410-z
Nyckelord: laktat, laktlylering, cancercelldöd, tumörmetabolism, ferroptos