Clear Sky Science · sv
Spektrum och funktioner hos jonkanaler och transportörer i osteoklaster
Varför våra ben behöver små grindvakter
Vårt skelett ser solitt och oföränderligt ut, men det bryts ständigt ned och byggs upp på nytt. Specialiserade celler som kallas osteoklaster fungerar som rivningsarbetare och löser upp gammalt ben så att nytt kan bildas. Denna översiktsartikel undersöker en dold skara mikroskopiska ”grindvakter” — jonkanaler och transportörer — som tillåter laddade atomer och näringsämnen att röra sig in och ut ur osteoklaster. Genom att förstå hur dessa små portar styr bennedbrytning hoppas forskare kunna utforma bättre behandlingar för benskörhet och andra bensjukdomar.
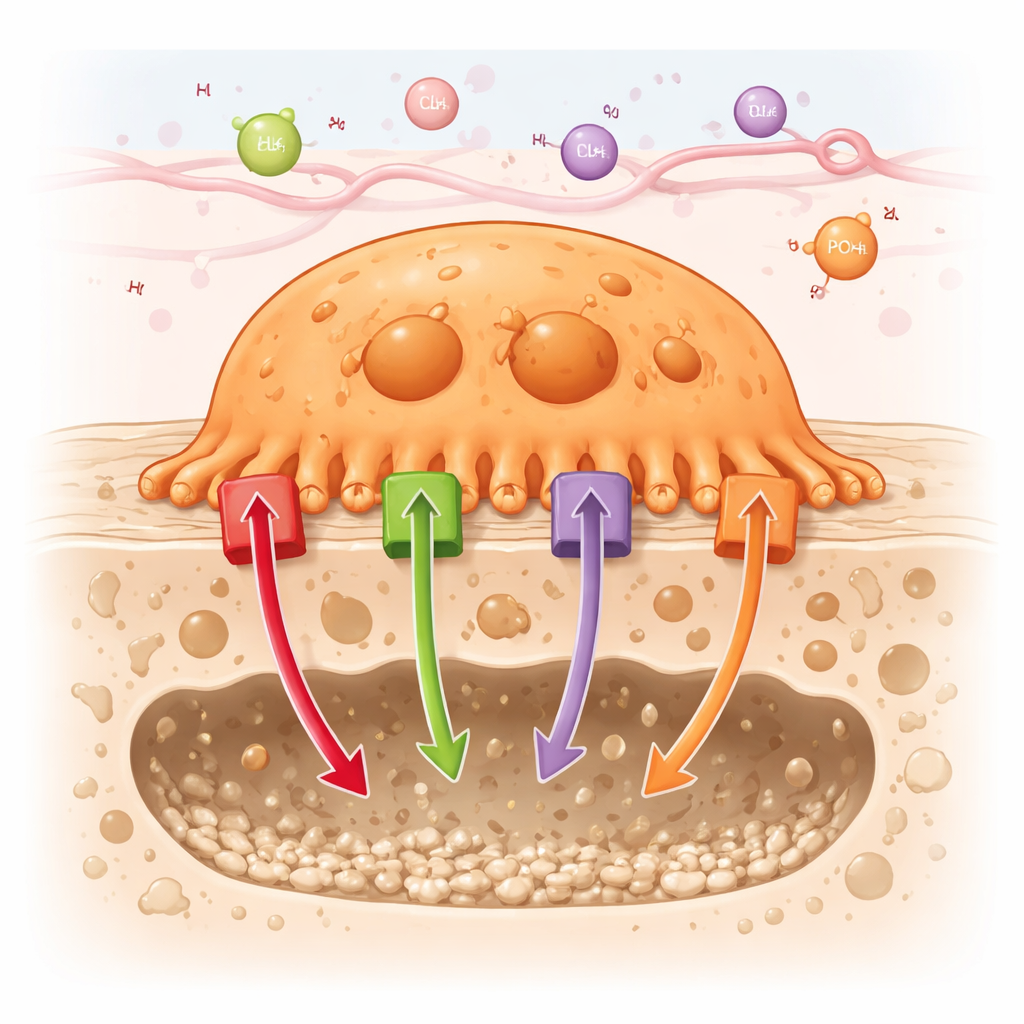
Hur benätande celler utför sitt arbete
Osteoklaster fäster sig tätt mot benytan och skapar ett avskärmat fack där de säkert kan lösa upp mineral och bryta ner proteiner. För att göra denna lilla ”matsmältningskammare” extremt sur pumpar osteoklaster stora mängder protoner (vätejoner) in i facket. Samtidigt transporterar de andra joner — som klorid, kalcium och fosfat — genom sina membraner och interna kompartment. Artikeln går igenom cirka 90 olika kanaler och transportörer som hittas i osteoklaster och grupperar dem i sex familjer, inklusive energidrivna pumpar (ATPaser), katjon‑ och anjonkanaler, kopplade transportörer, näringsbärare och ATP‑bindande kassett‑(ABC)transportörer.
Syra, salt och energi: kärnmaskineriet
Två proteinsystem framstår som centrala för bennedbrytning. För det första driver vakuolära protonpumpar, kända som V‑ATPaser, aktivt protoner in i resorptionsfacket och gör det tillräckligt surt för att lösa upp benmineral och aktivera proteinnedbrytande enzymer. Specifika V‑ATPase‑subenheter, såsom a3, d2 och flera V1‑komponenter, är rikligt förekommande vid osteoklastens skrynkliga rand och i lysosomer, och genetiska defekter i dessa subenheter kan antingen försvaga ben eller orsaka onormal benförtjockning. För det andra tar en klorid–proton‑utbytare kallad ClC‑7, som samarbetar med ett protein vid namn OSTM1, in kloridjoner till samma område. Detta balanserar elektrisk laddning och möjliggör kontinuerlig protonpumpning. När ClC‑7 är muterat utvecklar människor och möss osteopetros, ett tillstånd som kännetecknas av överdrivet täta men sköra ben, vilket illustrerar hur avgörande korrekt jonflöde är för normalt skelettillstånd.
Kalcium, fosfat och andra stödspelare
Utöver syraproduktionen är osteoklaster beroende av finjusterad hantering av kalcium och fosfat. Ett nätverk av kalciumkanaler och pumpar i cellmembranet, det endoplasmatiska retiklet, lysosomer och mitokondrier skapar rytmiska kalcium"oscillationer" som slår på viktiga gener för osteoklastbildning och fusion. Transportörer vid den skrynkliga randen och cellens motsatta sida förflyttar kalcium och fosfat bort från löst ben, antingen för att återanvändas i cellen eller för att återföras till blodomloppet. Andra metaller och mineraler — som mangan, magnesium, zink, koppar och järn — kontrolleras också av specialiserade transportörer och påverkar hur aggressivt osteoklaster resorberar ben. Till exempel kan järn och vissa former av celldöd kopplade till järn öka eller dämpa osteoklastaktivitet, medan zinktransportörer tenderar att begränsa överdriven benförlust.
Trafikledning inne i cellen
Jonkanaler är inte begränsade till det yttre membranet. Många sitter på interna kompartment som lysosomer, endosomer, Golgi‑apparaten och mitokondrier, vilket skapar ett flerskiktat transportnät. Dessa interna portar hjälper till att ställa in pH i matsmältningsvesiklar, driva energiproduktionen i mitokondrier och reglera förflyttning av enzymer och nedbrytningsprodukter. Översikten framhäver hur flera kanalsystem samarbetar: natrium–väte‑utbytare reglerar intern surhetsgrad, kalium–klorid‑kotransportörer hjälper till att bevara membranpotential och kloridbalans, och purinerga samt mekanosensitiva kanaler översätter kemiska eller mekaniska signaler till förändringar i bennedbrytning. Näringstransportörer för glukos, aminosyror, nukleosider och vitamin C stöder ytterligare de höga energetiska och biosyntetiska kraven hos aktivt resorberande osteoklaster.
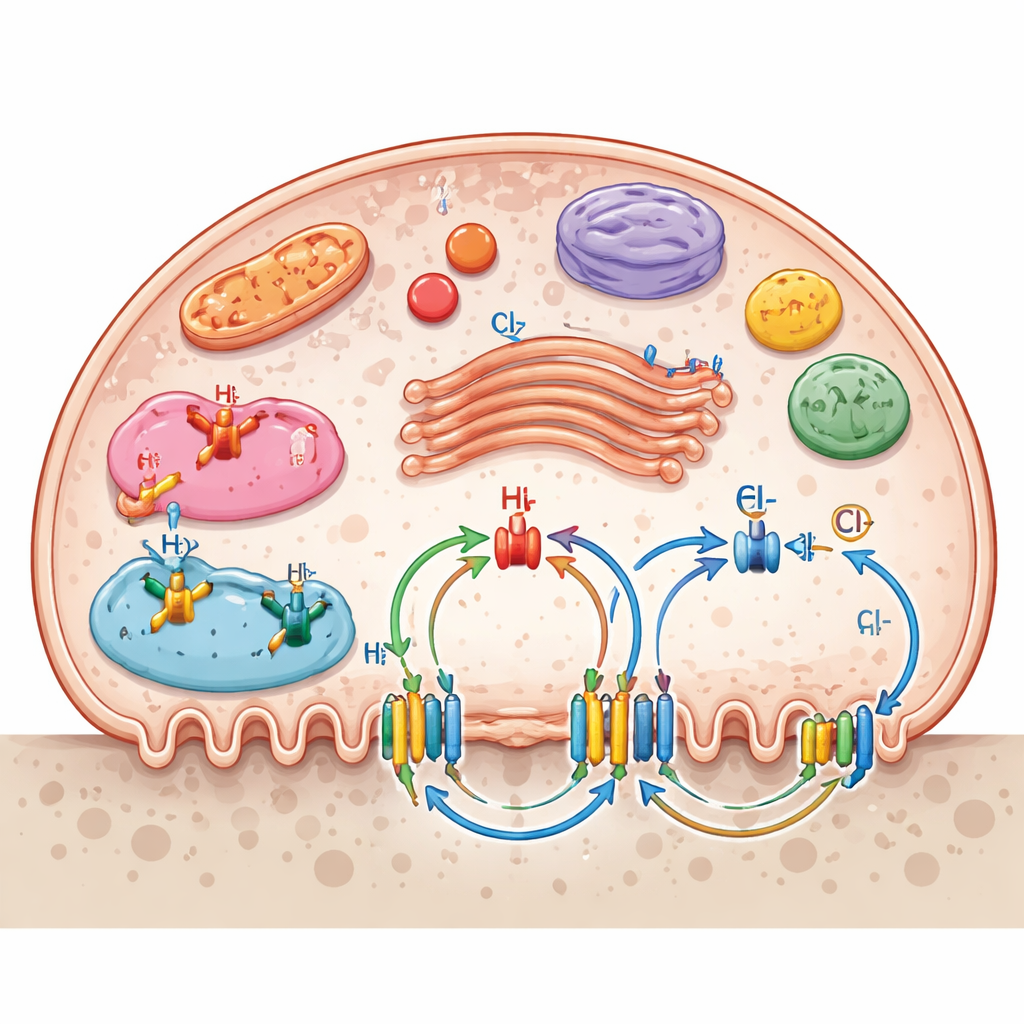
Från grundforskning till nya behandlingar
Eftersom så många bensjukdomar uppstår när osteoklaster är antingen överaktiva eller underaktiva är kanalerna och transportörerna som styr deras beteende attraktiva läkemedelsmål. Författarna går igenom befintliga och experimentella föreningar som blockerar V‑ATPaser, TRP‑kalciumkanaler, kloridutbytare, purinergiska receptorer och andra transportörer, samt nyare idéer som att störa specifika subenhetsinteraktioner eller använda riktade nanopartiklar för att leverera läkemedel direkt till ben. De poängterar att många av dessa proteiner också finns i andra vävnader, så att uppnå verklig osteoklast‑specificitet förblir en utmaning. Ändå, när genomiska och bildgivande verktyg avslöjar mer om var dessa kanaler sitter och hur de samverkar, kommer den expanderande "jonkartan" över osteoklaster sannolikt att ge mer precisa terapier för benskörhet, inflammatorisk bennedbrytning och sällsynta genetiska bensjukdomar.
Citering: Chen, H., Zhang, Y., Zhu, Y. et al. Spectrum and functions of ion channels and transporters in osteoclasts. Bone Res 14, 35 (2026). https://doi.org/10.1038/s41413-026-00513-9
Nyckelord: osteoklaster, jonkanaler, bennedbrytning, V-ATPase, benskörhet