Clear Sky Science · sv
TGF-β‑inducerad fibrotisk ärrbildning begränsar återhämtning efter ryggmärgsskada
Varför ärr i ryggmärgen spelar roll
När ryggmärgen skadas allvarligt lämnas många människor med bestående förlamning eller förlust av känsel eftersom skadade nervfibrer inte växer tillbaka. Denna studie ställer en enkel men avgörande fråga: vad är det exakt som blockerar denna återväxt — och kan vi säkert ta bort hindret? Genom att klarlägga hur en viss typ av ärr bildas inne i den skadade ryggmärgen pekar författarna på en ny väg för att hjälpa nervsystemet att reparera sig självt.
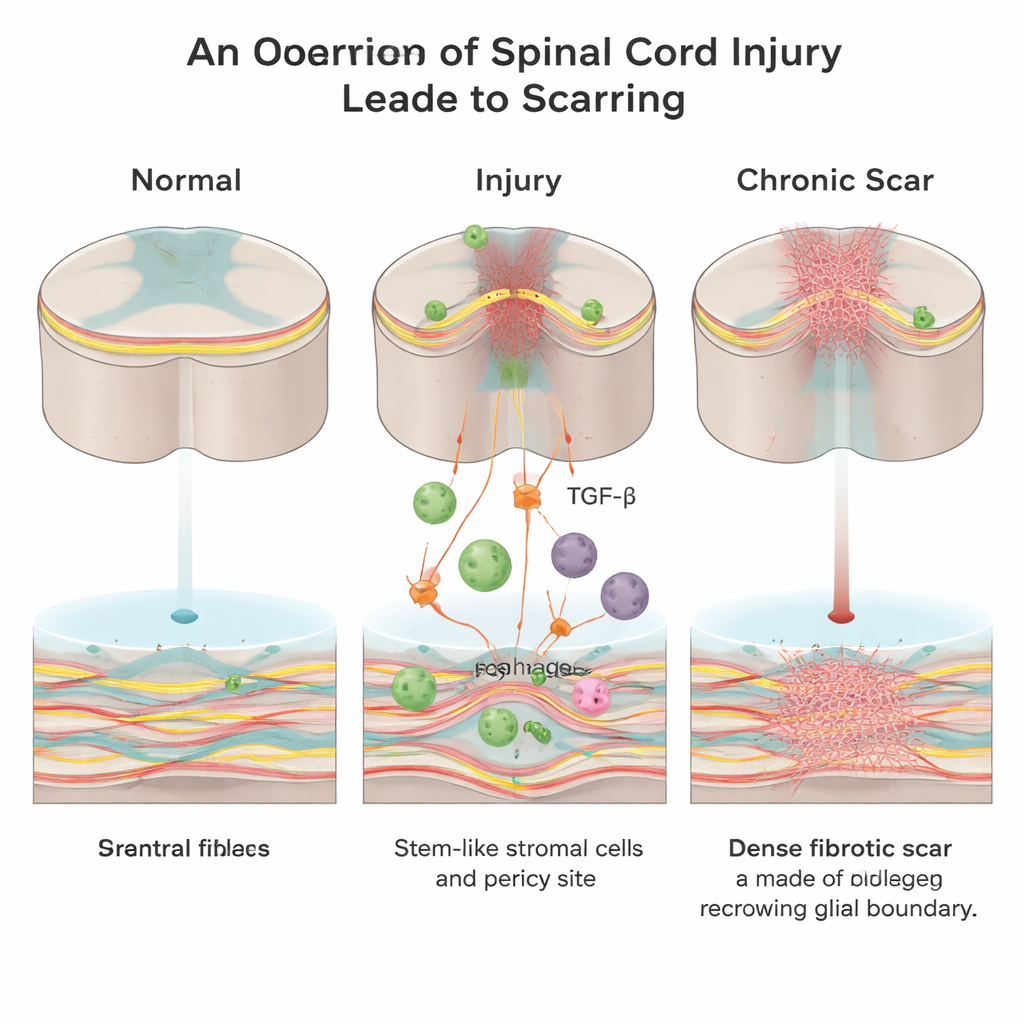
En dold mur inne i skadan
Efter en ryggmärgsskada skyndar kroppen för att täta såret. Två huvudsakliga typer av ärrvävnad bildas: ett ”gliärt” ärr som skapas av stödjeceller kallade astrocyter, och ett ”fibrotiskt” ärr rikt på kollagen, fibronektin och fibroblastceller. Medan det gliära ärret kan ha skyddande roller skapar det fibrotiska ärret en tät fysisk och kemisk barriär som växande nervfibrer inte lätt kan korsa. Fram till nu visste forskarna mycket mindre om hur denna fibrotiska kärna uppstår och vilka signaler som driver dess bildning.
Immuncellernas roll och en kraftfull signal
I studier på vuxna möss fokuserade forskarna på en signalsubstans kallad transformerande tillväxtfaktor‑beta (TGF‑β), som hjälper till att samordna sårläkning i hela kroppen och ofta är överaktiv vid fibrotiska sjukdomar. De fann att invaderande immunceller, så kallade makrofager, efter ryggmärgsskada blir en stor källa till aktiv TGF‑β1 vid skadans centrum. Denna ökning av TGF‑β1 rekryterar lokala mesenkymala stromala/stamceller och kärlassocierade celler kallade pericyter och driver dem att omvandlas till fibroblaster — de celler som avsätter det kollagenrika fibrotiska såret.
Dämpa signalen för att öppna en väg
För att testa om denna signalväg verkligen orsakar skadligt ärrbildande använde teamet flera genetiska knep hos möss. När de avlägsnade makrofager, eller tog bort TGF‑β1‑genen endast i makrofag‑linjens celler, minskade mängden fibrotisk vävnad i den skadade ryggmärgen kraftigt, och fler nervfibrer och serotoninhalterande banor kunde korsa skadzonen. På samma sätt minskade borttagning av TGF‑β‑receptorn specifikt i pericyter deras respons på TGF‑β, ledde till mindre kollagena ansamlingar och förbättrade rörelse‑ och känselprestationer i beteendetester. Viktigt är att pericyterna och relaterade stamliknande celler fortfarande fanns kvar men var mindre benägna att bli ärrbildande fibroblaster.
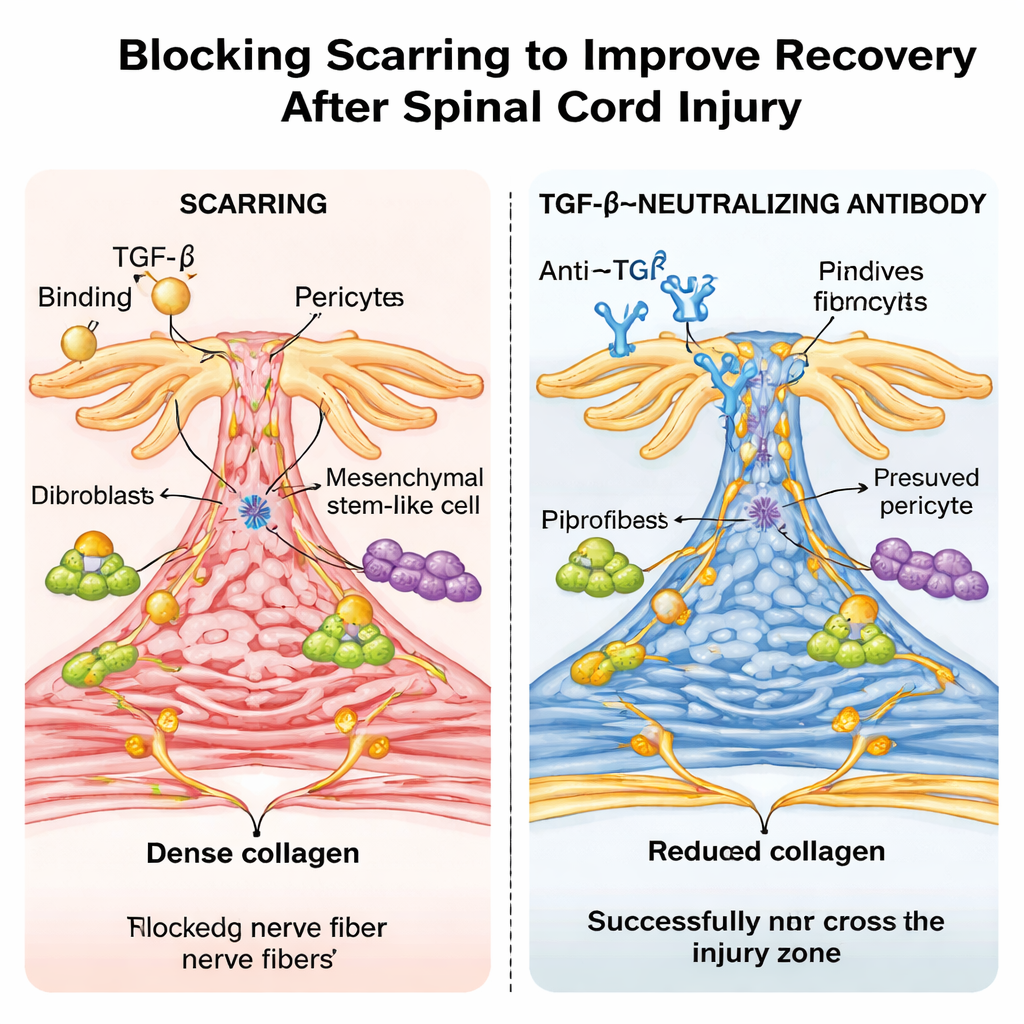
En läkemedelsliknande antikropp och en överraskande ålderseffekt
Forskarna prövade sedan ett mer kliniskt relevant tillvägagångssätt: de behandlade vanliga möss med en laboratorieantikropp som neutraliserar TGF‑β. Upprepade doser efter skada sänkte nivåerna av aktivt TGF‑β i blod och ryggmärg, krympte det fibrotiska ärret och gjorde det möjligt för nervfibrer att bättre överbrygga skadan, med påtagliga förbättringar i gång och sensorisk funktion. Enkelcells‑RNA‑sekvensering bekräftade att TGF‑β‑responsiva gener var mycket aktiva i ärrbildande celltyper hos obehandlade möss och dämpades av antikroppen. Slående nog, när samma typ av ryggmärgskross utfördes på nyfödda möss läkte djuren nästan utan fibrotisk ärrbildning, visade ingen mätbar TGF‑β‑aktivering vid skadans plats och återfick nära normal rörelse — vilket liknar den ärrfria reparation som ses hos vissa icke‑däggdjur.
Vad detta kan innebära för framtida behandling
Tillsammans tyder resultaten på att överdriven aktivering av TGF‑β efter ryggmärgsskada omdirigerar hjälpsamma reparationsceller till att bygga en rigid fibrotisk vägg som blockerar nervåterväxt och funktionell återhämtning. Genom att förhindra denna överaktivering — antingen genom att rikta in sig på TGF‑β‑produktionen i makrofager, blockera dess receptor på pericyter och stromala celler eller använda en neutraliserande antikropp — kan det bli möjligt att minska det skadliga ärret samtidigt som mer gynnsamma typer av vävnadsrespons bevaras eller till och med förbättras. Även om översättning av dessa strategier till människor kommer att kräva noggranna studier för att undvika biverkningar, lyfter arbetet fram TGF‑β‑driven fibrotisk ärrbildning som ett centralt och potentiellt läkemedelsbart hinder för ryggmärgsreparation.
Citering: Pan, D., Wu, P., Noller, K. et al. TGF-β-induced fibrotic scar formation limits recovery of spinal cord injury. Bone Res 14, 27 (2026). https://doi.org/10.1038/s41413-026-00507-7
Nyckelord: ryggmärgsskada, fibrotiskt ärr, TGF‑beta, makrofager, nervregenerering