Clear Sky Science · sv
HIF-1α och BMAL1 i benregenerering: korsprat mellan hypoxirespons och dygnsrytm
Varför brutna ben läker bättre än du tror
När vi bryter ett ben eller drar ut en tand startar kroppen tyst ett anmärkningsvärt välkoordinerat reparationsprojekt. Djupt inne i det skadade området sjunker syrenivåerna och vår inre dag–natt-klocka fortsätter att ticka. Den här artikeln utforskar hur två huvudbrytare—HIF‑1α, som känner av lågt syre, och BMAL1, ett kärnprotein i klockan—samarbetar för att styra benceller genom inflammation, ny vävnadstillväxt och slutlig återställning av styrka. Att förstå detta partnerskap kan förbättra behandlingar för frakturer, osteoporos, artrit och även tandimplantat.
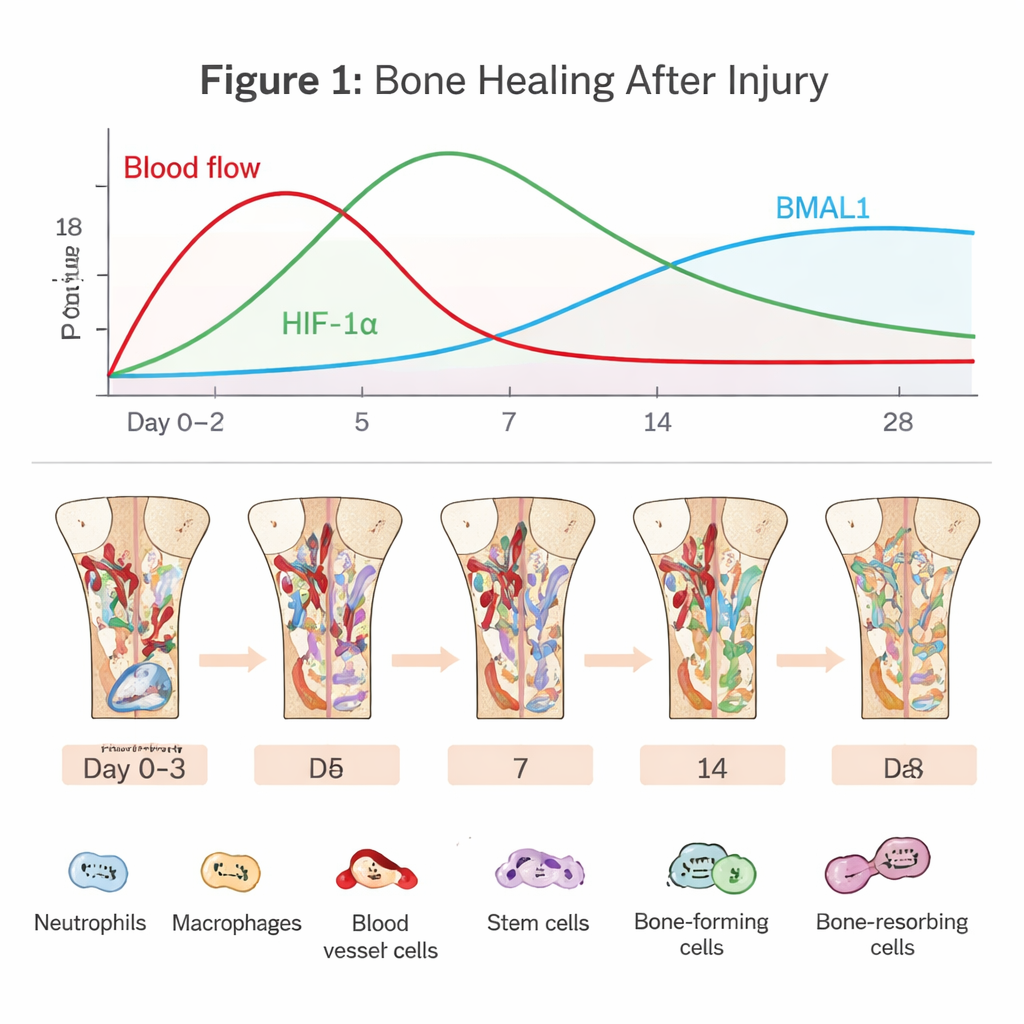
Den dolda dramatiken inne i ett läkande ben
Benregenerering börjar i samma ögonblick som blodkärl slits sönder. En blodpropp bildas, vilket avskärmar stora delar av syretillförseln och skapar en karg, lågsyremiljö. Immunceller som neutrofiler och makrofager skyndar till för att städa upp skräp och försvara mot mikrober. Samtidigt rekryteras stamceller från benmärgen och blodkärlsceller för att bygga upp området igen. Denna tidiga «inflammatoriska fas» är ett tveeggat svärd: en kort, väl avvägd inflammationspuls sätter igång reparationen, men om den pågår för länge eller blir för intensiv kan läkningen stanna av eller misslyckas. Artikeln understryker att navigeringen längs denna smala väg i hög grad beror på hur celler känner av syre och tid.
Hur celler använder lågt syre till sin fördel
I den syrefattiga frakturzonen stabiliseras proteinet HIF‑1α och slår på gener som hjälper cellerna att anpassa sig. Det driver endotelceller att skjuta ut nya blodkärl, vilket säkerställer att färskt syre och näring når defekten. Det omställar också cellernas metabolism mot glykolys, ett sätt att generera energi som fungerar även när syre är knapp. För stamceller och benbildande osteoblaster kan måttlig aktivering av HIF‑1α öka proliferation, migration och bentillväxt, delvis genom att öka faktorer som VEGF som kopplar blodkärlsbildning till ny benvävnad. Men om hypoxin är alltför svår eller långvarig byggs stressmolekyler och reaktiva syreföreningar upp, vilket skjuter osteoblaster mot celldöd och stimulerar bentärande osteoklaster. Samma hypoxisignal kan alltså antingen stödja eller sabotera läkningen, beroende på dess intensitet och längd.
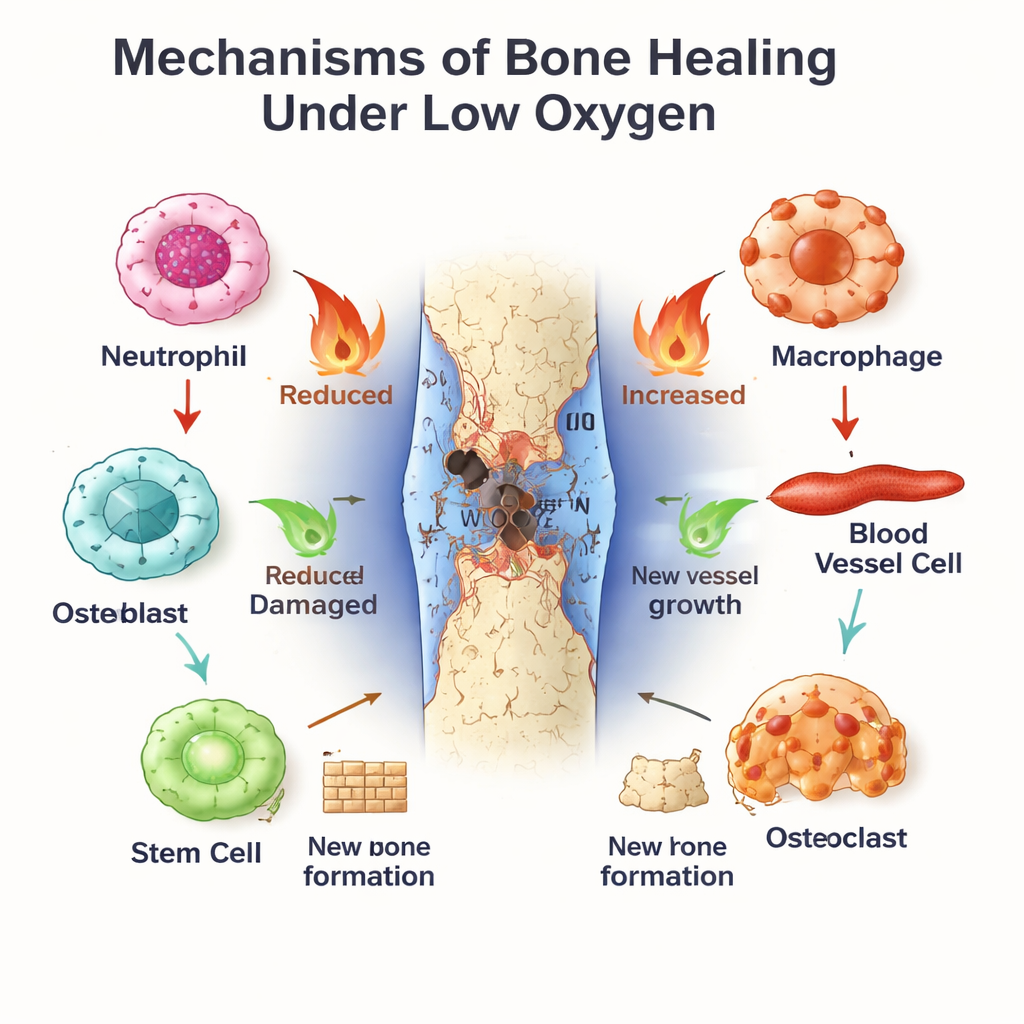
Kroppens inre klocka som chef för benreparation
Parallellt löper dygnsrytmen, en molekylär tidsgivare som finns i nästan varje cell. BMAL1, en av dess centrala komponenter, hjälper till att sätta dagliga rytmer i immunaktivitet, blodkärlsbeteende och stamcellsdifferentiation. Neutrofiler och makrofager visar tid på dygnet‑skillnader i hur kraftigt de svarar på skada och hur snabbt de åldras eller växlar från inflammatoriska (M1‑lika) till läkande (M2‑lika) tillstånd. I blodkärlsceller och benmärgsstamceller främjar BMAL1 hälsosam proliferation och ordnad bentillväxt, delvis genom att finjustera tillväxtsignaler som Wnt och TGF‑β/SMAD. När BMAL1 rubbas—genom gendefekter, skiftarbete eller metabol sjukdom—tenderar benen att förlora massa, stamceller blir utmattade och balansen mellan benbildning och nedbrytning förskjuts mot förlust.
En konversation mellan syresensorik och kroppsklockan
Hjärtat i översikten är den framväxande «korspraten» mellan HIF‑1α och BMAL1. Dessa två proteiner har liknande strukturer och kan interagera fysiskt, till och med bilda blandade par som binder DNA och kontrollerar överlappande genuppsättningar. Var och en kan påverka den andra gällande produktion och stabilitet, vilket skapar återkopplingsslingor som knyter dygnsrytmen till hur celler svarar på hypoxi. Tillsammans reglerar de också cellernas redoxbalans—hur mycket skadliga reaktiva syreföreningar som bildas kontra hur stor antioxidantkapacitet som finns—och de samreglerar nyckelenzymer som avgör om celler förlitar sig mer på syreberoende andning eller på syrefri glykolys. Denna gemensamma kontroll hjälper avgöra om frakturmiljön gynnar konstruktiv återuppbyggnad eller överdriven inflammation och bennedbrytning.
Vad detta betyder för sjukdom och behandling
Samma HIF‑1α–BMAL1‑partnerskap syns i många benrelaterade tillstånd. Hos skiftarbetare kan rubbade sömn‑ och ljusförhållanden sannolikt förändra BMAL1, öka oxidativ stress och störa HIF‑1α‑styrd reparation, vilket bidrar till osteoporos. Vid diabetes försvagar högt blodsocker både klockfunktionen och hypoxisignaleringen, vilket undergräver blodkärlsbildning och stamcellsdriven bentillväxt. Vid artros stör förlust av BMAL1 i broskceller deras rytm och deras skyddande samspel med HIF‑1α, vilket påskyndar brosknedbrytning. Runt titanimplantat verkar kontrollerad hypoxi och en frisk dygnsrytm stödja bättre osseointegration, vilket antyder att framtida implantatytor kan utformas för att försiktigt aktivera både HIF‑1α och BMAL1. Sammanfattningsvis drar artikeln slutsatsen att framgångsrik benregenerering inte bara beror på vilka celler som finns närvarande, utan på hur de tolkar syre och tid—och att rikta in sig på denna dialog kan öppna nya vägar till snabbare, starkare läkning.
Citering: Weng, Y., Xiong, J., Zhao, Q. et al. HIF-1α and BMAL1 in bone regeneration: crosstalk between hypoxia response and circadian rhythm. Bone Res 14, 25 (2026). https://doi.org/10.1038/s41413-026-00506-8
Nyckelord: benregenerering, dygnsrytm, hypoxi, osteoporos, frakturläkning