Clear Sky Science · sv
Synovialt inflammatoriska makrofag‑härledda extracellulära vesiklar förvärrar broskskador på ett FMRP‑selektivt sorterat sätt vid osteoartrit
Varför ledinflammation spelar roll för värkande knän
Många ser osteoartrit som enkel ”slitage” i åldrande leder, men växande bevis visar att låggradig inflammation inne i leden tyst kan driva sjukdomen framåt. Denna studie ställer en konkret fråga: hur kommunicerar immunceller i ledens hinna med broskceller, och kan den dialogen avbrytas för att skydda lederna? Svaren avslöjar ett litet molekylärt kurirsystem som förvärrar skadan — men som också erbjuder nya möjligheter för diagnos och behandling av osteoartrit.
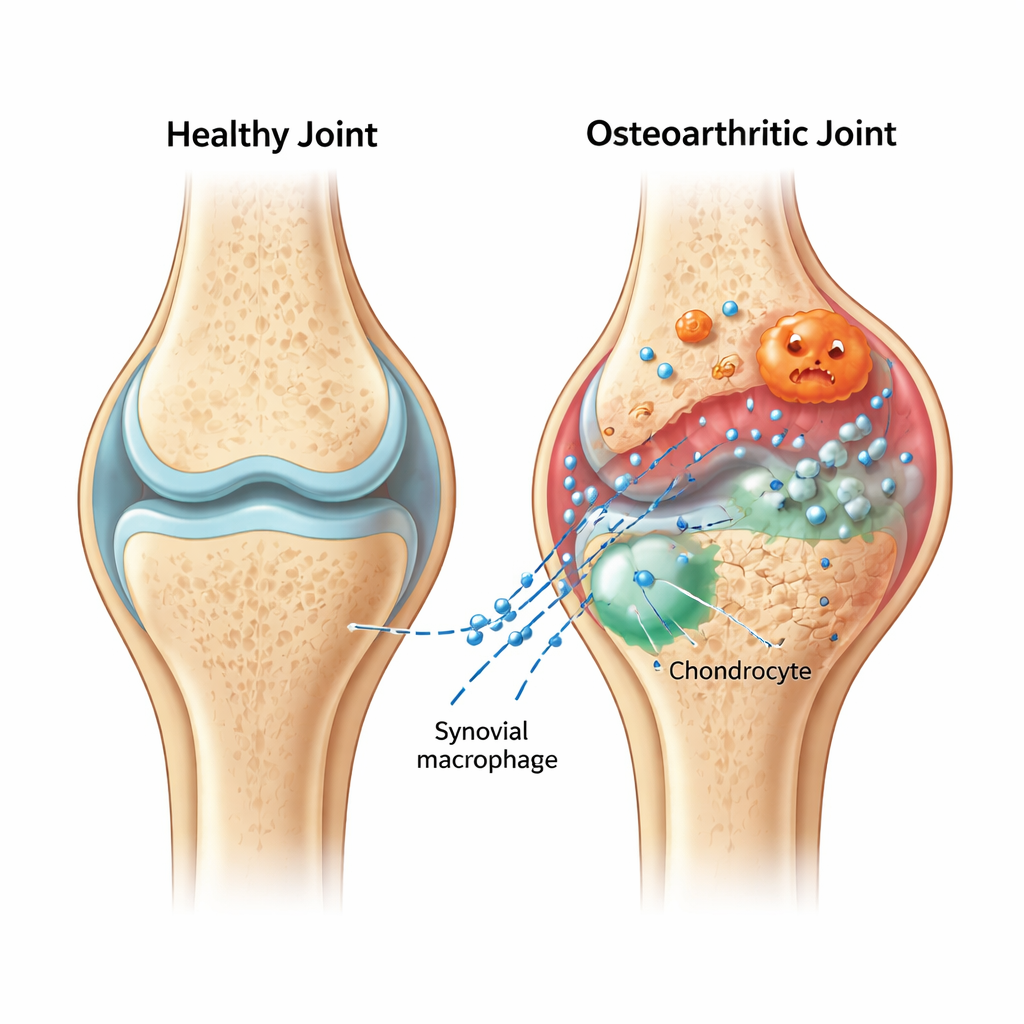
Små paket som för med sig dåliga nyheter
I ett artritiskt knä blir den mjuka synoviala hinnan inflammerad och full av immunceller kallade makrofager. Författarna fokuserade på den ”hetlevrade” varianten av dessa celler — proinflammatoriska makrofager — och de mikroskopiska blåsor de släpper, kända som extracellulära vesiklar. Dessa vesiklar fungerar som förseglade paket som för molekyler mellan celler. Hos råttor med kirurgiskt inducerad osteoartrit visade teamet att vesiklar från inflammerade makrofager når brosket och förvärrar skadan: den normalt släta, stötdämpande ytan blev grövre och tunnare, viktiga broskproteiner minskade medan nedbrytande enzymer ökade.
Hur inflammation stänger av broskets självstädning
Broskceller, eller kondrocyter, förlitar sig på en städprocess kallad autofagi för att återvinna utslitna komponenter och hålla sig friska över livet. När forskarna jämförde vilka gener som aktiverades i brosk exponerat för inflammatoriska vesiklar kontra en ofarlig saltlösning såg de tydliga tecken på att autofagi‑vägarna undertrycktes. I elektronmikroskopet innehöll brosk från vesikelbehandlade leder betydligt färre av de karakteristiska återvinningsvesiklarna. I cellkulturer bildade kondrocyter som exponerades för makrofagvesiklar också färre autofagosomer och autolysosomer, vilket bekräftar att deras självstädningsmaskineri stängdes av samtidigt som skadan ansamlades.
En enda microRNA vänder en kritisk brytare
Vid en närmare granskning undersökte teamet de små RNA‑regulatorerna packade i makrofagvesiklarna. En molekyl, miR‑155‑5p, stack ut: den var berikad i vesiklar från osteoartritiska djur och i mänsklig osteoartritvävnad, särskilt i synovium. Experiment visade att vesikellevererad miR‑155‑5p går in i kondrocyter och direkt riktar in sig på ett protein kallat GSK‑3β, som normalt hjälper till att hålla en tillväxtreglerande väg, mTORC1, i schack. När GSK‑3β undertrycks blir mTORC1 överaktivt och autofagin minskar, vilket gör broskceller mindre kapabla att hantera stress. Att blockera miR‑155‑5p med en designad ”antagomiR” hos råttor återställde autofagin, bevarade broskstrukturen och minskade tecken på osteoartrit, medan möss som genetiskt saknade miR‑155 i sina makrofager utvecklade mildare sjukdom och mindre synovit.
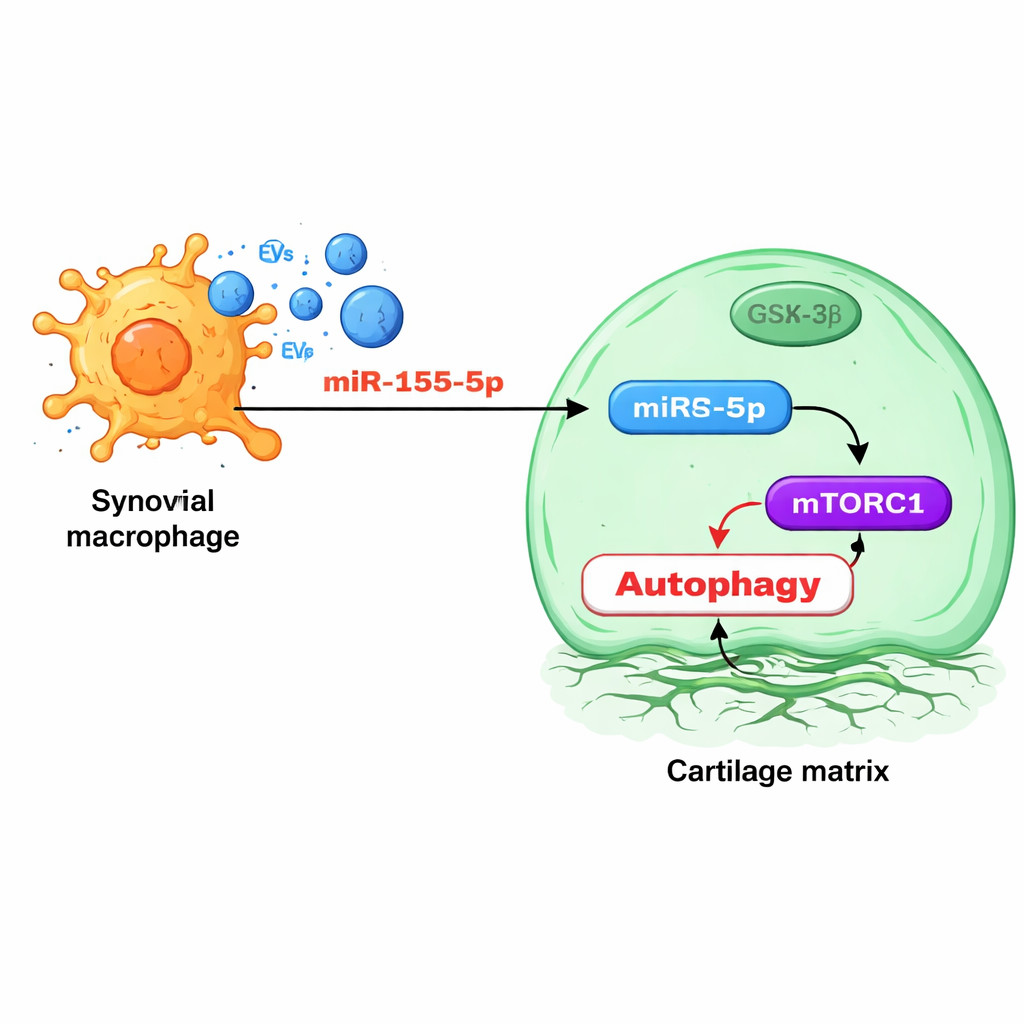
Sortering och riktning av den skadliga signalen
Intressant nog fann studien att makrofager använder ett specifikt RNA‑bindande protein, FMRP, för selektivt lasta miR‑155‑5p i vesiklar. När FMRP‑nivåerna ökade bar vesiklarna mer miR‑155‑5p och skadade broskceller i större utsträckning; när FMRP minskades blev vesiklarna mindre toxiska och kondrocyternas autofagi återhämtade sig. Nivåerna av FMRP i vesiklar cirkulerande i blodet ökade i takt med osteoartritprogression hos både råttor och mänskliga patienter, vilket tyder på att detta protein, eller vesiklarna som bär det, skulle kunna fungera som en blodbaserad markör för sjukdomsaktivitet utan behov av bilddiagnostik eller invasiva ingrepp.
En cellfri terapi som hittar rätt celler
Byggt på dessa mekanistiska insikter konstruerade forskarna en potentiell terapi med vesiklar från adipose‑deriverade stromaceller, en typ av stamliknande celler i fettväv. De dekorerade dessa vesiklar med en liten peptid som fungerar som en målsökaranordning för proinflammatoriska makrofager, och lastade dem med antagomiR‑155‑5p. Hos osteoartritiska råttor minskade upprepade injektioner av dessa riktade vesiklar synovial inflammation, förskjöt makrofager mot ett mer ”läkande” tillstånd, sänkte miR‑155‑5p‑nivåerna i leden, återställde GSK‑3β och förbättrade broskets struktur och sammansättning mer tydligt än oriktade vesiklar. När de applicerades på mänskliga synoviala vävnadsprover i laboratoriet minskade de konstruerade vesiklarna också inflammatoriska markörer och ökade antiinflammatoriska signaler.
Vad detta betyder för personer med osteoartrit
Detta arbete omformulerar osteoartrit som en sjukdom som drivs inte bara av mekaniskt slitage, utan av en molekylär dialog mellan inflammerade ledhinnorceller och brosk. Proinflammatoriska makrofager skickar ut vesiklar lastade med miR‑155‑5p, vilket dämpar broskcells självreparationssystem via GSK‑3β/mTORC1‑vägen och påskyndar vävnadsnedbrytning. Genom att blockera denna signal — antingen genetiskt eller med riktade terapeutiska vesiklar — kunde forskarna dämpa både inflammation och broskskada i djurmodeller och mänsklig vävnad. Även om mycket arbete återstår innan sådana strategier når kliniken, lyfter studien fram nya möjligheter: blodtester baserade på vesikelinnehåll för att följa sjukdomen, och precisa, cellfria behandlingar som lugnar skadlig inflammation samtidigt som brosket får bättre förutsättningar att skydda sig.
Citering: Zhao, S., Wang, J., Xue, M. et al. Synovial inflammatory macrophage-derived extracellular vesicles exacerbate cartilage lesions with a FMRP-selectively sorted manner in osteoarthritis. Bone Res 14, 26 (2026). https://doi.org/10.1038/s41413-025-00502-4
Nyckelord: osteoartrit, extracellulära vesiklar, makrofager, brosk, microRNA-155