Clear Sky Science · sv
MicroRNA-132/212 modulerar negativt opiatbelöning genom att rikta in sig på dopamintransportören i ventrala tegmentala området
Varför denna forskning är viktig i vardagen
Opioida smärtstillande medel och närbesläktade droger kan ge lindring men innebär också en allvarlig risk för beroende. Denna studie undersöker belöningssystemet i hjärnan för att identifiera små genetiska reglage som påverkar hur starkt opioider upplevs som belönande. Genom att förstå dessa reglage hoppas forskare kunna utforma smartare behandlingar som lindrar smärta eller minskar beroende utan att kapra hjärnans nöjeskretsar.
Små molekyler med stort inflytande
Våra hjärnor förlitar sig på ett ämne kallat dopamin för att signalera nöje och motivera oss att söka belönande upplevelser, från god mat till beroendeframkallande droger. Styrkan och varaktigheten i denna signal kontrolleras delvis av ett protein kallat dopamintransportören, som fungerar som en dammsugare och återupptar dopamin i nervcellerna. Författarna fokuserade på två mycket små genetiska komponenter, microRNA-132 och microRNA-212, som kan skruva ner produktionen av specifika proteiner. Tidigare arbete kopplade dessa microRNA till kokainanvändning och stress. Här frågade teamet om de också påverkar hur hjärnan svarar på opioider, särskilt morfin.
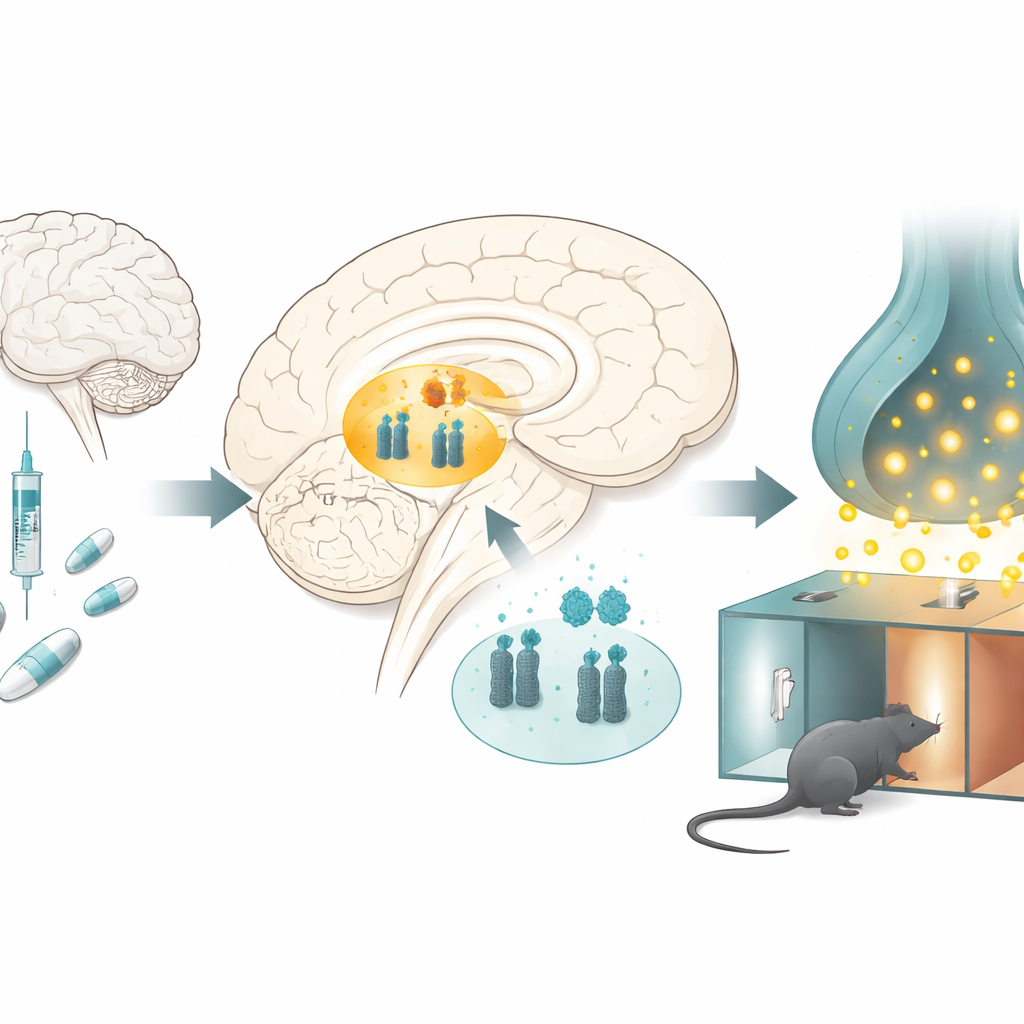
Hur opioider förändrar hjärnans belöningscentrum
Forskarnas studier på råttor som fick upprepade doser morfin i ett klassiskt test för drogbelöning — där djuren får lära sig att föredra ett rum kopplat till drogen — visade att de morfinbehandlade djuren efter några dagar tillbringade mer tid i det morfinparade kammaren, vilket visar att läkemedlet blivit belönande. När forskarna undersökte en nyckelregion för belöning djupt i hjärnan, ventrala tegmentala området, fann de ett påfallande mönster: nivåerna av microRNA-132 och microRNA-212 var minskade, medan nivåerna av dopamintransportören ökade. Liknande förändringar observerades när råttor fick morfin utan inlärningsuppgiften, vilket tyder på att kronisk dropexponering i sig förskjuter denna molekylära balans.
Att peka ut en direkt molekylär koppling
För att avgöra om dessa microRNA verkligen styr dopamintransportören vände sig teamet till humana nervliknande celler i laboratoriet. Genom att artificiellt öka mängden microRNA-132 eller microRNA-212 såg de en minskning både av budbärar-RNA och av proteinet för transportören. Blockering av microRNA gav motsatt effekt. De konstruerade sedan en rapportör där ett ljusproducerande enzym kopplades till transportörens reglerande svans. Tillsättning av microRNA dämpade ljussignalen, men denna effekt försvann när ett par viktiga baser i bindningsstället muterades. Tillsammans visade dessa experiment att microRNA-132 och microRNA-212 direkt binder till transportörens budskap och undertrycker dess produktion.
Från molekyler till dopaminnivåer och beteende
Nästa fråga var hur denna molekylära kontroll agerar i levande hjärnceller. I odlade nervceller minskade en ökning av microRNA upptaget av dopamin, medan blockering förstärkte dopaminrensningen. När forskarna artificiellt ökade eller minskade nivåerna av dopamintransportören steg eller sjönk microRNAernas effekt i enlighet med detta, vilket bekräftade att transportören är huvudmedlaren. I levande råttor ökade en förstärkning av microRNA-132 i ventrala tegmentala området dopaminnivåerna som spillde över till anslutna regioner, vilket speglar svagare transportöraktivitet. Beteendemässigt gjorde användning av virala verktyg för att suga upp ("svamp") microRNA-132 eller microRNA-212 i denna hjärnregion att råttor utvecklade en starkare preferens för morfin, tillsammans med högre transportörnivåer. Omvänt sänkte tvingad ökning av microRNA-132 i samma område transportörnivåerna och dämpade morfinpreferensen hos hankön, honkön och unga djur, utan att påverka rörelse eller njutning av naturliga belöningar som sockervatten.
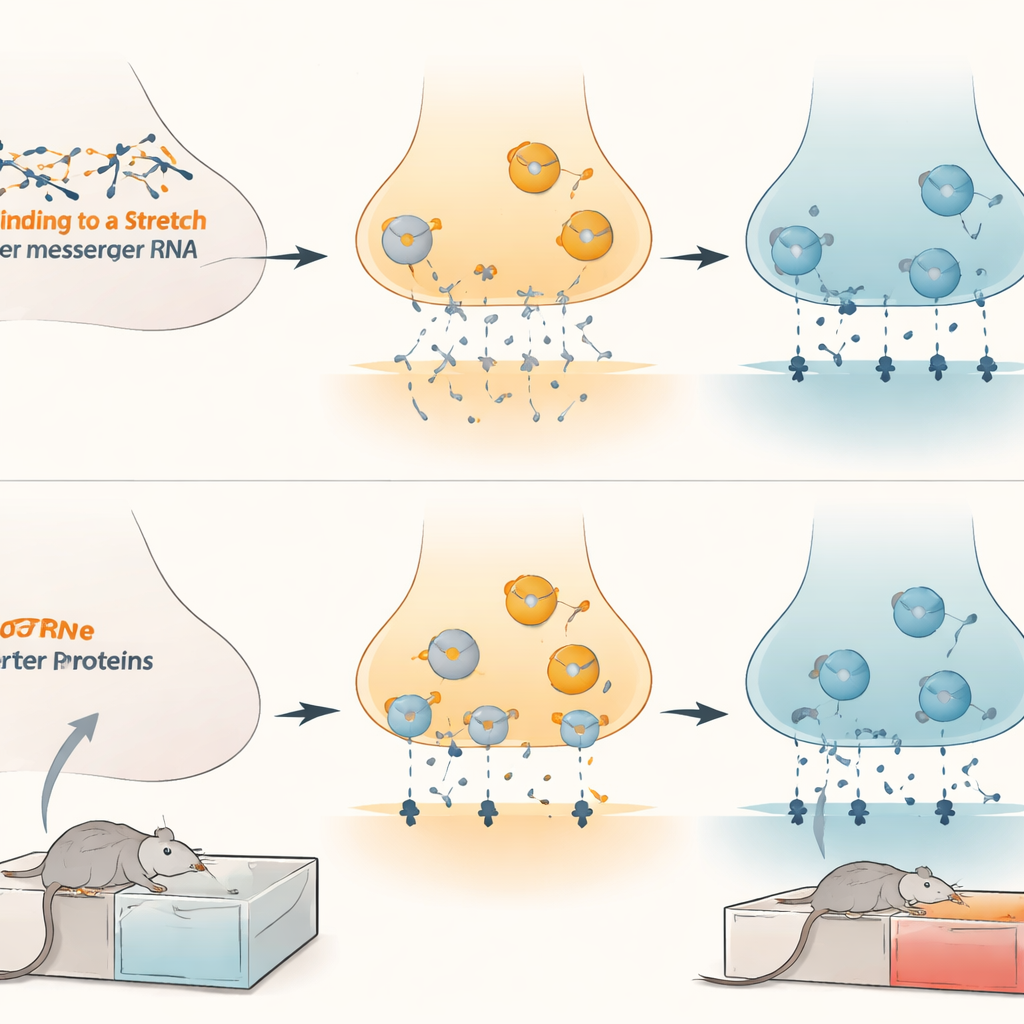
Implikationer för behandling av opioidberoende
Dessa fynd avslöjar ett finjusterat bromssystem inom hjärnans belöningskretsar: microRNA-132 och microRNA-212 håller dopamintransportören i schack och formar hur kraftfullt opioider upplevs som belönande. Kroniskt morfin verkar lyfta denna broms genom att sänka nivåerna av microRNA, vilket tillåter transportörnivåerna att stiga och bidrar till att befästa drogrelaterade belöningssignaler. Genom att återställa eller efterlikna dessa microRNA:s verkan specifikt i ventrala tegmentala området kan det bli möjligt att mildra opioiders grepp utan att allmänt dämpa nöje eller rörelse. Mycket arbete återstår innan sådana strategier kan testas på människor, men studien pekar på en ny, mycket riktad väg för framtida behandlingar som angriper beroende på hjärnans egna molekylära reglage.
Citering: Meng, J., Li, Z., Zhang, Y. et al. MicroRNA-132/212 negatively modulates opioid reward by targeting dopamine transporter in the ventral tegmental area. Transl Psychiatry 16, 152 (2026). https://doi.org/10.1038/s41398-026-03915-9
Nyckelord: opioidberoende, dopamintransportör, microRNA-132, ventrala tegmentala området, morfinbelöning