Clear Sky Science · sv
Låga koncentrationer av amyloid‑beta‑oligomerer inducerar synaptogenes som kännetecknar mild kognitiv svikt och förändrar den de novo‑proteomen
Tidiga förändringar som kan signalera minnesproblem
Innan Alzheimers sjukdom berövar människor på minnet passerar hjärnan ett dimmigt mellanläge som kallas mild kognitiv svikt. I detta skede är tankefunktioner påtagligt påverkade, men vardagslivet fortsätter ofta som vanligt. Märkligt nog visar vissa hjärnregioner i detta skede fler, inte färre, förbindelser mellan nervceller. Denna studie undersöker om små mängder av en toxisk molekyl kopplad till Alzheimer kan driva denna våg av nya förbindelser, och om ett läkemedel som redan testats på cancerpatienter kan dämpa dessa mycket tidiga förändringar.
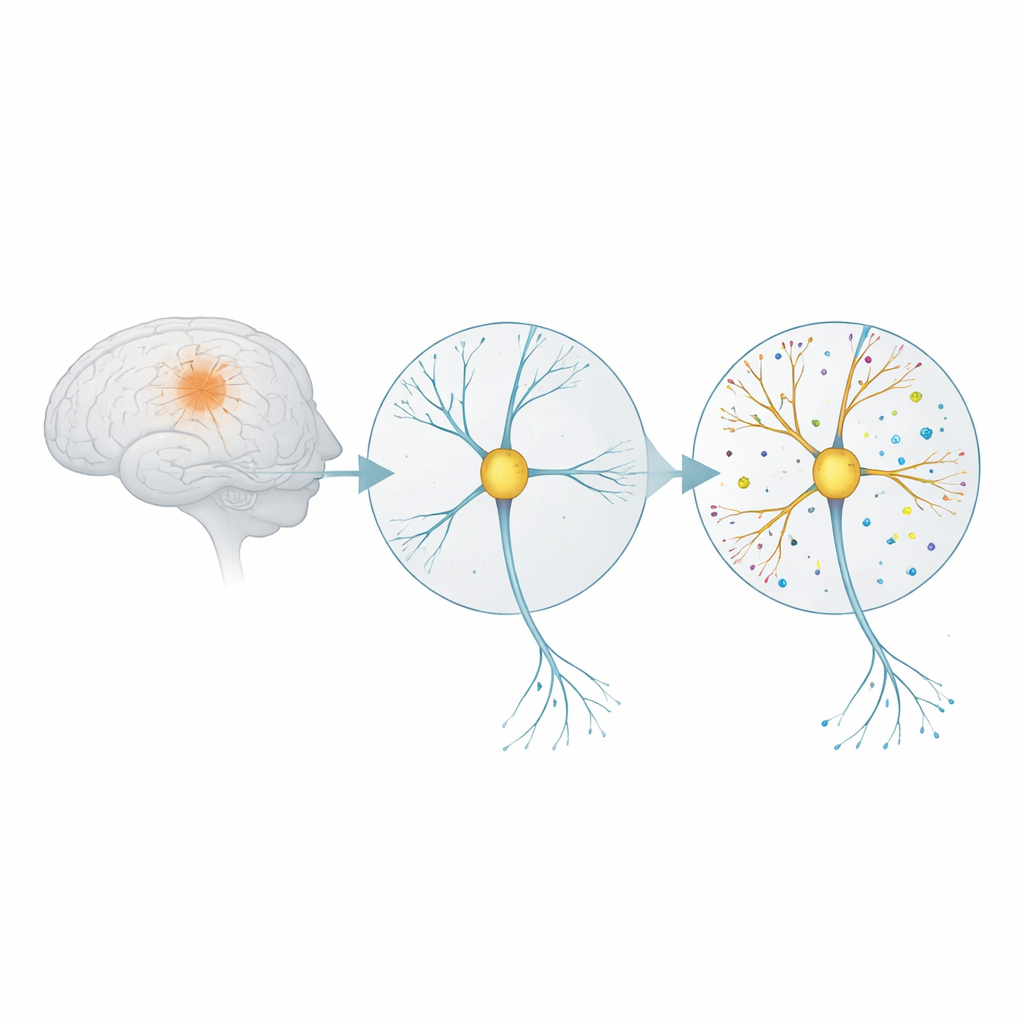
Hur hjärnförbindelser reagerar på en toxisk utlösare
Alzheimers sjukdom är nära kopplad till små ansamlingar av ett proteinfragment som kallas amyloid‑beta. I sin oligomerform är detta fragment särskilt skadligt för synapser—kontaktpunkterna där nervceller kommunicerar med varandra. Forskarna odlade råtthjärnceller i en skål tills de bildade mogna nätverk, och exponerade dem sedan i fem dagar för en låg dos amyloid‑beta‑oligomerer. De testade också vad som hände när de tillsatte en förening kallad eFT508, som blockerar ett signaleringsenzym (MNK) involverat i initiering av proteinsyntes inne i cellerna. Denna uppställning var avsedd att efterlikna mycket tidiga sjukdomsstadier, innan utbredd celldöd inträffar.
Att se dolda detaljer i nya synapser
För att undersöka hur förbindelserna förändrades använde teamet ”expansionsmikroskopi”, en teknik som fysikaliskt sväller bevarade celler i en mjuk gel så att små strukturer kan ses i mycket större detalj. De märkte nervtrådar och båda sidor av synapsen med fluorescerande taggar och rekonstruerade dem i 3D. Exponering för amyloid‑beta orsakade en tydlig ökning av antalet synapser längs nervcellernas grenar. Särskilt fanns fler enkla boutons—enkla en‑till‑en‑kontakter—och ovanliga ”multi‑innervated spines”, där mer än en ingående fiber konvergerar på en enda mottagande punkt. Dessa mönster liknar de synaptiska ökningar som rapporterats hos personer med mild kognitiv svikt. När eFT508 var närvarande sjönk synapsantalen tillbaka mot normala nivåer, vilket tyder på att läkemedlet kan motverka denna tidiga överväxt.
Nya proteiner förändras, även när totalmängden inte gör det
Synapser omformas ständigt genom att proteiner byggs upp och bryts ner. Teamet tittade därefter på vilka proteiner som nyproducerades under och efter exponering för amyloid‑beta. De gav neuronerna en ofarlig konstgjord aminosyra som byggs in i färska proteiner, och använde sedan kemiska ”click”‑reaktioner och masspektrometri för att plocka ut och identifiera dessa molekyler. Överraskande nog förändrades inte den totala mängden nyproducerat protein efter flera dagars lågdos‑amyloid‑beta, varken med eller utan eFT508. Men när de granskade vilka specifika proteiner som producerades var bilden en helt annan: över tusen nyproducerade proteiner upptäcktes, och många av dem ökade eller minskade som svar på amyloid‑beta. Många var involverade i synaptisk kommunikation, cellens interna skelettverk, energiproducerande mitokondrier, avfallshanteringssystem och proteinsorterings‑/kvalitetskontrollmekanismer.
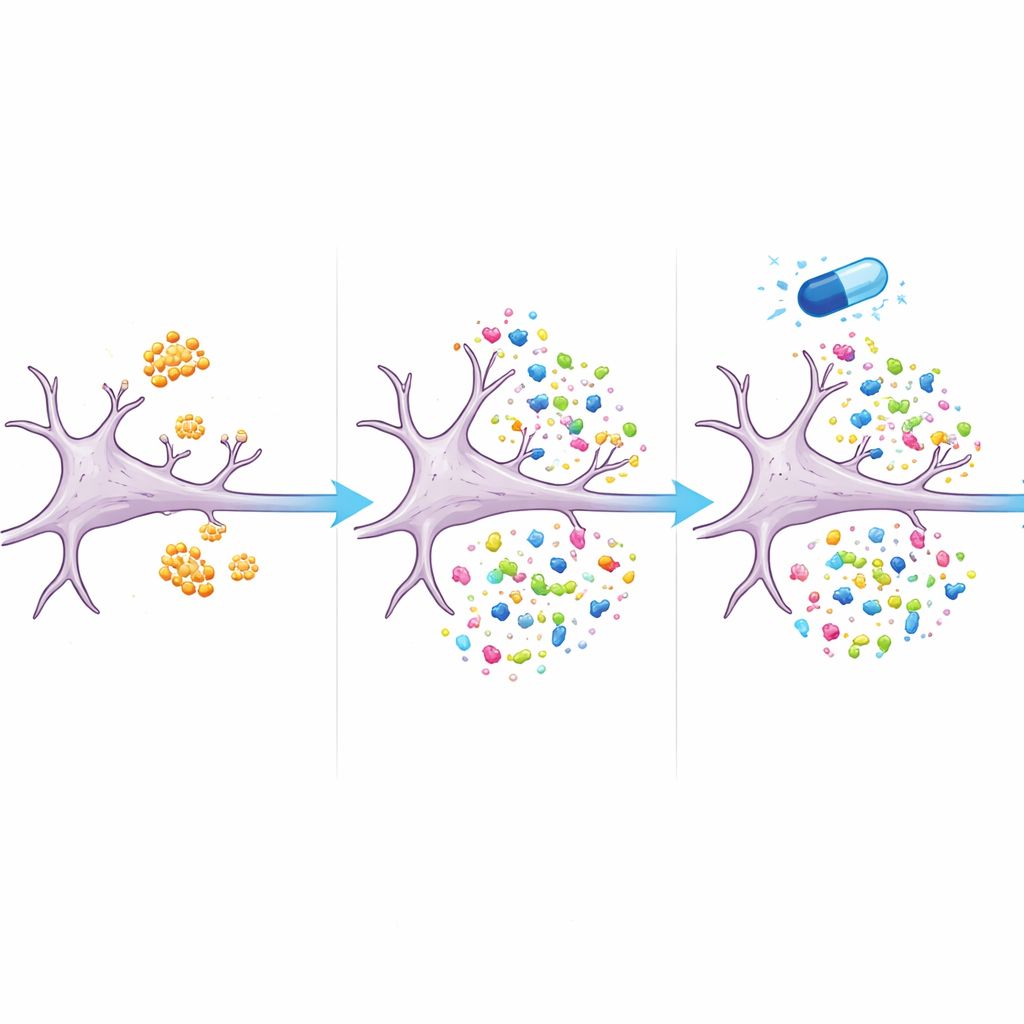
Ett läkemedel som styr proteinbalansen
Avgörande är att många av de rubbade proteinerna återgick mot normala nivåer när cellerna behandlades med eFT508 tillsammans med amyloid‑beta. Mer än två tredjedelar av de proteiner som påverkades av amyloid‑beta ensam var inte längre signifikant olika från obehandlade celler när läkemedlet var närvarande. Dessa inkluderade proteiner kopplade till synapsstruktur och -funktion, liksom komponenter i cellens återvinnings‑ och energisystem. Resultaten tyder på att eFT508 inte helt enkelt släcker proteinsyntesen; istället tycks det omforma vilka proteiner som tillverkas och styra systemet bort från ett Alzheimer‑liknande mönster och mot en hälsosammare balans.
Vad detta kan innebära för framtida behandling
Detta arbete målar upp en bild av tidig Alzheimer‑relaterad skada som ett stadium av överförbindelse och subtilt proteinmisskötsel snarare än ren förlust. Låga nivåer av amyloid‑beta driver bildandet av extra, ibland ovanliga synapser och förvränger selektivt blandningen av proteiner som nervcellerna tillverkar. I denna skålbaserade modell kan eFT508 både normalisera synapsantal och korrigera många av proteinförändringarna, vilket antyder att en noggrann justering av proteinsyntesen kan bromsa eller förhindra övergången från mild kognitiv svikt till fullskalig demens. Även om mycket återstår att testa i levande djur och människor framhäver studien ett nytt sätt att tänka kring—och kanske ingripa i—de allra tidigaste stadierna av Alzheimers sjukdom.
Citering: Wu, K., Lee, S., Martinez-Serra, R. et al. Low concentrations of amyloid-beta oligomers induce synaptogenesis characteristic for mild cognitive impairment and alter the de novo proteome. Transl Psychiatry 16, 132 (2026). https://doi.org/10.1038/s41398-026-03905-x
Nyckelord: Alzheimers sjukdom, synapsförändringar, amyloid beta‑oligomerer, proteinsyntes, tidig neurodegeneration