Clear Sky Science · sv
METTL3-medierad m6A-modifiering reglerar CDKN1A för att dämpa kronisk sömndeprivation-inducerad kognitiv försämring och neuronal apoptos hos råttor
Varför sömnlösa nätter kan skada ditt minne
Många avfärdar kronisk sömnbrist som en normal del av det moderna livet, men vetenskapen visar att förlorad sömn tyst kan skada de hjärnregioner som stöder lärande och minne. Denna studie på råttor går ner till nivån av enskilda molekyler i hippocampala neuroner och identifierar en specifik kemisk växel — kallad METTL3 — som verkar skydda hjärnceller från de skadliga effekterna av kronisk sömnbrist. Att förstå denna växel skulle i förlängningen kunna peka mot nya sätt att skydda minnet hos människor som har svårt att undvika sömnförlust, såsom skiftarbetare, vårdgivare och patienter med sömnstörningar.
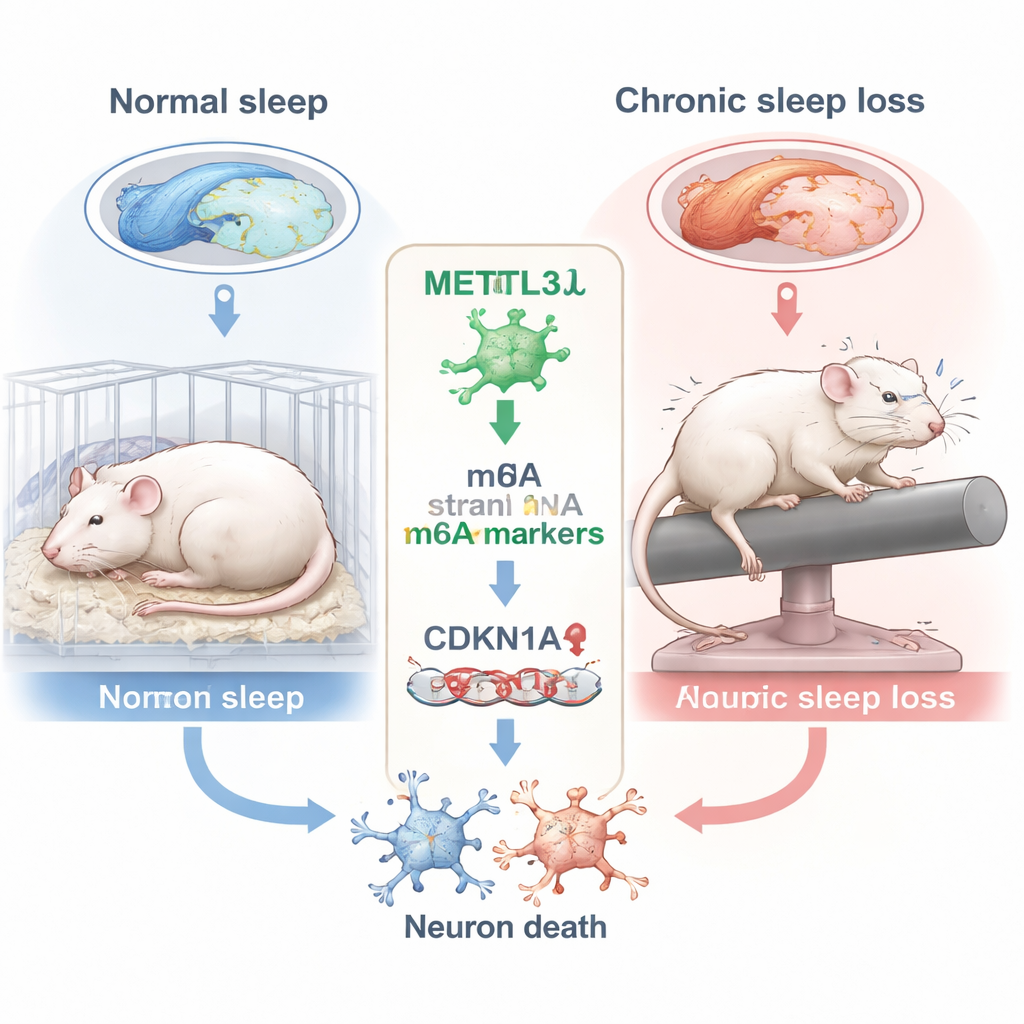
Hur långvarig sömnbrist skadar minnescentret
Forskarnas fokus låg på hippocampus, en sjöhästsformad hjärnregion som är avgörande för att bilda nya minnen. Inom hippocampus zoomade de in på en subregion kallad CA3, som hjälper till att koda och återkalla spatial information — färdigheter som testas med uppgifter som att hitta en dold plattform i vatten. Råttorna hölls vakna i 10 timmar per dag under sex veckor med hjälp av en mjuk roterande stång som upprepade gånger väckte dem. När deras minne testades i den välkända Morris Water Maze tog sömnbristiga råttor mindre direkta vägar, korsade den tidigare plattformens plats färre gånger och tillbringade mindre tid i målkvadranten — alla tecken på nedsatt spatialt minne jämfört med välvilade djur.
En kemisk markering på RNA som försvinner
För att förstå vad som hände inne i CA3-neuronerna analyserade teamet en kemisk etikett på RNA kallad m6A, en av de vanligaste interna markeringarna på budbärar-RNA. Dessa etiketter hjälper till att kontrollera hur länge RNA-molekyler kvarstår och hur effektivt de används för att tillverka proteiner. Ett nyckelenzym som lägger till m6A-markeringar är METTL3. Med hjälp av höggenomströmmande m6A-sekvensering och genuttrycksanalys fann forskarna att kronisk sömndeprivation signifikant minskade METTL3 i CA3-regionen. Denna nedgång bekräftades både på RNA- och proteinnivå. Mönstret av påverkade gener föreslog störningar i kontrollen av cellcykeln och stressrespons, vilket antyder att sömnbrist kan driva neuroner mot ohälsosamma tillstånd.
Från molekylär förändring till neuron-död
För att se hur lägre METTL3 direkt kunde påverka neuroner vände sig forskarna till mus-hippocampusceller odlad i skålar. När de använde små interfererande RNA för att tysta METTL3 blev cellerna mycket mer sårbara för skadlig behandling med rapamycin, ett läkemedel som stressar neuroner. Dessa METTL3-depleterade celler visade högre nivåer av klassiska ”cellsjälvmords”-proteiner såsom Bax och klyvt caspas-3, och fler celler flaggades som apoptotiska vid flödescytometri. Djupare RNA-analyser pekade ut en enskild gen, CDKN1A (som kodar för proteinet p21), som en central aktör: när METTL3 slogs ner ökade CDKN1A-nivåerna kraftigt.
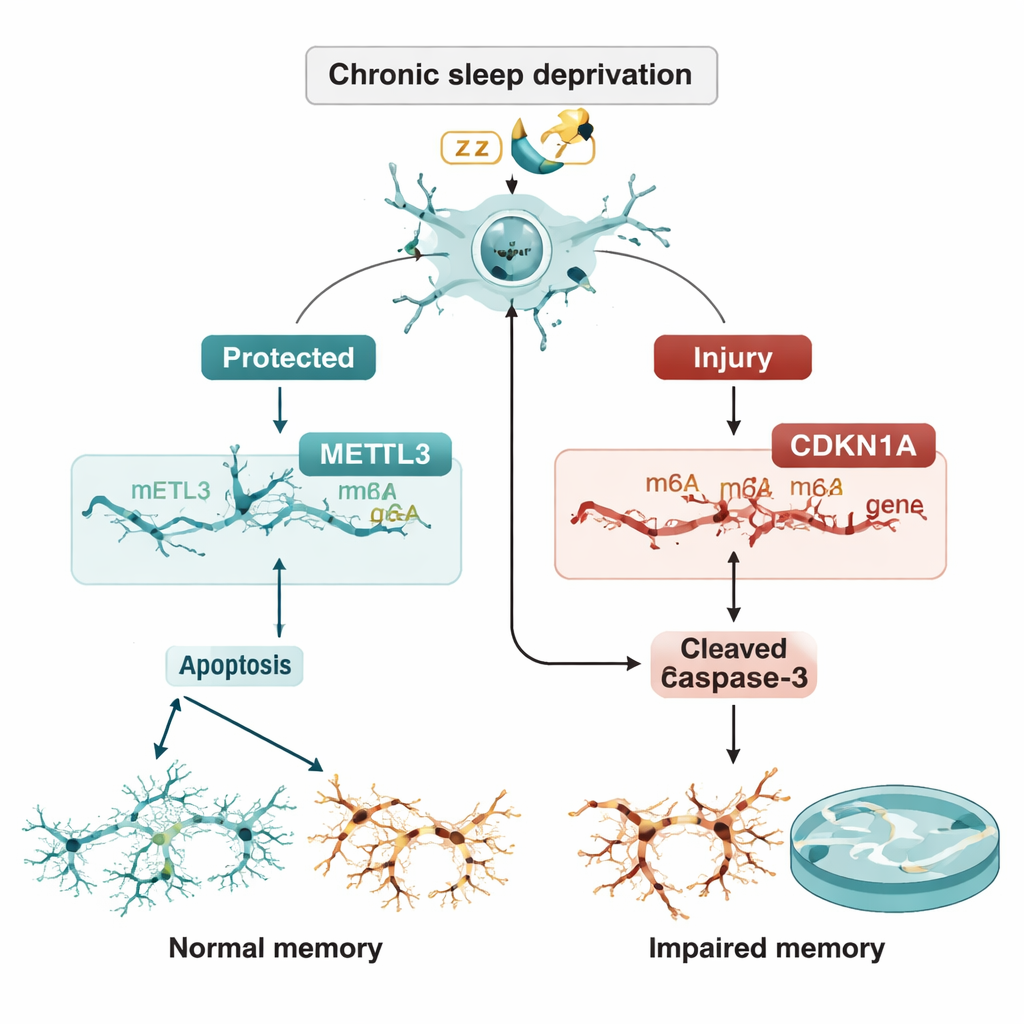
En skör balans mellan skydd och självförstörelse
Teamet undrade sedan om METTL3 styr CDKN1A via m6A-märkning. De visade att minskad METTL3 sänkte m6A-markeringarna på CDKN1A-RNA och gjorde det RNA:t mer stabilt, så att dess nivåer byggdes upp istället för att brytas ner. Högre CDKN1A drev i sin tur neuroner mot apoptos. Avgörande var att när CDKN1A självt slogs ner återställdes den extra celldöd som orsakats av förlust av METTL3 till stor del. Hos levande råttor minskade leverans av extra METTL3 direkt in i CA3-regionen med ett virusvektor CDKN1A-nivåerna, sänkte förekomsten av apoptosproteiner, bevarade neuronal struktur vid vävnadsfärgning och förbättrade prestationen i vattenlabyrinten trots fortsatt sömnbrist.
Vad detta betyder för personer som inte får tillräckligt med sömn
Enkelt uttryckt verkar kronisk sömndeprivation dämpa ett skyddande enzym, METTL3, i en kritisk minneskrets i hjärnan. När METTL3 sjunker kan det inte längre märka vissa RNA korrekt, särskilt det som kodar för CDKN1A. Det RNA:t ackumuleras då, driver neuroner mot programmerad celldöd och bidrar till minnesproblem. Genom att återställa METTL3 kunde forskarna sänka CDKN1A, minska neuronförlust och rädda minnet hos sömnbristiga råttor. Även om detta arbete fortfarande är på djurstadiet identifierar det METTL3–CDKN1A-vägen som ett lovande mål för framtida läkemedel som syftar till att skydda hjärnan från de kognitiva konsekvenserna av kronisk sömnbrist.
Citering: Xing, F., Shi, XS., Gu, HW. et al. METTL3-mediated m6A modification regulates CDKN1A to attenuate chronic sleep deprivation-induced cognitive impairment and neuronal apoptosis in rats. Transl Psychiatry 16, 96 (2026). https://doi.org/10.1038/s41398-026-03855-4
Nyckelord: kronisk sömnbrist, hippocampus, RNA-metylation, neuronal apoptos, minnesnedsättning