Clear Sky Science · sv
Olika och platsbundna roller för PlexinA2, PlexinA4 och NCAM i utvecklande hippocampala mossfibrer
Hur nervbanor formar minneskretsar
Hippocampus, en hjärnregion avgörande för att bilda och hämta minnen, kopplas ihop av tunna nervfibrer som under tidig utveckling måste navigera med precision. Denna studie ställer en till synes enkel fråga: hur vet dessa växande fibrer exakt vart de ska — och vad händer när deras vägledningssystem fungerar fel, vilket potentiellt kan bidra till tillstånd som schizofreni, autism eller epilepsi?
Två motorvägar till minnescentret
I hippocampus skickar nervceller i ett område som kallas dentate gyrus ut långa fibrer, så kallade mossfibrer, mot ett annat område som kallas CA3. När de går in i CA3 delar dessa fibrer normalt upp sig i två distinkta ”motorvägar”: en som löper ovanför ett lager av CA3-cellkroppar och en som löper under. Varje väg kopplar till olika delar av CA3-cellerna och hjälper till att ställa in aktivitetens balans i denna minneskrets. Om dessa banor inte separerar ordentligt kan fibrer hamna på fel plats, vilket kan störa hur information flödar genom hippocampus.
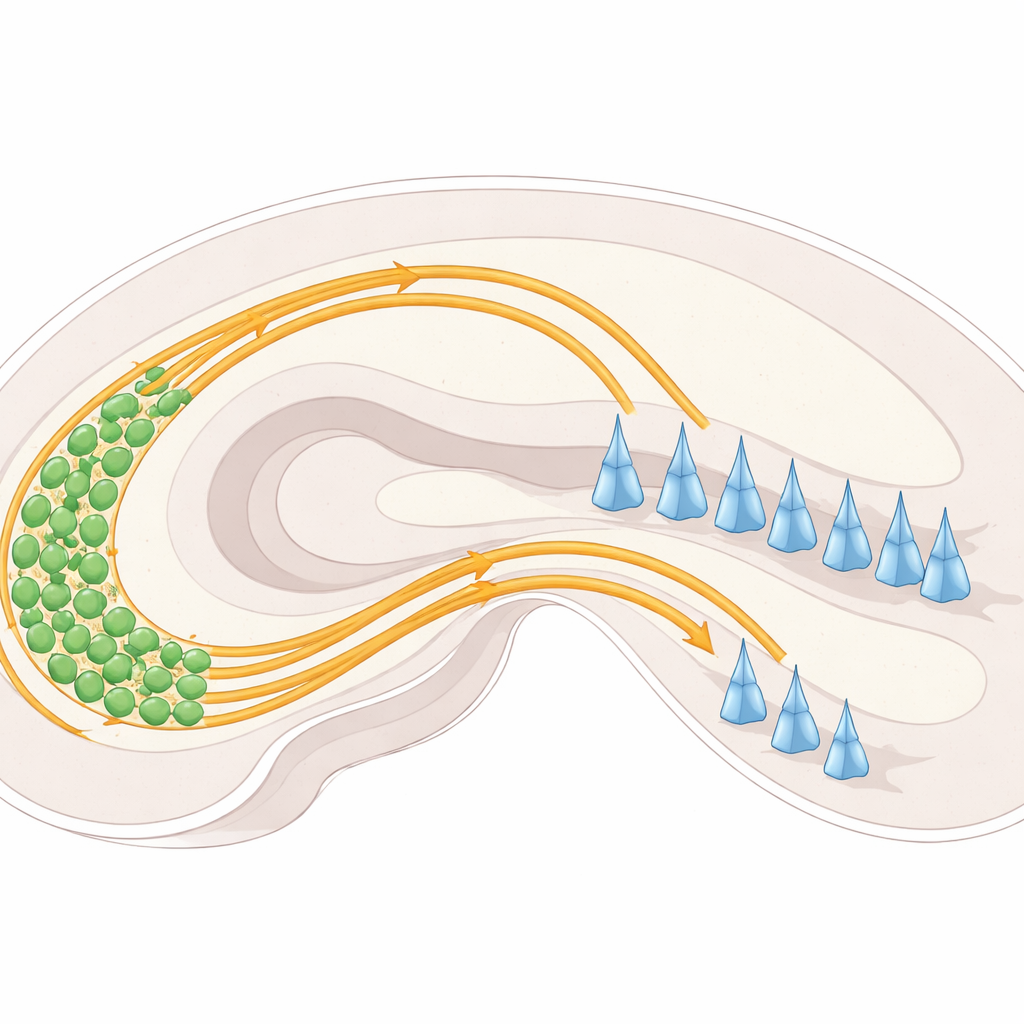
Vägledningssignaler: bortstötning, dragning och cell-till-cell-grepp
Forskarna fokuserade på ett nätverk av molekylära vägvisare och ythandtag på nervceller som styr mossfibrerna. En proteinfamilj kallad plexiner (PlexinA2 och PlexinA4) sitter på nervcellers yta och svarar på partnermolekyler kända som semaphoriner, särskilt Sema6A. Dessa interaktioner kan fungera som ”stopp”-signaler som pressar fibrer bort från vissa områden, eller finjustera hur hårt intilliggande fibrer håller ihop. Ett annat ytprotein, NCAM, beter sig mer som kardborre — främjar adhesion och hjälper buntar av fibrer att hålla ihop. Genom att undersöka var dessa proteiner uttrycks och vad som händer när de tas bort eller förändras i möss, kartlade teamet hur de samarbetar i levande hjärnor snarare än i isolerade celler.
Att dissekera roller med designer-möss
För att reda ut varje komponents roll skapade forskarna och kombinerade 27 olika muslinjer. Vissa saknade Sema6A helt, andra saknade PlexinA2 eller PlexinA4, och ytterligare andra bar subtila punktmutationer som inaktiverade endast en specifik ”enzymkärna” inom plexinerna medan resten av molekylen förblev intakt. De tog också bort Sema6A eller NCAM selektivt från vissa celltyper, såsom granuleceller i dentate gyrus, för att testa var signalen verkligen spelade roll. I möss som saknade Sema6A i dessa granuleceller delade sig inte mossfibrerna rent i övre och nedre buntar, och den nedre bunten växte för långt och översköt sitt normala slutmål. Liknande men inte identiska ledningsfel sågs i möss som saknade PlexinA2 eller PlexinA4, vilket visar att dessa proteiner agerar vid olika kontrollpunkter längs samma väg.
Närmare granskning av mekanismer och partnerskap
När författarna inaktiverade den katalytiska kärnan i PlexinA4 återuppstod många — men inte alla — av de defekter som sågs i fullständiga PlexinA4-utslagningsmöss. Detta visade att PlexinA4 ofta förlitar sig på denna kärna för att omforma det inre skelettet i växande nervfibrer, vilket hjälper dem att buntas korrekt och stanna vid rätt lager. PlexinA2 visade sig vara annorlunda: några av dess roller berodde på dess katalytiska kärna, medan andra inte gjorde det, vilket indikerar ytterligare, enzymoberoende signalvägar. Teamet använde sedan en närhetsmärkningsteknik för att identifiera närliggande proteiner runt PlexinA2 på unga hippocampala neuroner. Flera celladhesionsmolekyler framträdde, där NCAM stack ut. Genetiskt såg man att en samtidig reduktion av både PlexinA2 och NCAM gav starkare felstyrning av mossfibrerna än reduktion av endera för sig, vilket visar att dessa två system samarbetar: NCAM ger adhesion, medan PlexinA2-baserad repulsion kalibrerar hur fibrerna separerar i övre och nedre banor och hur långt den nedre banan sträcker sig.
När signaler går i motsatt riktning
Intressant nog fungerar Sema6A inte bara som en extern ”skylt” som plexiner läser av; den kan också fungera som en mottagare på mossfibrerna själva. Forskarna studerade möss där Sema6A:s interna svans togs bort medan dess yttre del var intakt. Hos dessa djur kvarstod vissa vägledningsfel — särskilt överväxt av den nedre bunten — vilket indikerar att signaler som rinner inåt genom Sema6A:s svans (”revers signalering”) är nödvändiga för normal beskärning och formning av mossfibrerna. Detta reversa läge verkar troligtvis fungera tillsammans med den mer bekanta plexinbaserade signaleringen i ett steg- och platsberoende sätt.
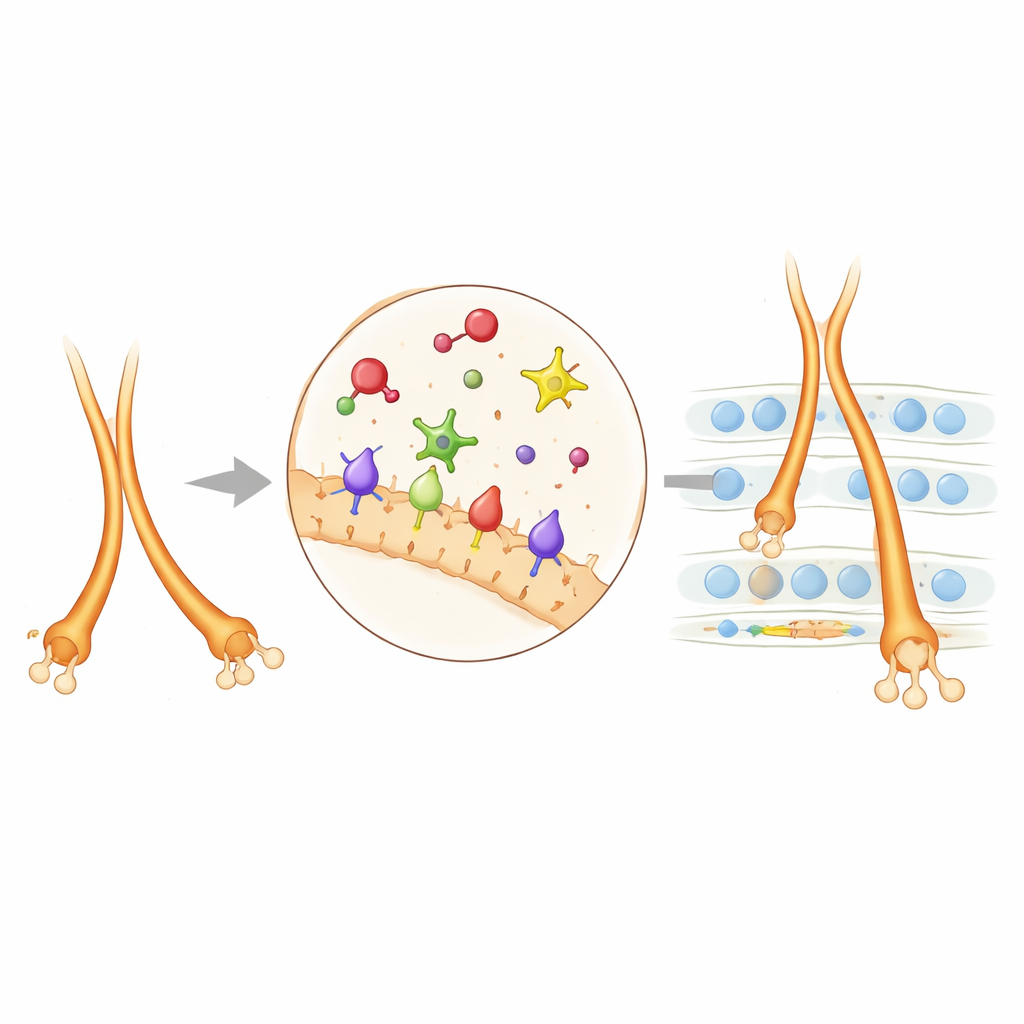
Varför denna koppling är viktig för hjärnhälsa
Mutationer i mänskliga motsvarigheter till PLXNA2, SEMA6A och NCAM1 har kopplats till neurodevelopmentala och psykiatriska tillstånd, från intellektuell funktionsnedsättning till schizofreni och autism. Genom att visa exakt hur dessa molekyler samarbetar för att forma mossfibervägarna hos möss erbjuder studien en konkret modell för hur subtila genetiska förändringar kan störa bildandet, separationen och beskärningen av viktiga minneskretsar. I vardagliga termer antyder arbetet att hjärnans vägledningsverktyg använder en noga avvägd blandning av signaler för ”skjut”, ”dra” och ”klibbighet” för att bygga hippocampus kopplingsschema — och att även små störningar i detta verktyg kan ge ringar på vattnet i form av förändringar i lärande, minne och mental hälsa.
Citering: Zhao, XF., Kohen, R., Van Battum, E.Y. et al. Diverse and location-specific roles of PlexinA2, PlexinA4, and NCAM in developing hippocampal mossy fibers. Transl Psychiatry 16, 126 (2026). https://doi.org/10.1038/s41398-026-03846-5
Nyckelord: hippocampala mossfibrer, axonavledning, semaphorin-plexin-signalering, NCAM och celladhesion, neurodevelopmentala störningar