Clear Sky Science · sv
Funktionstörning hos GABAerga interneuroner ligger bakom förändrade nervnätsoscillationer associerade med epileptiform aktivitet hos PPT1-bristande möss
När hjärtrytmer går fel
Anfall är inte bara plötsliga stormar av hjärnaktivitet; de växer ofta fram ur subtila förändringar i hur nervceller kommunicerar med varandra. Denna studie undersöker en sällsynt barndomsneurologisk sjukdom, CLN1, och ställer en enkel men långtgående fråga: vad händer med hjärnans inre "rytmhållare" när ett enda enzym, kallat PPT1, saknas? Genom att följa dessa förändringar i möss över tid visar forskarna hur små tidiga fel i inhibering kan växa till anfall och omfattande hjärnskador.
Balansens väktare i hjärnan
Våra hjärnor är beroende av två huvudtyper nervceller. Excitatoriska celler, som pyramidceller i hippocampus, driver aktiviteten framåt. Inhibitoriska celler, kallade interneuroner, fungerar som bromsar, håller denna aktivitet i schack och formar hjärnans elektriska rytmer. Bland dessa finns två viktiga grupper: parvalbumin-positiva (PV+) interneuroner och somatostatin-positiva (SST+) interneuroner. De hjälper till att generera och samordna rytmiska hjärnvågor, såsom theta- och gamma-oscillationer, som stödjer funktioner som inlärning och minne. Vid CLN1-sjukdom förlorar barnen enzymet PPT1, som normalt avlägsnar fettsyragrupper från proteiner. Författarna använde en musmodell med samma mutation som hos patienter för att se hur denna förlust påverkar interneuronerna och de rytmer de hjälper till att kontrollera.
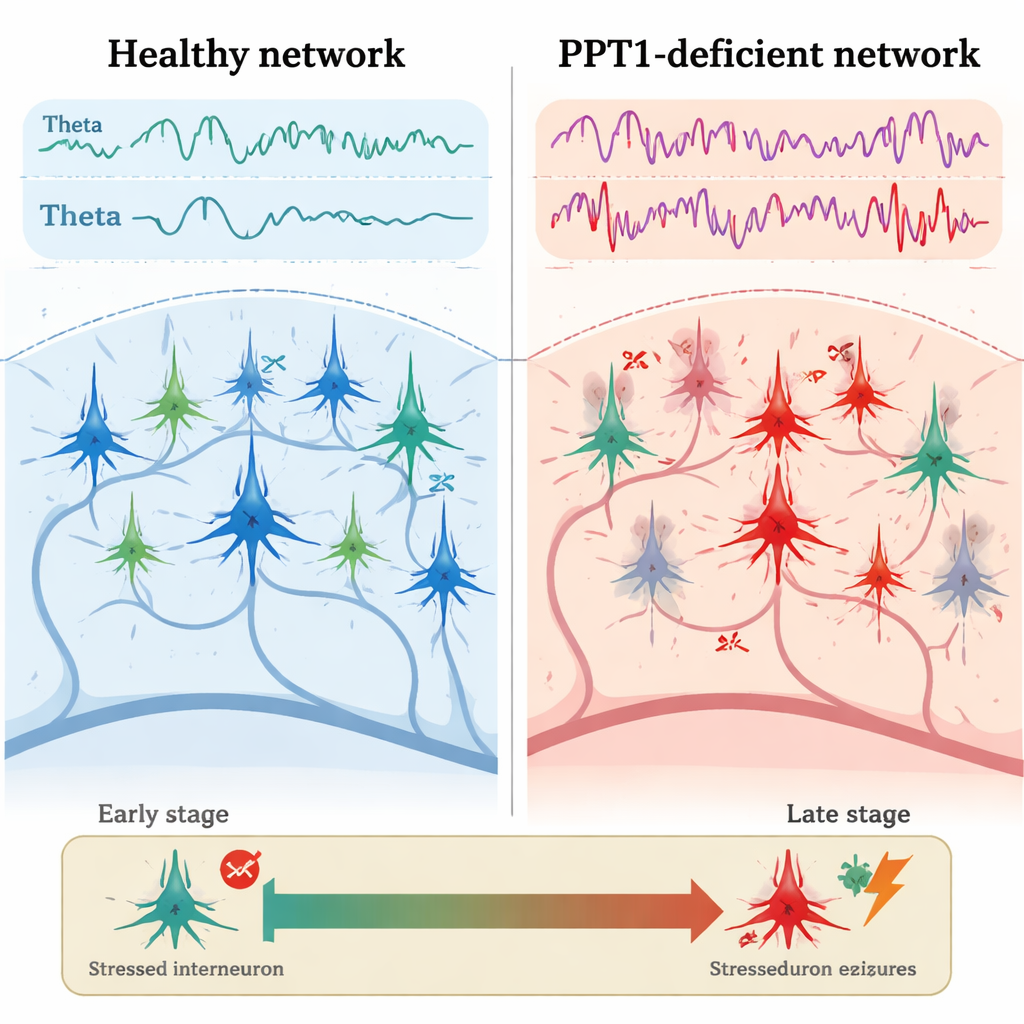
Tidiga sprickor i det inhibitoriska systemet
Hos unga vuxna mutantmöss, cirka tre till fyra månader gamla, dök det första tydliga problemet upp i PV+ interneuronerna. Elektriska inspelningar från hippocampus visade att dessa inhibitoriska celler fyrade mindre frekvent än hos friska möss, medan närliggande pyramidceller fyrade snabbare och med kortare pauser mellan spikarna. Mikroskopi avslöjade att många PV+ interneuroner hade aktiverat kaspas-3, en nyckelutförare i programmerad celldöd, även om deras totala antal ännu inte hade sjunkit. Samtidigt ökade styrkan i theta- och gammahjärnvågor, och kalciumbildning visade starkare aktivitet i hippocampala neuroner när djuren rörde sig runt. Avgörande var att den normala "korssnacket" mellan theta- och gamma-rytm—där långsammare vågor hjälper till att organisera snabbare—försvagades, vilket antyder en tidig kollaps i den fina tidningen av nätverksaktivitet.
Från störda rytmer till anfallsutbrott
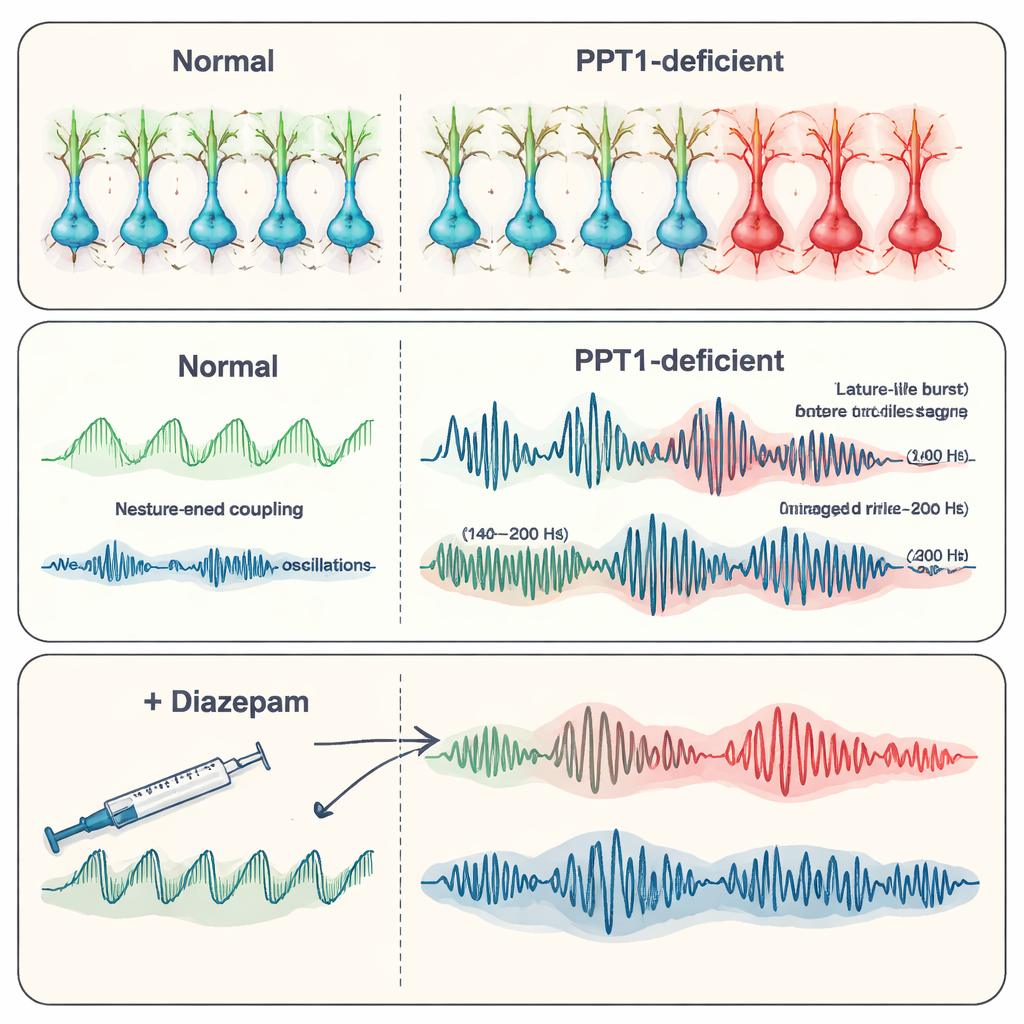
Vid sex till sju månaders ålder förvärrades situationen. Många PV+ interneuroner var förlorade, och nu visade även SST+ interneuroner tecken på kaspas-3-aktivering. Inspelningar från hippocampus avslöjade spontana epileptiforma urladdningar—korta, onormala aktivitetsutbrott associerade med anfall. Teamet fokuserade på högfrekventa "ripplar", snabba oscillationer som normalt hjälper till att lagra minnen. Hos mutationsmössen blev fysiologiska ripplar (runt 140–200 hertz) mindre frekventa men med större amplitud, medan ännu snabbare "patologiska" ripplar (200–500 hertz), som är starkt kopplade till epilepsi, blev starkare och vanligare. Tillsammans föreslog dessa förändringar en förskjutning från organiserade, minnesrelaterade rytmer mot kaotiska, anfallsbenägna mönster när den inhibitoriska kontrollen brast.
Neuroner slits ut och diazepam träder in
När sjukdomen framskred började själva hippocampus degenerera. Kalciumsignaler i neuroner minskade, Golgi-färgning visade tunnare, mindre förgrenade dendritiska träd, och det fanns färre små taggar där synapser bildas. Räkningar av neuroner i viktiga hippocampala regioner (CA1 och CA3) bekräftade omfattande cellförlust, och färre aktiva enheter kunde plockas upp i elektriska inspelningar. Forskarna testade sedan diazepam, ett vanligt anfallsdämpande läkemedel som förstärker den inhibitoriska signalsubstansen GABAs verkan. Hos äldre mutantmöss minskade diazepam frekvensen av epileptiska urladdningar och återställde delvis mer normala oscillationsmönster, inklusive ripplar, även om det inte reparerade den underliggande receptorförlusten. Detta tyder på att förstärkning av kvarvarande inhibitoriska signaler fortfarande kan lugna nätverket, åtminstone tillfälligt.
Varför dessa fynd betyder något
För en allmän läsare är huvudbudskapet att CLN1-sjukdom inte bara handlar om ansamling av avfall i hjärnceller. Förlusten av PPT1 sätter igång en kedjereaktion: först blir specialiserade inhibitoriska interneuroner stressade och börjar svikta, vilket frigör överaktiva pyramidceller och förvränger hjärnans rytmer. Med tiden leder denna obalans till anfall och så småningom till storskalig förlust av hjärnceller och förbindelser. Studien pekar på ett tidsfönster tidigt i sjukdomen då skydd eller räddning av PV+ interneuroner—kanske genom att blockera kaspasaktivering—kan förhindra senare anfall och degeneration. Även om diazepam inte kan bota CLN1, belyser dess förmåga att dämpa onormala rytmer i denna modell den bredare idén att återställande av inhibering kan vara en kraftfull strategi vid epilepsi och närliggande hjärnsjukdomar.
Citering: Tong, J., Liu, W., Wang, Q. et al. Dysfunction of GABAergic interneurons underlies altered neural network oscillations associated with epileptiform activity in PPT1-deficient mice. Transl Psychiatry 16, 106 (2026). https://doi.org/10.1038/s41398-026-03843-8
Nyckelord: epilepsi, interneuroner, hippocampus, hjärnoscillationer, lysosomal lagringssjukdom