Clear Sky Science · sv
Tidiga funktionella förändringar och plasmatiskt GFAP i svenska familjer med autosomalt dominant Alzheimers sjukdomsmutationer
Varför denna studie betyder något för familjer
Alzheimers sjukdom upplevs ofta som ett plötsligt insjuknande, men i verkligheten byggs skadliga förändringar i hjärnan upp tyst under många år. I sällsynta familjer som bär ärftliga (”autosomal dominanta”) Alzheimersmutationer kan forskare uppskatta när symtomen sannolikt börjar och följa dessa tidiga förändringar. Denna studie följde svenska familjer med sådana mutationer för att förstå hur hjärnans energianvändning, tänkande förmågor och en blodmarkör för hjärnans stödjeceller (GFAP) förändras lång tid innan minnesproblem uppstår — och hur dessa förändringar skiljer sig mellan gener.
Att följa sjukdomsklockan i högriskfamiljer
Eftersom personer med autosomalt dominant Alzheimers sjukdom (ADAD) vanligtvis utvecklar symtom vid en hyfsat förutsägbar ålder kan forskare beräkna ”uppskattade år till symtomdebut” (EYO) — hur många år någon befinner sig före eller efter sin förväntade första sjukdomssignal. Teamet studerade 45 vuxna från svenska familjer med APP- eller PSEN1-mutationer samt släktingar utan mutationer. Under i genomsnitt mer än sju år genomgick deltagarna hjärnavbildning som mäter hur mycket socker hjärnan använder (FDG PET), detaljerade kognitiva och minnestest, och för en del deltagare blodprover för GFAP, ett protein som frisätts när hjärnans stödjeceller, astrocyter, blir reaktiva. Denna uppläggning gjorde det möjligt för forskarna att lägga olika biologiska förändringar längs en gemensam sjukdomstidlinje i stället för att bara jämföra personer vid ett enda tillfälle.
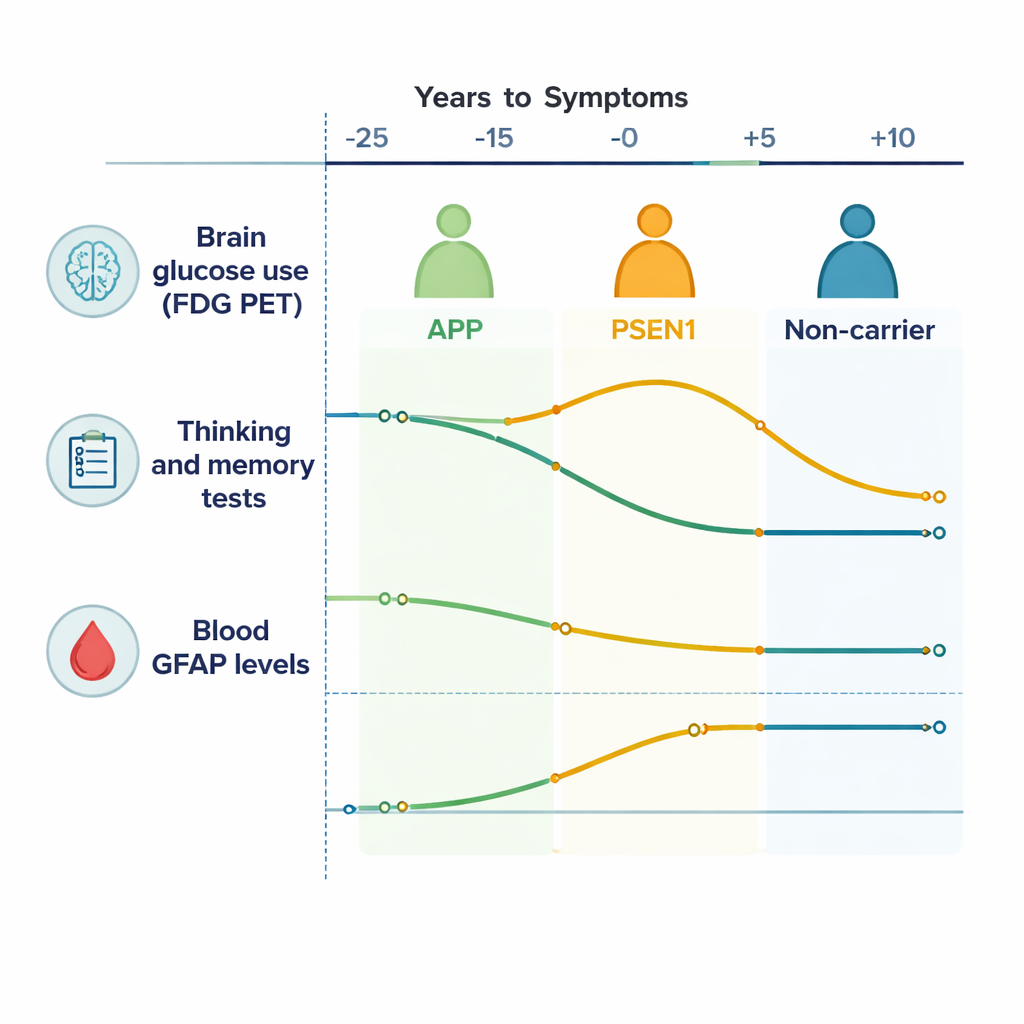
Att följa hjärnans energi och tänkande över tid
Över hjärnans yttre lager (kortex) visade personer med Alzheimersmutationer en gradvis minskning av FDG PET-signal jämfört med familjemedlemmar utan mutationer, vilket betyder att deras hjärnor använde mindre socker över tid — ett tecken på nedsatt cellfunktion. Subkortikala områden djupt i hjärnan, särskilt nucleus caudatus och thalamus, visade också minskad aktivitet, främst drivet av dem med APP-mutationer. Kognitiva och minnestester försämrades över flera domäner, inklusive episodiskt minne och mental flexibilitet, med start ungefär 10–15 år före förväntad symtomdebut. Med andra ord, även när personer fortfarande kände sig och fungerade normalt i vardagen, avslöjade känsliga tester och avbildningar att deras hjärnor redan arbetade hårdare och mindre effektivt.
Olika mönster för olika Alzheimers-gener
En viktig insikt var att de två stora mutationsgrupperna — APP och PSEN1 — inte följde identiska banor. Hos PSEN1-bärare observerade forskarna en tidig period, cirka 20 till 10 år före förväntade symtom, där delar av hjärnan faktiskt visade ovanligt hög sockeranvändning (”hypermetabolism”), tillsammans med bättre testprestationer, innan de senare sjönk. Detta återspeglar sannolikt en tillfällig kompensationsfas där hjärnan och dess stödjeceller ökar aktiviteten för att hantera växande skada. APP-bärare, däremot, visade ett mer rakt förlopp med en gradvis minskning av hjärnmetabolismen utan denna tidiga topp. Dessa genspecificerade mönster tyder på att ”Alzheimers sjukdom” inte är en enda biologisk berättelse, även i ärftliga former, utan en familj av besläktade processer som utvecklas olika beroende på underliggande mutation.
Vad ett blodprov avslöjar om tidig hjärnpåfrestning
GFAP, mätt i ett enkelt blodprov, gav en inblick i hur astrocyter svarar på tidiga Alzheimersförändringar. GFAP-nivåerna tenderade att stiga stadigt när personer närmade sig sin förväntade symtomsålder både hos mutationsbärare och icke-bärare, men sambanden mellan GFAP, hjärnmetabolism och kognition var genspecificerade. Hos APP-bärare var högre GFAP kopplat till fallande hjärnskockeranvändning i djupa hjärnregioner och till försämrad prestation i de flesta kognitiva tester, vilket tyder på att astrocytaktivering är nära kopplat till tidig skada och funktionsförlust. Hos PSEN1-bärare var dessa samband svagare eller saknades, vilket återigen pekar på olika biologiska vägar till samma kliniska slutpunkt, demens.
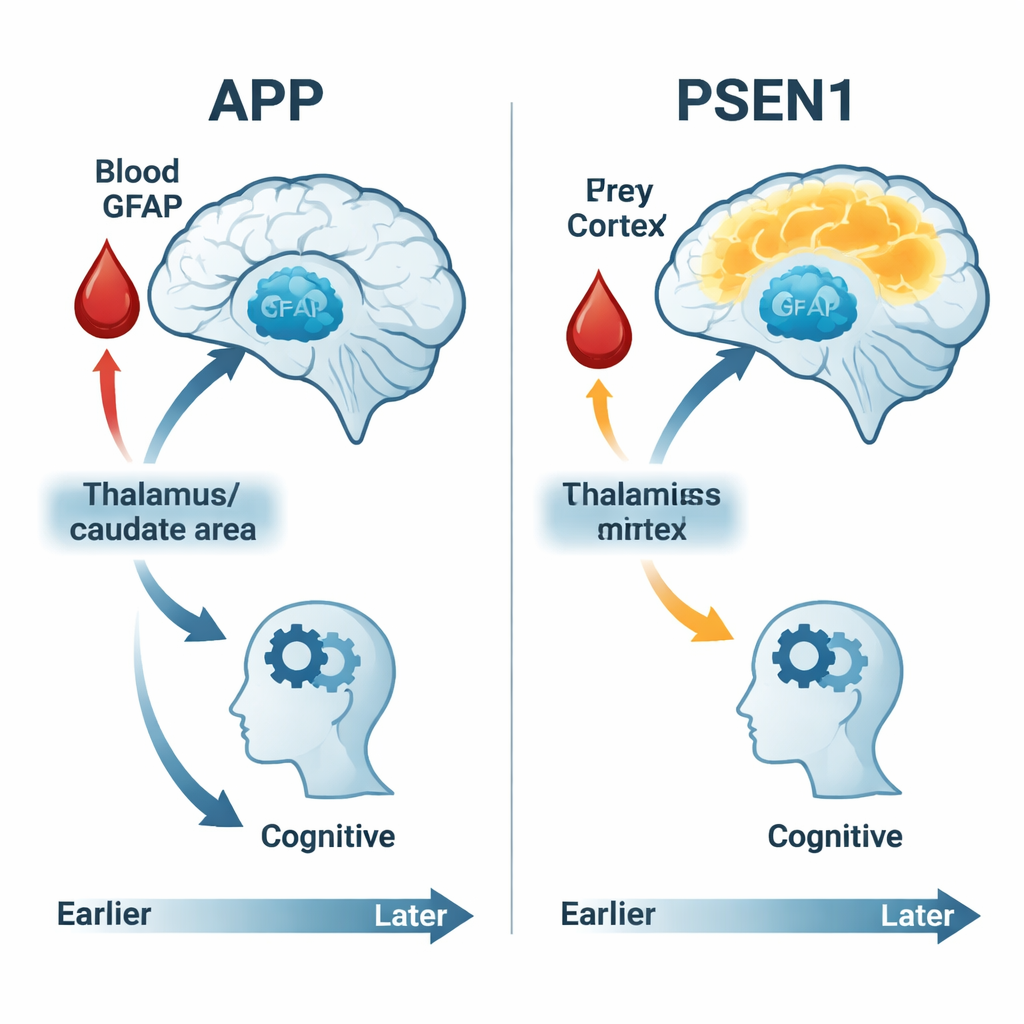
Vad detta betyder för tidig upptäckt och behandling
För en lekmannaläsare är huvudbudskapet att i dessa högriskfamiljer börjar Alzheimersrelaterade förändringar decennier innan tydlig minnesförlust — och att de inte ser likadana ut för alla. Hjärnavbildning av sockeranvändning, finmaskig kognitiv testning och en enda blodmarkör som GFAP kan tillsammans visa när hjärnan börjar få svårigheter och hur snabbt dessa svårigheter utvecklas. Viktigt är att personer med olika genetiska former av Alzheimers visar olika förändringssekvenser: vissa har en tidig överaktiv fas, andra visar en stadig nedgång, och blodmarkören för astrocytstress hänger starkare ihop med skada i vissa grupper än i andra. Att känna igen dessa distinkta spår kan hjälpa till att skräddarsy framtida läkemedel och prövningar till rätt personer vid rätt tidpunkt, och stärker hoppet om att blodprov som GFAP kan fånga Alzheimers tidigare — innan symtom berövar människor deras självständighet.
Citering: Luckett, E.S., Zapater-Fajari, M., Almkvist, O. et al. Early functional changes and plasma GFAP in Swedish families with Autosomal Dominant Alzheimer’s disease mutations. Transl Psychiatry 16, 67 (2026). https://doi.org/10.1038/s41398-026-03829-6
Nyckelord: autosomal dominant Alzheimers sjukdom, GFAP blodbiomarkör, hjärnans glukosmetabolism, astrocyter och neurodegeneration, tidig upptäckt av Alzheimers