Clear Sky Science · sv
Histamin H3-receptorn som mål för alkoholrelaterade störningar: att utmana djurmodellers förutsägbarhet för klinisk översättning i läkemedelsutveckling
Varför denna forskning spelar roll i vardagen
Alkoholrelaterade störningar drabbar miljontals människor världen över, men de läkemedel som finns i dag hjälper bara en bråkdel av dem som behöver det. Denna artikel följer den kompletta resan för en lovande ny läkemedelskandidat, BP1.3656B, från labbbank till mänskliga prövningar. Den visar hur en idé som fungerar utmärkt i djur ändå kan misslyckas hos människor — och varför det gapet spelar roll för alla som hoppas på bättre behandlingar för problematiskt drickande.
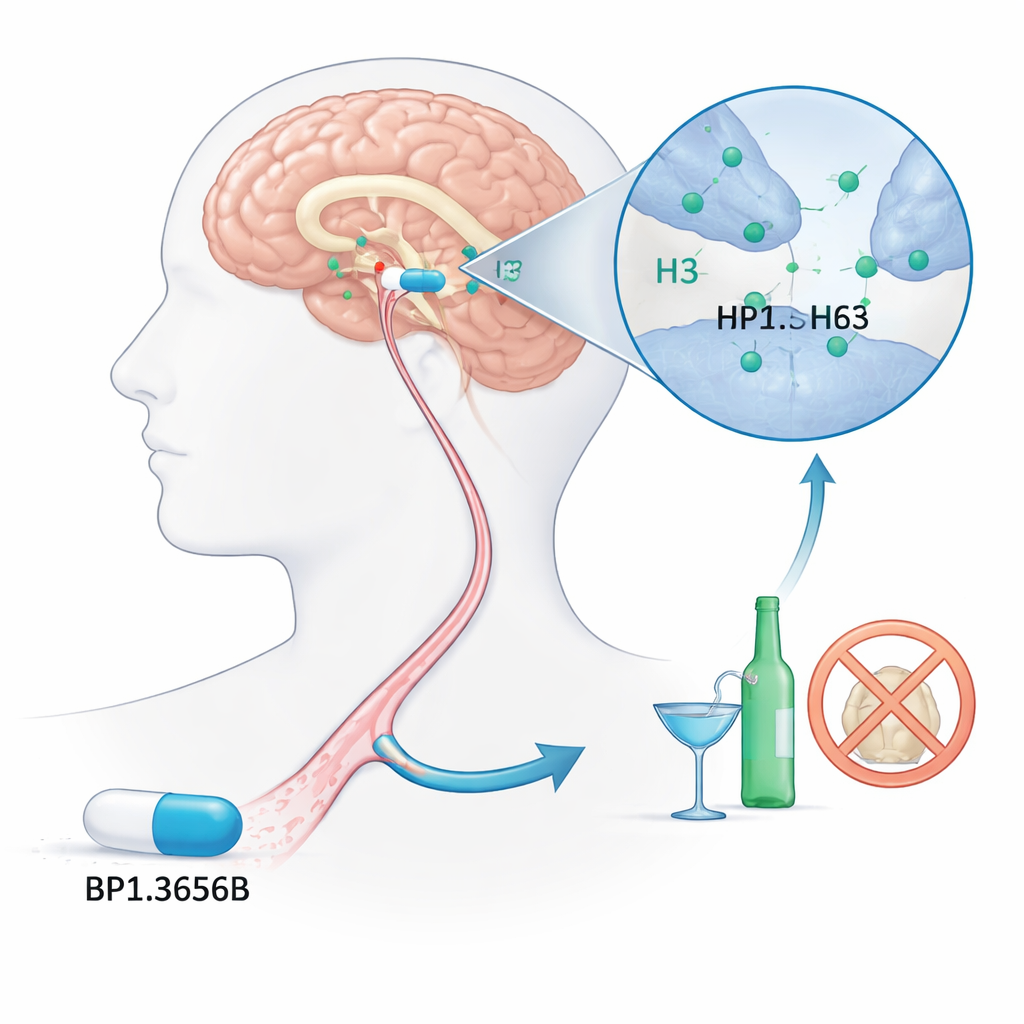
Ett nytt hjärnmål för problematiskt drickande
Forskarna fokuserade på en mindre känd hjärnreglerare kallad histamin H3-receptorn. Histamin är mest känt för sin roll vid allergier, men i hjärnan hjälper det till att reglera vakenhet och kommunikationen mellan nervceller. H3-receptorn fungerar som en dimmer som dämpar frisättningen av histamin och flera andra kemiska budbärare som är involverade i belöning och motivation. Eftersom alkohol starkt påverkar dessa hjärnsystem har forskare länge misstänkt att blockering av H3-receptorer skulle kunna minska driften att dricka. BP1.3656B designades som en kraftfull blockerare av H3, i hopp om att den skulle kunna dämpa alkohols dragningskraft på hjärnans belöningskretsar.
Från kemi till framgångar i djurförsök
I tidiga tester visade BP1.3656B den typ av profil som läkemedelsutvecklare drömmer om. Den band mycket hårt och selektivt till H3-receptorn, tog sig väl in i hjärnan och verkade säker i standardiserade labbtester. Hos möss minskade läkemedlet den aktivitetstopp som normalt följer efter en alkoholdos och minskade måttligt binge-liknande drickande i ett ”drickande i mörkret”-test. Hos råttor tränade att trycka på en spak för alkohol minskade BP1.3656B kraftigt hur mycket de drack och hur hårt de var villiga att arbeta för att få alkohol, både hos djur som helt enkelt var storspottare och hos de som gjorts fysiskt beroende. Det dämpade också återfalls-liknande drickande och lindrade ångest kopplad till alkoholabstinens. Tillsammans pekade dessa resultat på att läkemedlet kunde sänka alkoholförstärkning och hjälpa till att förhindra återgång till tungt bruk.
Tidiga mänskliga tester: når läkemedlet sitt mål?
Därefter följde fas I-studier i friska frivilliga. Enstaka och upprepade doser upp till 90 mikrogram tolererades generellt väl, med främst milda sömnrelaterade biverkningar som stämmer med H3-blockerares vaknadsfrämjande natur. Blodmätningar visade ett tydligt, förutsägbart mönster för hur läkemedlet absorberades och utsöndrades. För att säkerställa att det träffade sitt avsedda mål i den levande mänskliga hjärnan använde teamet positronemissions-tomografi, en typ av hjärnavbildning som kan visa hur många receptorer som är ockuperade av ett läkemedel. Även relativt låga doser av BP1.3656B blockerade de flesta H3-receptorer i flera hjärnregioner viktiga för motivation och belöning, vilket bekräftade att läkemedlet åtminstone biologiskt gjorde vad det var utformat för att göra.
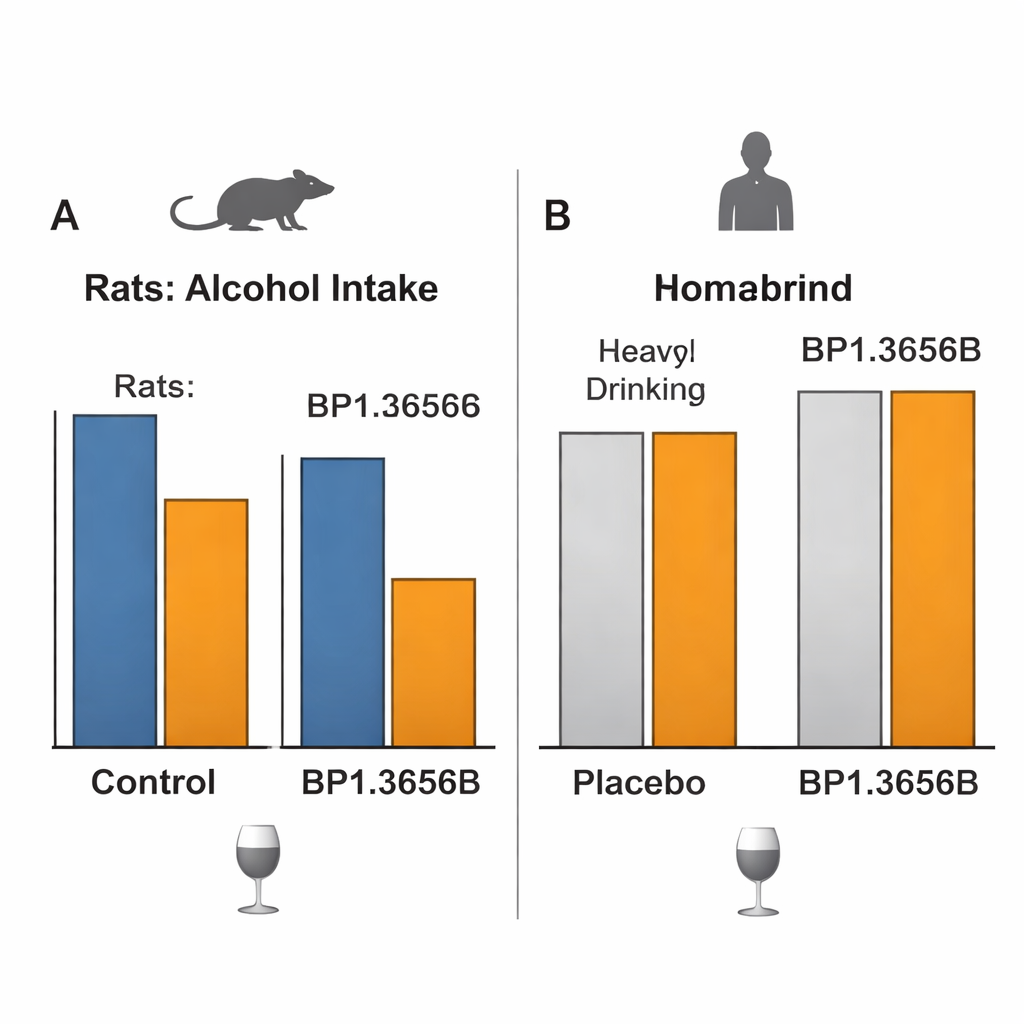
När lovande djurresultat inte översätts till människor
Den avgörande frågan var om allt detta skulle översättas till meningsfulla förändringar i drickande för människor med alkoholrelaterade störningar. I en noggrant kontrollerad labbstudie fick vuxna med alkoholproblem som inte sökte behandling BP1.3656B eller placebo och genomgick sedan sessioner där de själva kunde administrera intravenös alkohol genom att trycka på en knapp, under förhållanden avsedda att mäta både njutning och motivation. Läkemedlet hade ingen påtaglig effekt på hur mycket alkohol de valde att få. En större, 12-veckors multinationell klinisk prövning i patienter som sökte behandling prövade sedan tre dagliga doser av BP1.3656B mot placebo. Alla grupper, inklusive placebo, minskade avsevärt antalet tunga drickardagar och det totala alkoholintaget över tid, men läkemedlet överträffade inte placebo i någon större mått på drickande eller sug, trots god säkerhet och tydlig målbindning.
Vad detta betyder för framtida behandlingar
För en allmän läsare är slutsatsen dämpande men viktig: ett läkemedel som såg utmärkt ut i celler, möss och råttor — och tydligt nådde sitt mål i mänsklig hjärna — lyckades ändå inte få människor att dricka mindre. Det betyder inte att vetenskapen var felaktig, men det belyser hur osäkert det är att förutspå mänskliga resultat endast utifrån djurmodeller. Författarna argumenterar för att mindre, tidiga människor-labbstudier som direkt testar ett läkemedels effekt på alkoholbruk bör användas mer rutinmässigt för att ”minska risken” i utvecklingen innan stora, kostsamma prövningar. Med andra ord visar detta arbete att vi behöver inte bara nya läkemedelsidéer utan även bättre sätt att avgöra vilka av dessa idéer som verkligen har en chans att hjälpa människor som kämpar med alkoholrelaterade störningar.
Citering: Le Foll, B., Naassila, M., Jeanblanc, J. et al. Histamine H3 Receptor as a target for alcohol use disorder: challenging the predictability of animal models for clinical translation in drug development. Transl Psychiatry 16, 55 (2026). https://doi.org/10.1038/s41398-026-03807-y
Nyckelord: alkoholrelaterad störning, histamin H3-receptor, BP1.3656B, behandling av beroende, translativ forskning