Clear Sky Science · sv
Hämning av mitokondriell energiproduktion av ett fotosyntetiskt bakteriellt cupredoxinpeptid hämmar tumörtillväxt
Att omvandla bakterier till cancerkämpar
Cancerceller är energiförgärande. De är beroende av små interna ”kraftverk” kallade mitokondrier för att generera den energi de behöver för att växa, sprida sig och motstå behandling. Denna studie undersöker en oväntad allierad i kampen mot cancer: en kort fragment av ett protein som ursprungligen hittades i fotosyntetiska bakterier. Forskarlaget visar att denna designade peptid kan smyga in i cancerceller, stänga av deras energiförsörjning vid källan och göra strålbehandling betydligt effektivare – samtidigt som normala celler i stort sett skonas.
En liten peptid med ett stort uppdrag
Teamet utgick från en tidigare upptäckt att ett bakteriellt protein kallat azurin kan bromsa tumörtillväxt genom att påverka den välkända tumörsupressorn p53. De sökte därefter i bakterier som lever i och kring mänskliga tumörer, med fokus på fotosyntetiska mikrober som använder ljus för att skapa energi. Dessa bakterier bär på en besläktad familj av proteiner kallade cupredoxiner. Genom att jämföra deras strukturer och evolutionära historia identifierade forskarna en särskild cupredoxin, auracyanin B, och skar ut en kort, 28-aminosyra lång region som de kallade aurB. Detta fragment är vattenlösligt, kan passera cellmembran och har en form som antydde att det skulle kunna interagera med nyckelkomponenter i cellernas energiproducerande maskineri.
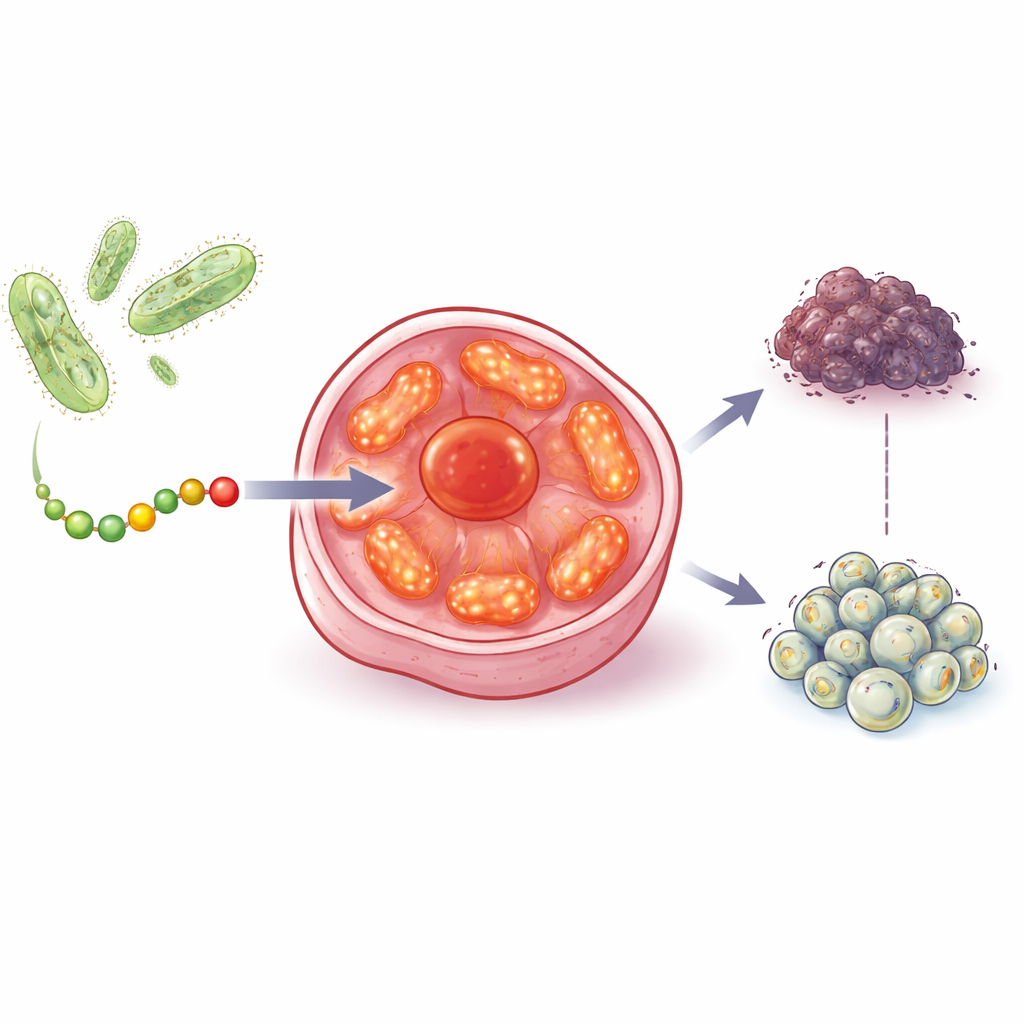
Att hitta och slå mot cancerns kraftverk
I laboratorietester minskade aurB överlevnaden hos bröst-, prostata-, kolorektal- och äggstockscellinjer, även när dessa celler saknade fungerande p53 eller hormonreceptorer som många nuvarande läkemedel kräver. Viktigt är att aurB hade mycket svagare effekter på normala prostata-, hjärt- och muskelceller, trots att dessa friska celler är rika på mitokondrier. Avbildningsexperiment visade att aurB föredrog att tränga in i cancerceller och sedan koncentreras i deras mitokondrier. Elektronmikroskopi, med aurB fäst vid små guldstänger som ett visuellt handtag, bekräftade att peptiden faktiskt ackumulerades i dessa organeller.
Att kapa energiförsörjningen
När aurB väl befann sig i mitokondrierna bundet den till en specifik komponent i ATP-syntaset – den molekylära turbinen som tillverkar ATP, cellens huvudsakliga energivaluta. Biokemiska pull-down-experiment och masspektrometri identifierade denna partner som ATP5C, en del av enzymets centrala kärna. Surface plasmon resonance-mätningar visade att aurB binder till ATP5C med måttlig styrka och långsam frisättning, vilket överensstämmer med en stabil interaktion. Funktionella tester visade vad denna bindning leder till: aurB reducerade kraftigt mitokondriellt ATP i prostatacancerceller, saktade ner hur snabbt de förbrukade syre och blockerade både andning och den backup-glykolysväg som kan kompensera. När energiproduktionen kollapsade uppvisade cancercellerna kännetecken för programmerad celldöd drivna av caspas-3, ett viktigt verkställarenzym.
Blockera tumörer och förstärka strålning
Forskarna testade därefter aurB i musmodeller av aggressiv prostatacancer. Hos djur med humana prostattumörer under huden krympte tumörtillväxten med ungefär två tredjedelar vid regelbundna injektioner av aurB, jämförbart med eller bättre än cytostatikumet paclitaxel, men utan uppenbar viktminskning eller tecken på lidande. Tumörprover från behandlade möss innehöll färre delande celler och många fler döende celler. I en andra modell som efterliknar skelettmetastas – en vanlig och dödlig plats för prostatacancerutbredning – bromsade aurB ensam tumörspridningen i lårbenet och minskade antalet lungmetastaser. När peptiden kombinerades med en måttlig stråldos blev effekten dramatisk: tumörer i det behandlade benet var nästintill utplånade, och lungmetastaserna minskade med mer än 90 procent jämfört med kontroller.
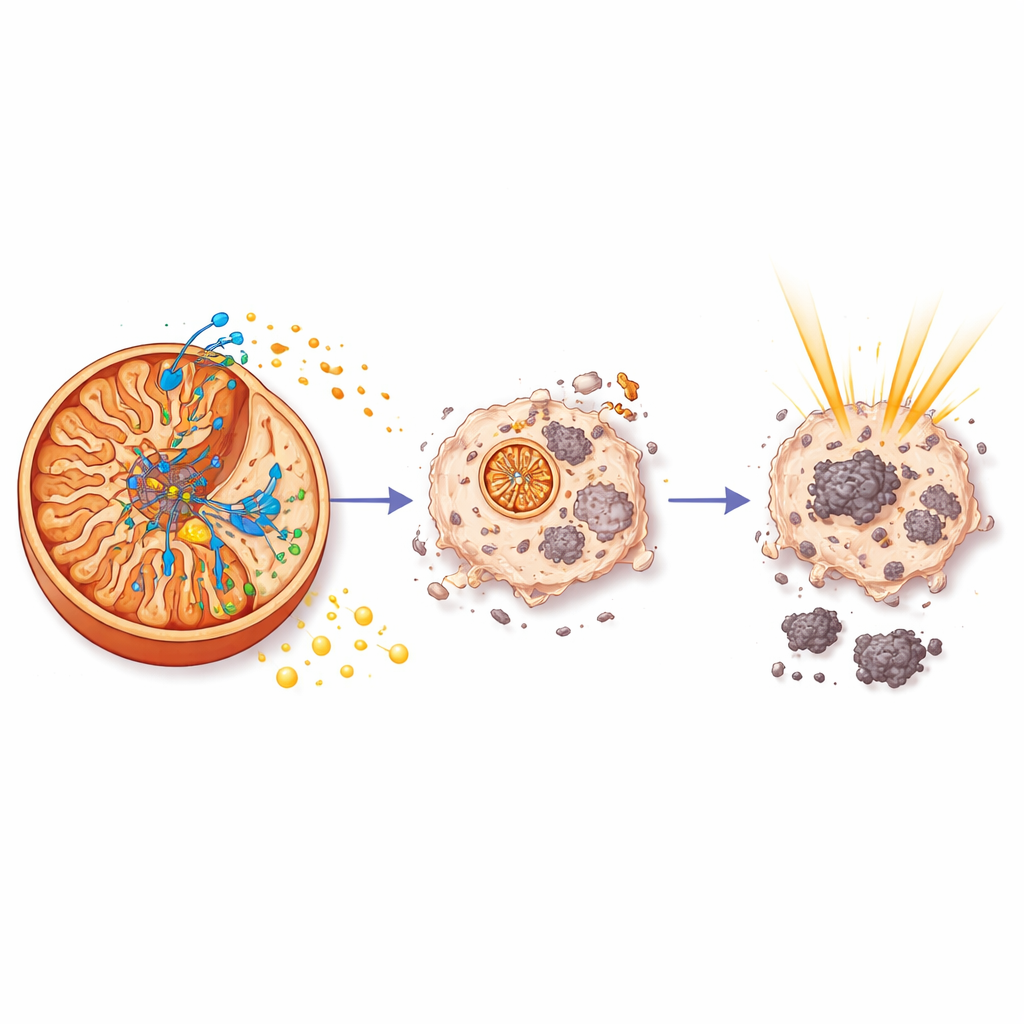
Varför energi spelar roll för strålning
För att förstå varför aurB gör strålning mer effektiv undersökte teamet genaktivitet i tumörer från behandlade möss. De fann att aurB, men inte strålning ensam, dämpade ett nätverk av gener styrda av HIF-1, en huvudregulator som hjälper cancerceller att anpassa sig till låg syrehalt och som driver resistens mot terapi. Under de energifattiga förhållanden som aurB skapade skruvades viktiga tillväxt- och överlevnadsvägar drivna av PI3K och c-Myc ner, och den glykolytiska maskineriet som tillåter tumörer att frodas i hårda miljöer undertrycktes också. I praktiken, genom att sabotera ATP-produktionen direkt vid den mitokondriella turbinen, kastade aurB cancercellerna i en energikris som gjorde dem mycket mer sårbara för strålningsskador.
En ny klass av precisionsinriktade energihämmare
Detta arbete introducerar en ny strategi för cancerterapi: att designa små, bakterieinspirerade peptider som söker upp mitokondriella energisystem som är förändrade i tumörer. AurB, härledd från ett fotosyntetiskt bakteriellt protein, riktar selektivt in sig på en komponent av ATP-syntas som ofta är överaktiv i cancerformer som prostata-, bröst-, äggstocks- och hjärntumörer. Genom att direkt svälta ut cancerceller på energi och försvaga deras försvar, särskilt mot strålning, kan sådana peptider komplettera befintliga behandlingar och erbjuda alternativ där immunbaserade metoder inte räcker. Mycket arbete återstår innan denna idé når kliniken, men studien visar att urgamla bakteriella energiproteiner kan återanvändas till moderna, höggradigt riktade anticancer-verktyg.
Citering: Naffouje, S.A., Tran, D.B., Rademacher, D.J. et al. Suppression of mitochondrial energy production by a photosynthetic bacterial cupredoxin peptide inhibits tumor growth. Sig Transduct Target Ther 11, 124 (2026). https://doi.org/10.1038/s41392-026-02703-7
Nyckelord: mitokondriell ATP-syntas, cancermetabolism, terapeutiska peptider, prostatacancer, strålningssensibilisering