Clear Sky Science · sv
Cykliskt guanosinmonofosfat–proteinkinas G‑signalering dämpar förkalkning av aortaklaffen via ULK1‑medierad autofagi
Varför ”rost” på hjärtklaffar spelar roll
Med åldern kan aortaklaffen – hjärtats främsta utloppsport – gradvis stelna och täckas av kalcium, ett tillstånd som kallas förkalkande aortaklaffsjukdom. Denna ”förhårdning” tvingar hjärtat att arbeta hårdare och kan leda till bröstsmärta, svimning, hjärtsvikt eller behov av klaffbyte. I dag finns inget läkemedel som pålitligt bromsar processen; läkarna kan bara vänta tills klaffen är allvarligt skadad och sedan operera. Denna studie undersöker en inneboende cellulär väg som verkar skydda klaffen från förkalkning, och testar ett modernt hjärtsviktsläkemedel som ett möjligt sätt att återaktivera det skyddet.
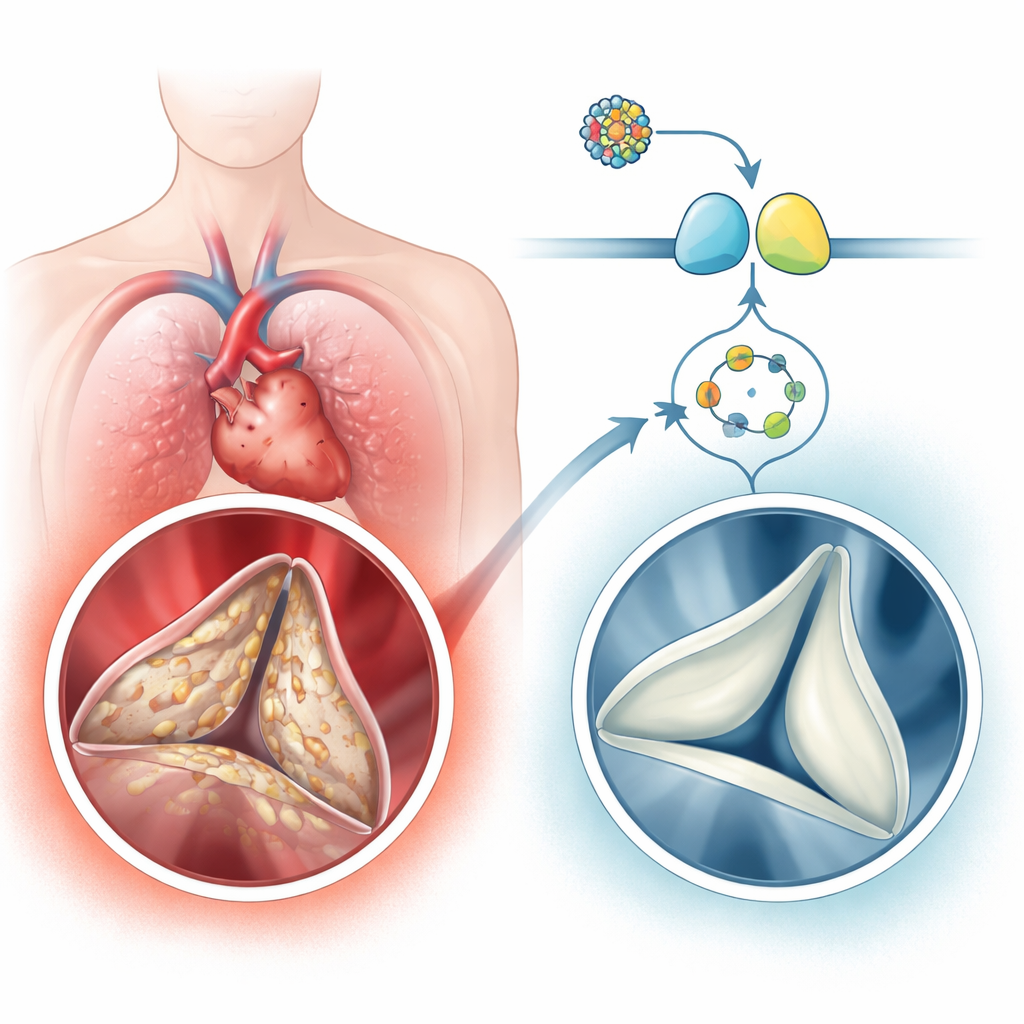
Ett vanligt men förbisedda hjärtproblem
Förkalkande aortaklaffsjukdom är förvånansvärt vanligt bland äldre och drabbar ett par procent av personer över 65 och upp till en av tio över 75. Sjukdomen är inte bara passivt ”slitage”. I stället omprogrammeras de mjuka bindvävscellerna i klaffen, så kallade valvulära interstitiella celler, till läknings‑ och benliknande tillstånd. De lägger ner extra kollagen och deponerar sedan kalcium, vilket förvandlar de tidigare flexibla seglen till styva, stenliknande flikar. Författarna analyserade mänsklig klaffvävnad och stora genuttrycksdatamängder och fann att en signalväg centrerad kring den lilla molekylen cGMP och dess partnerenzym proteinkinas G (PKG) konsekvent var nedreglerad i förkalkade klaffar, medan gener och proteiner kopplade till benbildning var uppreglerade. Personer med svår klafförkalkning hade också lägre cGMP‑nivåer i blodet, vilket korrelerade med hur trånga och hinderbildande deras klaffar var.
En skyddande signal som försvinner
För att undersöka orsak och verkan använde teamet möss och odlade mänskliga klaffceller. Möss konstruerade för att producera mindre PKG utvecklade tjockare, mer kraftigt förkalkade klaffsegel efter en kontrollerad skada på aortaklaffen, och deras klaffar visade högre nivåer av ett huvudreglerande benbildningsprotein. I mänskliga klaffceller odlade i skål under förhållanden som gynnar kalciumansamling accelererade nedreglering av PKG med genetiska verktyg denna benliknande omvandling. Dessa resultat tyder på att cGMP‑PKG‑signalering normalt fungerar som en broms mot skadlig cellomprogrammering i klaffen – och när denna broms försvagas accelererar förkalkningen.
Omdirigering av ett hjärtsviktsläkemedel
Forskarna frågade därefter om förstärkning av denna väg kunde sakta ner eller vända förkalkningen. De testade tre läkemedel som ökar cGMP på olika sätt, inklusive vericiguat, ett godkänt läkemedel för vissa patienter med hjärtsvikt. I mänskliga klaffceller minskade alla tre läkemedlen kalciumavlagringar och markörer för benliknande omvandling, där vericiguat visade starkast effekt. Vericiguat minskade också förkalkning i små bitar av mänsklig klaffvävnad som hölls levande utanför kroppen. I två musmodeller – en driven av en kolesterolrik diet och en av mekanisk skada på klaffen – ledde daglig behandling med vericiguat till tunnare, mindre förkalkade segel och bättre blodflöde över klaffen, utan att försvaga hjärtats pumpkraft. När PKG genetiskt reducerades förlorade vericiguat dock i stort sett sina fördelar, vilket indikerar att PKG är den avgörande nedströmsaktören.
Cellulär städning och friskare klaffar
Djupare analyser visade att vericiguat och PKG skyddade klaffcellernas små kraftverk, mitokondrierna. Under förkalkande förhållanden byggde cellerna upp skadliga reaktiva syreradikaler, förlorade mitokondriellt membranpotential och producerade mindre energi. Vericiguat återställde mitokondriernas funktion och minskade oxidativ stress. Storskaliga kartläggningar av proteiner och fosfat‑taggning pekade mot autofagi – cellens interna städ‑ och återvinningssystem. I förkalkade mänskliga klaffar visade mikroskopi och proteinmarkörer minskad bildning och aktivitet av autofagosomer, autofagins ”sopkassar”. I enkelcellanalyser visade flera undertyper av klaffceller från sjuka klaffar en bred undertryckning av autofagirelaterade program. I odlingsceller utsuddade blockering av autofagi den skyddande effekten av PKG‑aktivering, vilket antyder att PKG i huvudsak verkar genom att återuppliva detta städsystem.
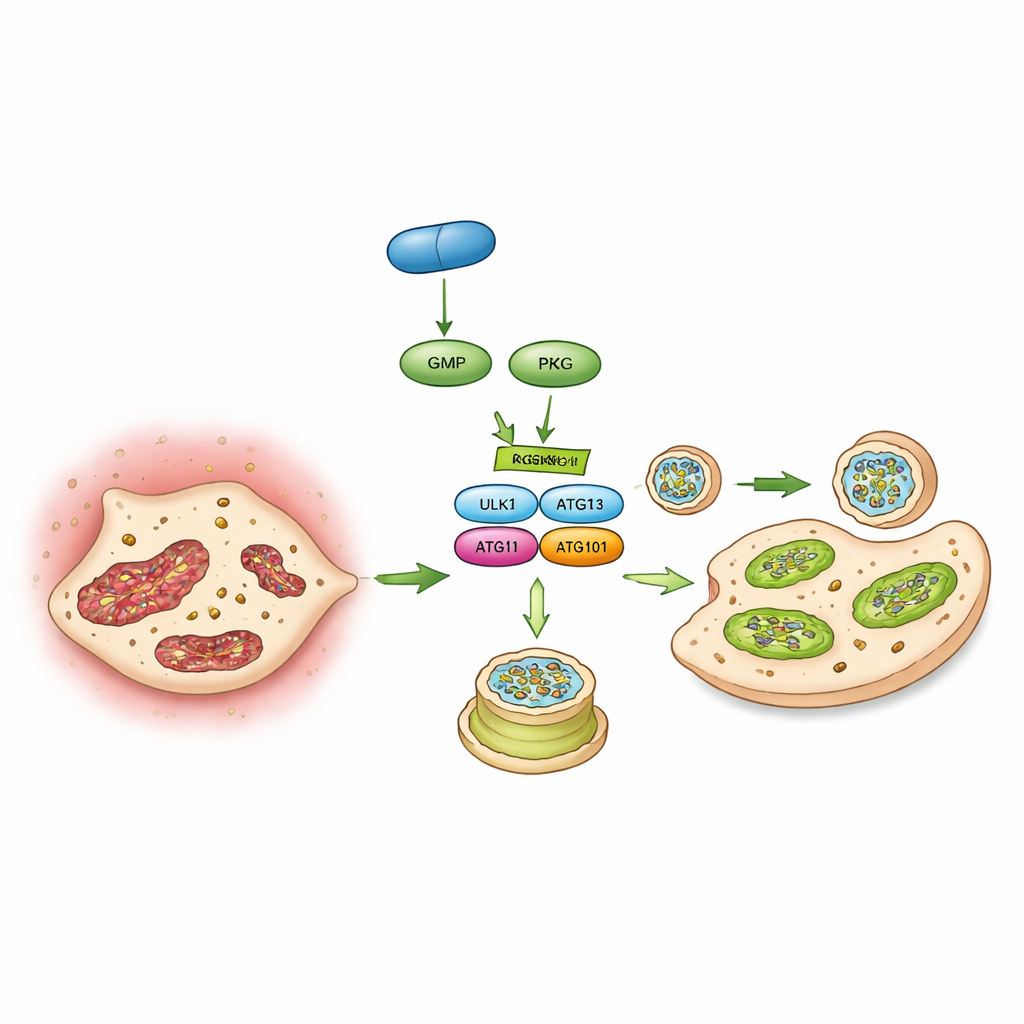
Att vända en molekylär strömbrytare
Slutligen identifierade författarna en specifik molekylär strömbrytare som kopplar PKG till autofagi: ett protein kallat ULK1 som sätter igång bildningen av autofagosomer. Genom fosfoproteomik, interaktionsstudier och kinastester i provrör visade de att PKG direkt fäster en fosfatgrupp på ULK1 vid en särskild plats (en aminosyra kallad serin 556). När denna plats muterades så att den inte längre kunde modifieras förlorade PKG förmågan att öka autofagin eller hämma förkalkningen i klaffceller. Hos möss eliminerade uttryck av denna icke‑responsiva ULK1‑mutant i klaffceller också vericiguats förmåga att skydda klaffen. Tillsammans skissar dessa fynd en händelsekedja: vericiguat stimulerar cGMP, vilket aktiverar PKG, som slår om ULK1‑brytaren, vilket återupplivar autofagin, bevarar mitokondrier och hindrar klaffceller från att omvandlas till benbildande celler.
Vad detta kan betyda för patienter
Denne studie placerar cGMP–PKG–ULK1–autofagi‑axeln som ett inneboende försvarssystem mot att aortaklaffen ”rostar”. Vid förkalkande klaffsjukdom är detta försvar försvagat, vilket tillåter cellerna att ackumulera skador och glida mot en benlik identitet. Genom att farmakologiskt återställa signalen med ett läkemedel som redan används i hjärtsviktsklinik gör forskarna förkalkningen långsammare i flera experimentella modeller. Fastän kliniska prövningar på människor med klaffsjukdom krävs erbjuder studien en tydlig och testbar idé: att noggrant stärka detta cellulära städsystem kan en dag fördröja eller minska behovet av klaffbytesoperation hos äldre med risk för aortastenos.
Citering: Wang, Y., Xu, F., Song, C. et al. Cyclic guanosine monophosphate-protein kinase G signaling attenuates aortic valve calcification through ULK1-mediated autophagy. Sig Transduct Target Ther 11, 90 (2026). https://doi.org/10.1038/s41392-026-02624-5
Nyckelord: förkalkande aortaklaffsjukdom, cGMP PKG‑signalering, vericiguat, autofagi, hjärtklaffsförkalkning