Clear Sky Science · sv
Glukokortikoider ökar känsligheten hos klarcelligt njurcellscarcinom för HIF-2α-hämmare genom att undertrycka H4K12-laktylering
Varför denna studie om njurcancer är viktig
Klarcellig njurcancer är den vanligaste och dödligaste formen av njurcancer, och många patienter får återfall eller svarar inte på befintliga läkemedel. Denna studie avslöjar en dold "beroende" i dessa tumörer: en särskild sätt att förbränna socker och använda spillprodukten laktat för att hålla cancergener aktiva. Ännu viktigare visar den att en välkänd läkemedelsgrupp—glukokortikoider, såsom dexametason—kan återanvändas för att försvaga detta beroende och göra ett nytt riktat läkemedel, HIF-2α-hämmaren belzutifan, mer effektivt.
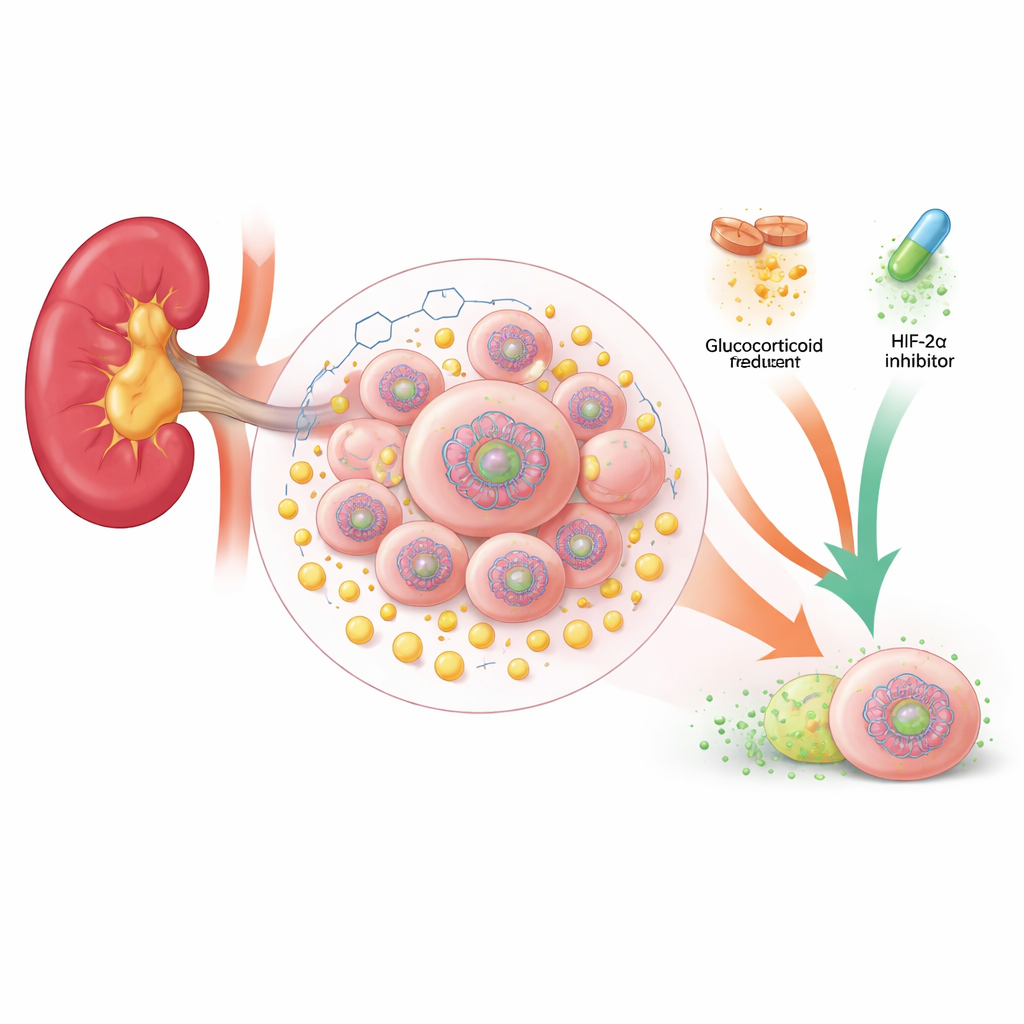
En sockerdriven slinga inne i njurtumörer
Många klarcelliga njurcancer förlorar en viktig skyddsgenen kallad VHL. Utan VHL beter sig cellerna som om de var syrebristiga även när de inte är det. De flyttar sin ämnesomsättning från effektiv energiproduktion i mitokondrier till en snabb och mindre effektiv process kallad glykolys, som ger energi och stora mängder laktat. Författarna fann att i njurtumörer utan VHL gör laktat mer än att bara ackumuleras som avfall: det tar sig in i cellkärnan och kemiskt märker de proteiner som paketerar DNA. Särskilt märket H4K12-laktylering var markant förhöjt i patienttumörer och kopplat till större, mer aggressiva cancerformer och sämre överlevnad.
Hur laktat hjälper cancergener att förbli aktiva
Genom att kartlägga var denna laktatbaserade märkning finns på DNA i cancerceller upptäckte teamet att den är kraftigt koncentrerad vid "på-knapparna" (promotorerna) för gener som driver tumörtillväxt och sockerförbränning. En framstående gen är PGK1, ett enzym som hjälper till att driva sockret genom glykolysen mot laktat. I VHL-bristfälliga celler och musemodeller betydde mer PGK1 mer laktat, vilket i sin tur gav mer H4K12-laktylering på PGK1 och andra tillväxtgener. Detta skapade en självförstärkande slinga: PGK1 ökar laktat; laktat pryder kromatin med H4K12-märket; det märket håller PGK1 och andra tumörfrämjande gener starkt aktiva och låser fast cancern i ett rigitt, högglykolytiskt tillstånd.
Att bryta slingan med befintliga läkemedel
Forskarna undrade sedan om några godkända läkemedel kunde dämpa denna laktat–kromatin-slinga. En screening av 2 468 FDA-godkända föreningar i njurcancerceller gav en överraskande träfflista: flera glukokortikoider minskade märkbart H4K12-signalen. Dexametason var mest potent och sänkte H4K12-laktyleringen även vid låga doser. Dessa hormoner verkar via glukokortikoidreceptorn, ett protein som flyttar in i kärnan och binder DNA när läkemedlet är närvarande. I cancerceller sammanföll glukokortikoidreceptorbindning vid promotorer för glykolysgener med förlust av H4K12-märket och minskad aktivitet hos PGK1 och andra sockerförbrännande gener. Som en följd producerade cellerna mindre laktat och återgick mot en mer normal, syreberoende metabolism.
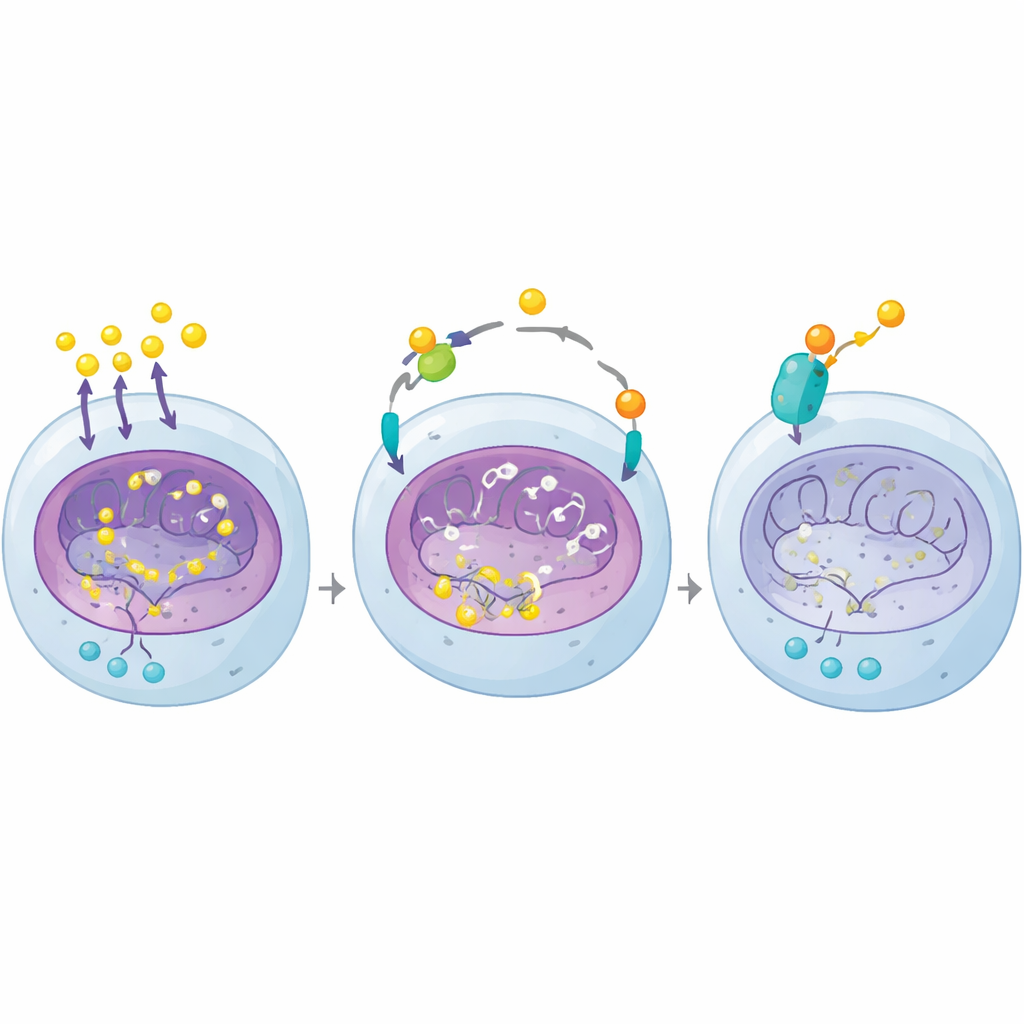
Att få ett riktat cancerläkemedel att fungera bättre
Belzutifan, en nyligen godkänd HIF-2α-hämmare, blockerar direkt en av de viktigaste downstream-effektorerna av VHL-förlust och har visat nytta hos patienter med avancerad klarcellig njurcancer. Svaren är dock ofullständiga och ofta kortvariga. Eftersom dexametason angriper cancerens laktatdrivna kromatinprogram ur en annan vinkel testade författarna de två läkemedlen tillsammans i musemodeller. I tumörer som växte från cellinjer och från patientvävnad krympte VHL-defektiga tumörer mycket mer av glukokortikoider plus belzutifan än av någon behandling ensam. Kombinationen minskade H4K12-laktylering och sänkte nivåerna av centrala glykolytiska och njurcellsrelaterade gener kopplade till tumörtillväxt, samtidigt som normal vävnad skonades i djurstudier.
Vad detta betyder för patienter och framtida behandlingar
Denna studie visar att många klarcelliga njurcancer är fast i en ond cirkel: ett VHL-defekt driver sockerhungrig metabolism som producerar laktat; det laktatet modifierar kromatinet kemiskt för att hålla samma tillväxt- och metabolismgener permanent aktiva. Studien visar att glukokortikoider, länge använda för sina antiinflammatoriska effekter, också kan fungera som riktade epigenetiska läkemedel som dämpar denna laktatdrivna slinga och gör tumörer känsligare för HIF-2α-blockad. Noggranna kliniska prövningar krävs naturligtvis—särskilt eftersom glukokortikoider kan dämpa immunsystemet—men fynden pekar mot en praktisk, mekanismbaserad kombinationsstrategi som kan göra befintliga riktade behandlingar mer effektiva för personer med denna svårbehandlade njurcancer.
Citering: Zhang, K., He, L., Wang, Y. et al. Glucocorticoids elevate clear cell renal cell carcinoma sensitivity to HIF-2α inhibitors by suppressing H4K12 lactylation. Sig Transduct Target Ther 11, 117 (2026). https://doi.org/10.1038/s41392-026-02622-7
Nyckelord: klarcelligt njurcellscarcinom, tumörmetabolism, histonlaktylering, glukokortikoider, HIF-2α-hämmaren belzutifan