Clear Sky Science · sv
Visinin-liknande protein 1 rubbar kalciumhomeostas och främjar förmaksflimmer i mänskliga och gnagarmodeller
Varför den här historien om hjärtrytmen är viktig
Förmaksflimmer är ett vanligt problem med hjärtrytmen som ökar risken för stroke och hjärtsvikt. Många lever med tillståndet, men läkare har fortfarande svårt att förebygga det eller förhindra återfall efter behandling. Denna studie avslöjar ett tidigare förbisett protein i hjärceller, kallat VILIP-1, som fungerar som en felaktig kalciumbrytare och bidrar till förmaksflimmer både hos människor och djur. Genom att identifiera denna brytare och visa att redan befintliga läkemedel kan dämpa dess effekt öppnar arbetet en ny väg mot säkrare, mer riktade terapier.
Närmare om ett kaotiskt hjärtslag
I ett friskt hjärta sprids elektriska vågor ordnat genom övre kamrarna, förmaken, och styr varje hjärtslag. Den ordningen är starkt beroende av kalcium, ett laddat mineral som strömmar in och ut ur hjärceller för att samordna kontraktion och avslappning. Vid förmaksflimmer blir den här kalciumtrafiken stökig: extra läckage och svängningar i kalciumnivåer ger upphov till vildfarna elektriska signaler som kan eskalera till snabba, oregelbundna rytmer. Läkare har länge vetat att felhantering av kalcium är central i detta tillstånd, men de utlösande mekanismerna högre upp i kedjan har varit dunkla.
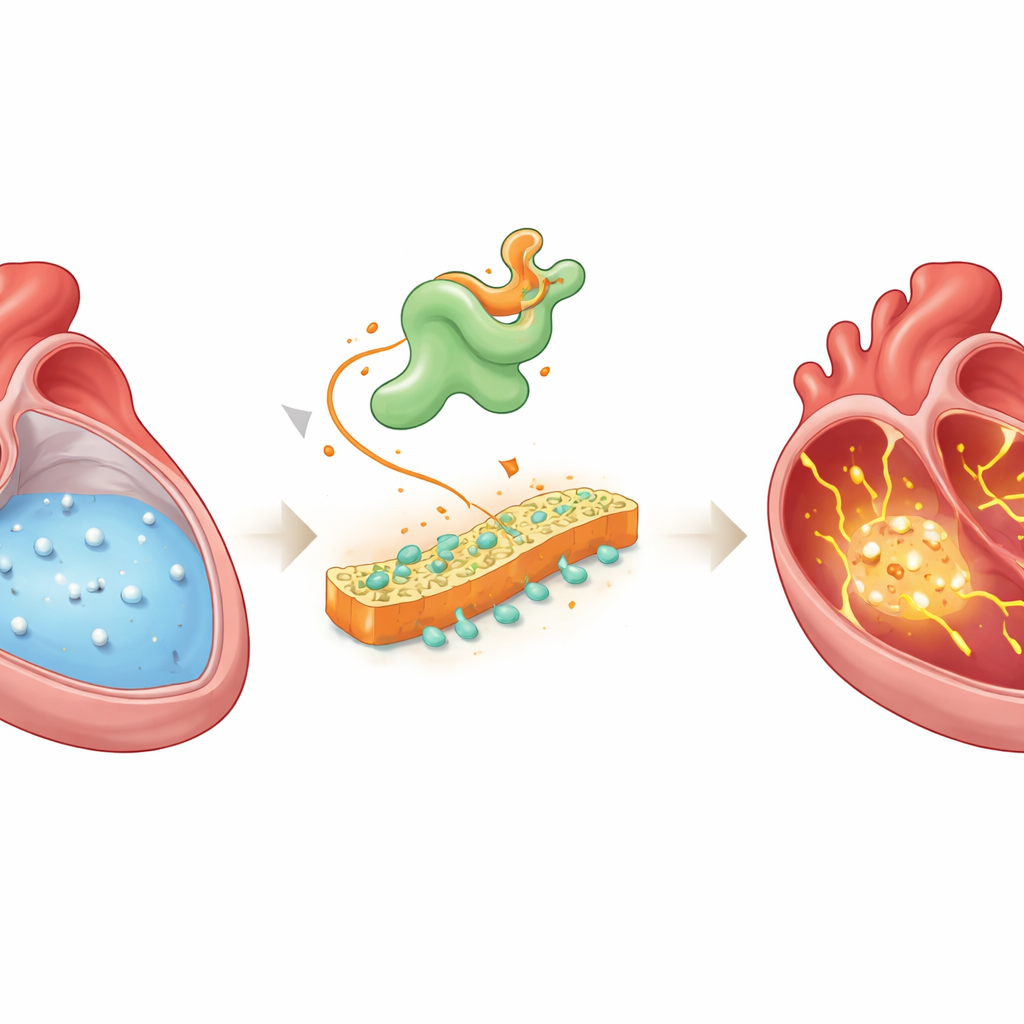
Upptäckten av en dold boven
Forskarna kombinerade flera avancerade metoder för att leta efter molekyler som kopplar störd kalciumhantering till förmaksflimmer. De spelade in kalciumsignaler från hundratals enskilda förmaksceller i råttor med pacing-inducerat förmaksflimmer och sekvenserade sedan hela uppsättningen aktiva gener i dessa samma celler. De jämförde också genaktivitet i förmaksvävnad från patienter med förmaksflimmer med vävnad från patienter med normal rytm. När de lade över dessa dataset och följde hur celler förändrades från friska till sjuka tillstånd framträdde en gen gång på gång: Vsnl1, som ger upphov till proteinet VILIP-1, ett kalciumkänsligt molekyl tidigare studerat mest i hjärna och bukspottkörtel, inte i hjärtat.
Hur VILIP-1 stör kalciumbalansen
I förmaksvävnad från både patienter och djurmodeller var nivåerna av VILIP-1 betydligt högre, och proteinet koncentrerades vid cellens yta. För att avgöra om denna förändring var en bihangare eller en drivare tvingade teamet förmaksceller i möss att producera extra VILIP-1. Dessa möss uppvisade inga uppenbara strukturella skador på hjärtat, men deras förmak blev mycket lättare att inducera till förmaksflimmer vid elektrisk pacing. Detaljerade elektriska inspelningar visade fler fördröjda efterdepolariseringar — onormala toppar efter varje slag — och växlingar i aktionspotentialens form från slag till slag, klassiska tecken på instabil elektrisk aktivitet kopplad till kalciumöverbelastning. Högupplöst kalciumavbildning bekräftade frekventa spontana kalciumvågor och uttömda interna kalciumförråd, vilket tyder på allvarliga läckage inne i cellerna.
Den avgörande partnern på cellytan
För att förstå hur VILIP-1 orsakar denna störning kartlade forskarna vilka proteiner som interagerar med det inne i hjärceller. Med två kompletterande metoder — att dra ner bindande partners från förmaksvävnad och att märka närliggande proteiner med en ”biotin-halo” i levande celler — kom de fram till NCX-1, den viktigaste natrium–kalcium-utbytaren i hjärtats yttre membran. Denna utbytare hjälper normalt till att föra ut kalcium i utbyte mot natrium, men under vissa förhållanden kan den arbeta i omvänd riktning och trycka kalcium in i cellen. Studien visade att VILIP-1 fysiskt binder NCX-1 och ökar antalet NCX-1-molekyler i membranet utan att öka den totala produktionen av NCX-1. Som följd blev utbytesströmmarna större, och blockering av NCX-1 med en selektiv hämmare minskade kalciumvågor och gjorde det svårare att framkalla förmaksflimmer i möss med överskott av VILIP-1.
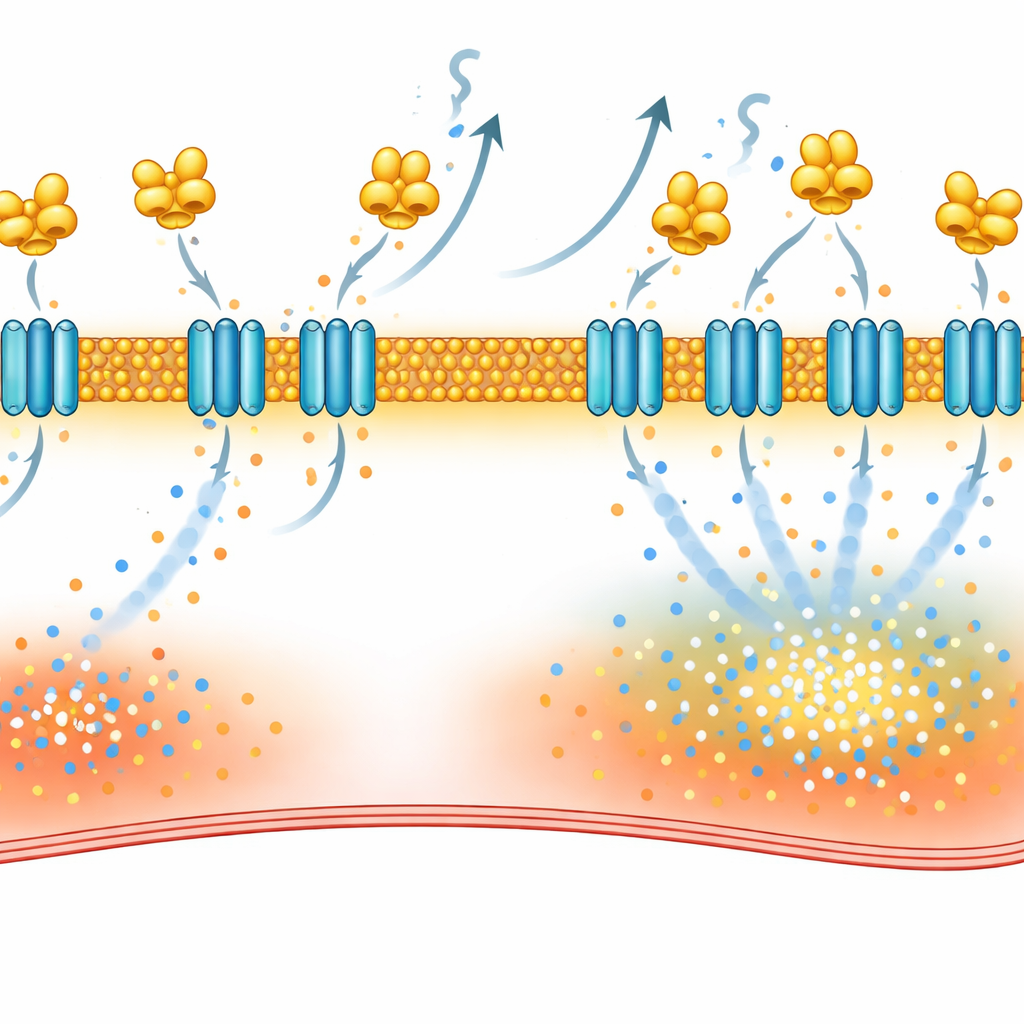
Stänga av den felaktiga brytaren med befintliga läkemedel
VILIP-1 fäster i membran via en fet tagg kallad myristat, vilken blir exponerad när kalcium binder proteinet. Teamet använde desloratadin, som tidigare visats störa detta märkningssteg, och fann att det sänkte NCX-1 vid cellytan, normaliserade utbytesströmmarna, minskade kalciumvågor och reducerade episoder av förmaksflimmer i råttmodeller. De testade också repaglinid, ett diabetesläkemedel känt för att binda närliggande kalciumsensorer. Biofysiska analyser bekräftade att repaglinid direkt binder till VILIP-1. I paced råttor och i förmaksvävnad från patienter med förmaksflimmer minskade repaglinidbehandling NCX-1 i membranet, lugnade kalciumläckaget i enskilda celler och minskade avsevärt hur lätt förmaksflimmer kunde inducera.
Vad detta betyder för människor med oregelbunden hjärtrytm
Sammanfattningsvis beskriver studien en självförstärkande loop: stigande kalciumnivåer rekryterar VILIP-1 till cellytan, där det ökar NCX-1, vilket i sin tur driver ytterligare kalciumöverbelastning och skapar förutsättningar för förmaksflimmer. Genom att bryta denna loop på nivån av VILIP-1 — antingen genom att blockera dess feta ankare eller genom att binda dess kalciumkännande kärna — kan befintliga läkemedel återställa en stabilare kalciumbalans och minska sårbarheten för arytmi i mänsklig och gnagarthjärnvävnad. Även om mer arbete behövs för att förfina läkemedelsspecificiteten och testa strategierna i större djurmodeller och kliniska prövningar framstår VILIP-1 nu som ett lovande nytt grepp för att förebygga och behandla denna utbredda och ofta svårbemästrade hjärtrytmstörning.
Citering: Xiong, K., Wang, G., Li, D. et al. Visinin-like protein 1 disrupts calcium homeostasis and promotes atrial fibrillation in human and rodent models. Sig Transduct Target Ther 11, 105 (2026). https://doi.org/10.1038/s41392-026-02615-6
Nyckelord: förmaksflimmer, kalciumsignalering, hjärtarytmi, natrium-kalcium-utbytare, terapeutiska mål