Clear Sky Science · sv
M6A-modifierad circArhgap26 dämpar hjärtats iskemi–reperfusionsskada genom att hämma palmitoylering av plakophilin-1
Varför det är viktigt att skydda hjärtat efter en hjärtattack
När en person drabbas av en hjärtattack skyndar läkarna för att återöppna den blockerade artären och återställa blodflödet. Detta räddar liv, men har också en baksida: den plötsliga återkomsten av blod kan skada hjärtat ytterligare — ett problem som kallas iskemi–reperfusionsskada. Den här sammanfattade studien undersöker en oväntad naturlig försvarare inne i hjärtcellerna — en cirkulär RNA-molekyl kallad circArhgap26 — som hjälper till att skydda hjärtmuskeln från denna sekundära våg av skada. Att förstå hur denna lilla molekyl fungerar kan peka mot nya behandlingar och blodprov för personer med hjärtsjukdom.
En dold cirkel i hjärtats genetiska manus
De flesta tänker på gener som raka DNA‑ och RNA‑strängar, men celler producerar också ringformade RNA‑molekyler, så kallade cirkulära RNA, som är ovanligt stabila och kan finjustera många cellulära processer. Forskarna sökte i mushjärtan efter cirkulära RNA som förändras vid hjärtskada och fokuserade på en, circArhgap26, vars nivåer föll kraftigt när blodflödet avbröts och sedan återställdes. De bekräftade att detta cirkulära RNA bildar en sluten loop, finns huvudsakligen i cellens vätskeomgivning och inte fungerar som mall för proteinsyntes. Istället verkar det fungera som en regulator som interagerar med andra molekyler för att påverka om en hjärtcell överlever eller dör efter stress. 
Bevis för att det cirkulära RNA skyddar hjärtat
För att se vad circArhgap26 faktiskt gör ökade eller minskade teamet dess nivåer i mushjärtan. När de använde ett virus för att höja circArhgap26 specifikt i hjärtmuskelceller hade djur som utsattes för en tillfällig blockering av en kranskärl följt av återställt blodflöde starkare hjärtpumpning, mindre skadade områden och färre döende celler. Klassiska markörer för skada i blod och hjärtvävnad var också lägre. Motsatsen gällde när det cirkulära RNA tystades: även utan en inducerad hjärtattack försämrades hjärtats funktion och celldöd ökade, och dessa problem blev värre när iskemi–reperfusion lades till. Liknande skyddande effekter observerades i humana hjärtliknande celler i laboratorium, vilket tyder på att mekanismen är bevarad mellan möss och människor.
En skadlig partnerprotein hålls i schack
Vid närmare analys frågade forskarna hur circArhgap26 utövar detta skydd. Med biokemiska fisketekniker fann de att det binder direkt till ett strukturellt protein kallat plakophilin‑1 (PKP1), som kan påverka hur starkt celler håller ihop och hur lätt de genomgår programmerad celldöd. I skadade hjärtan och stressade hjärtceller ökade PKP1-nivåerna och var kopplade till sämre skador. Att tysta PKP1 lindrade hjärtskada och celldöd, medan att tvinga fram dess produktion förvärrade utfallen. När circArhgap26 ökades föll mängden PKP1-protein trots att genaktiviteten inte förändrades, vilket pekar på en kontrollpunkt efter att RNA‑meddelandet har skapats. Experiment visade att circArhgap26 påskyndar nedbrytningen av PKP1‑proteinet genom att störa en fettmodifieringsprocess kallad palmitoylering som normalt stabiliserar PKP1.
Ett molekylärt dragkamp om dödssignaler
Palmitoylering utförs av en familj enzymer; en i synnerhet, ZDHHC1, fann man fäster fettsyragrupper på PKP1 och gör det mer långlivat. CircArhgap26 binder PKP1 på samma region som ZDHHC1 använder, vilket skapar en molekylär dragkamp. När det cirkulära RNA vinner får PKP1 färre fettmärken, blir mindre stabilt och rensas bort snabbare. Detta får en följdeffekt: PKP1 stärker normalt tillverkningen av ett annat protein, APAF1, genom att interagera med en kontrollsektion av dess RNA. APAF1 är en nyckelkomponent i maskineriet som aktiverar enzymerna caspase‑9 och caspase‑3, centrala verkställare av celldöd. Med mindre stabilt PKP1 minskar produktionen av APAF1‑protein, dödssignalernas kaskad dämpas och hjärtcellerna har större chans att överleva stressen från återställt blodflöde. 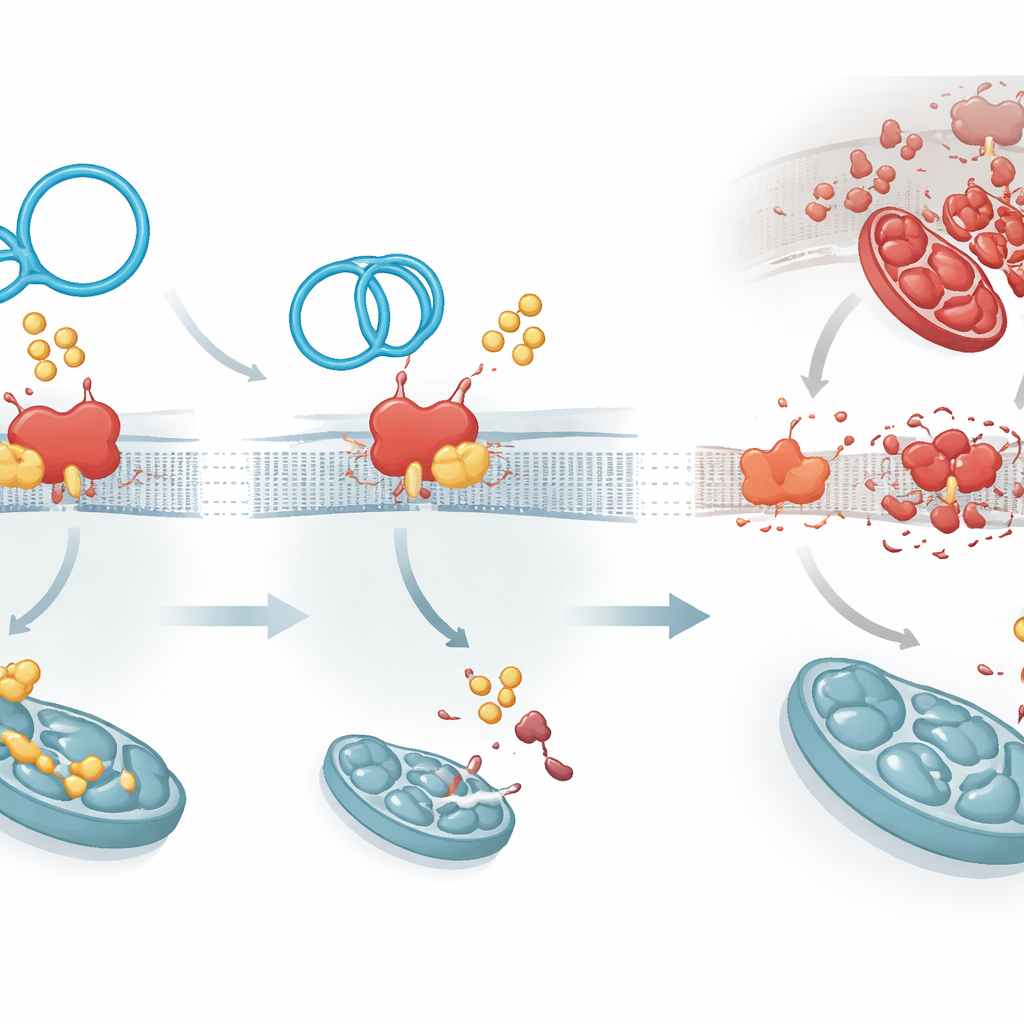
Finjustering av cirkeln och dess löfte för patienter
Studien visar också hur circArhgap26 själv skruvas ner under skada. En vanlig kemisk markering på RNA, kallad m6A, ackumuleras på detta cirkulära RNA i stressade hjärtan. Ett läsarprotein som heter YTHDF2 känner igen denna markering och främjar nedbrytningen av circArhgap26, vilket försvagar hjärtats naturliga försvar just när det behövs som mest. Viktigt är att den humana versionen av detta cirkulära RNA liknar musversionen mycket och är märkbart lägre i blodet hos patienter som genomgår artär‑öppnande ingrepp jämfört med friska frivilliga. Tillsammans tyder dessa fynd på att återställande eller efterliknande av circArhgap26 både skulle kunna fungera som en blodbaserad markör för risk och som en ny behandlingsprincip. Enkelt uttryckt avslöjar arbetet en liten cirkulär molekyl som fungerar som en väktare mot reperfusionsskador genom att oskadliggöra en dödlig kedjereaktion inne i hjärtceller.
Citering: Zhang, My., Ji, Dn., Qi, Wy. et al. M6A-modified circArhgap26 attenuates cardiac ischemia‒reperfusion injury by suppressing plakophilin-1 palmitoylation. Sig Transduct Target Ther 11, 99 (2026). https://doi.org/10.1038/s41392-026-02609-4
Nyckelord: iskemi reperfusionsskada, cirkulärt RNA, hjärtinfarkt, kardiomyocytapoptos, RNA-baserad terapi