Clear Sky Science · sv
Kemofototermisk synergi tänder antitumörimmunitet via ferroptos
Att omvandla kroppens värme och ljus till en cancerbekämpare
Kemoterapeutiska läkemedel kan krympa tumörer, men de ger ofta svåra biverkningar och stoppar inte alltid att cancern återkommer. Denna studie undersöker ett nytt sätt att få ett redan befintligt läkemedel, docetaxel, att verka hårdare och smartare genom att paketera det i små värmekänsliga partiklar och aktivera dem med nära‑infrarött ljus. Målet är inte bara att döda tumörceller mer precist, utan också att väcka immunsystemet så att det kan känna igen och jaga cancern i hela kroppen och förhindra framtida återfall. 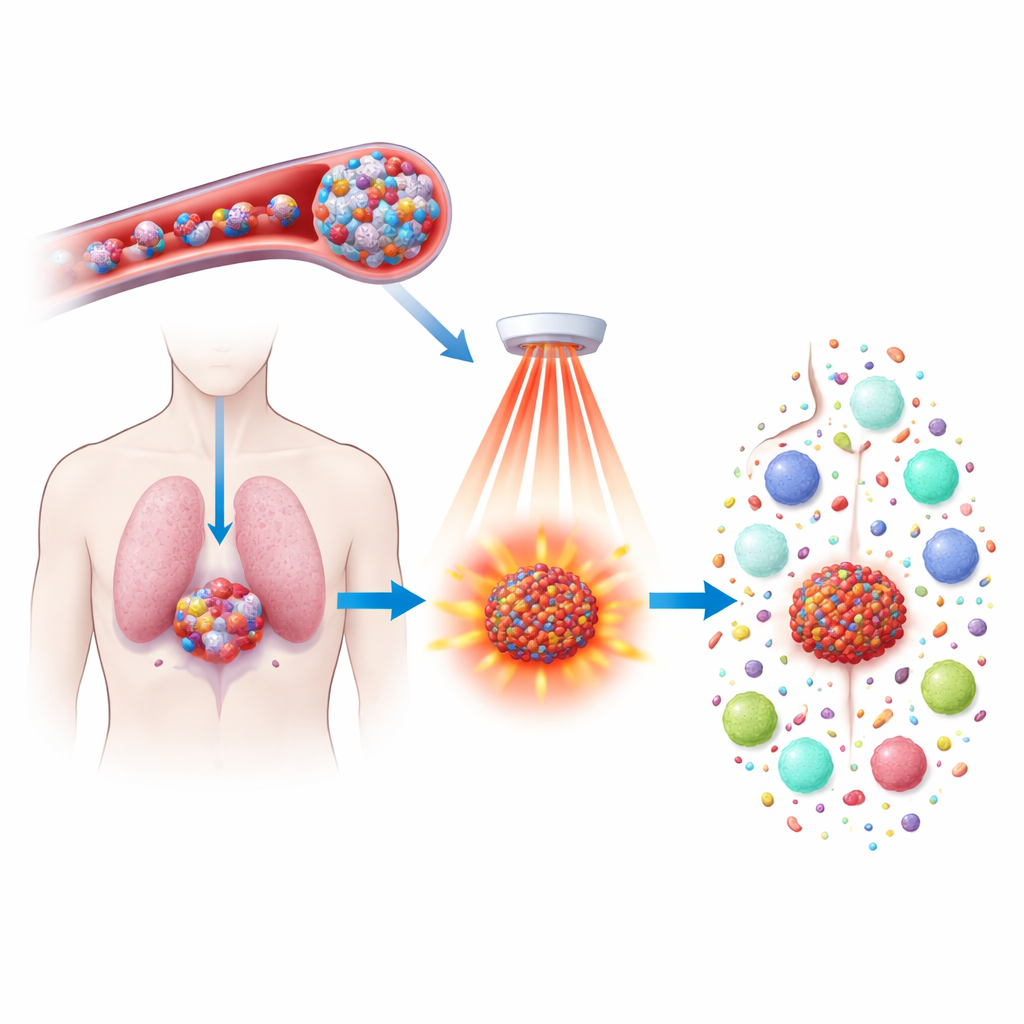
Mikroskopiska kurirer som vet vart de ska gå
Forskarna byggde en ny typ av nanopartikel av en polymer som innehåller ferrocene, en järnbärande molekyl som reagerar kraftigt med väteperoxid—en oxidant som finns i högre mängd i tumörer än i normalt vävnad. Dessa polymerer självsamlas till vattenvänliga sfärer som kan bära både docetaxel och ett ljupabsorberande färgämne kallat IR808. När de injiceras i blodomloppet är partiklarna tillräckligt små och stabila för att cirkulera och läcka in i tumörer, där de läckande blodkärlen och de höga väteperoxidhalterna börjar försvaga partiklarna och långsamt frigöra deras last. Denna design koncentrerar behandlingen i tumörer samtidigt som skada på friska organ begränsas.
Använda ljus för att förstärka lokal skada
Nära‑infrarött ljus, som säkert kan tränga igenom vävnad, riktas sedan mot tumörområdet. IR808 inuti nanopartiklarna absorberar detta ljus och omvandlar det till värme samtidigt som det genererar kemiskt reaktiva syreradikaler. Kombinationen av tumörproducerad väteperoxid och ljusdrivna oxidanter får partiklarna att falla sönder snabbare och släppa sin läkemedelslast precis där den behövs. Samtidigt hjälper järnet i ferrocene‑delen till att omvandla dessa oxidanter till särskilt aggressiva former som angriper de fettkomponenter som utgör cellmembran. Denna riktade kemiska och termiska assault ökar dödligheten markant jämfört med enbart docetaxel eller ljusbehandling. 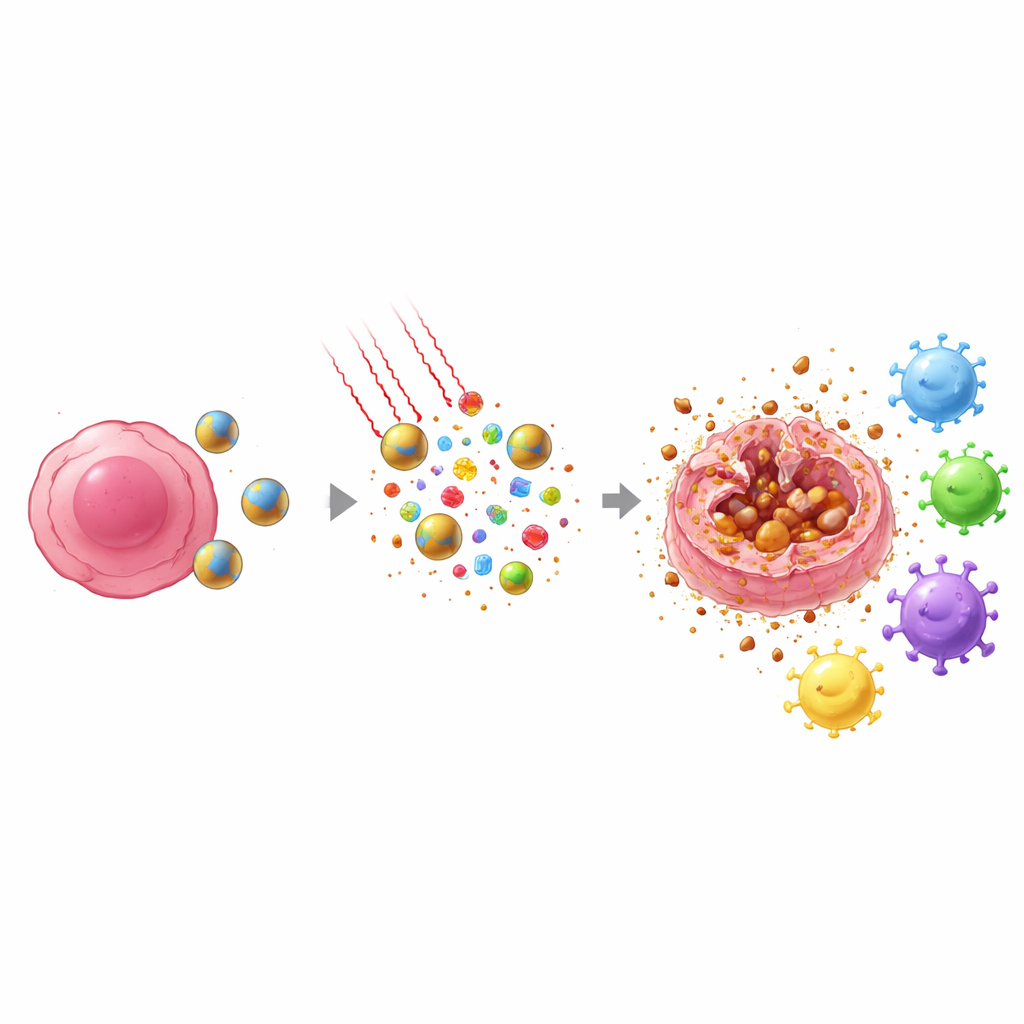
En kontrollerad bränning som signalerar till immunsystemet
Viktigt är att sättet tumörceller dör under denna behandling skiljer sig från vanlig kemoterapi. I stället för att tyst sönderfalla i prydliga fragment genomgår många celler en process som kallas ferroptos, en form av järn‑driven, lipid‑skadlig död där det yttre membranet brister. När det händer spills interna larm‑signaler och tumörspecifika fragment ut i omgivningen. Samtidigt trycker docetaxel ut ett viktigt kärnprotein, HMGB1, mot cellytan och förbereder det för frisättning. Tillsammans skapar värme, oxidanter och läkemedelseffekt en våg av fara‑ och antigen‑signaler som närliggande immunsensorer—dendritiska celler—kan upptäcka och föra vidare till lymfkörtlar.
Från lokal attack till helkroppsförsvar
I musmodeller för tumörer krympte denna kombinerade kemo‑fototermiska behandling inte bara de direkt uppvärmda tumörerna effektivare än någon enskild komponent, den förändrade också det immunologiska landskapet. Tumörerna visade fler mogna dendritiska celler och större antal cytotoxiska T‑celler, både i tumören själv och i de dränerande lymfkörtlarna. Hos vissa immun‑kompetenta möss försvann de primära tumörerna efter endast två behandlingscykler. När forskarna senare implanterade nya tumörer på avlägsna platser eller i motsatt flank, hämmdes eller undertrycktes dessa sekundära tillväxter, vilket tyder på att djuren utvecklat en form av cancerspecifikt immunminne. Tillägg av en checkpoint‑blockerande antikropp som förhindrar T‑cellsutmattning minskade ytterligare lungmetastaser och förlängde överlevnaden, vilket antyder att denna lokala behandling kan kombineras med moderna immunoterapier.
Varför detta är viktigt för framtidens cancervård
För en icke‑specialist är huvudpoängen att detta angreppssätt förvandlar docetaxel från ett grovt systemiskt gift till en del av en smart, flerstegs anti‑cancerstrategi. Genom att paketera läkemedlet i ljusaktiverade, järnhaltiga nanopartiklar som reagerar på tumörens egna kemi levererar terapin mer skada inne i tumörer samtidigt som frisk vävnad skonas. Det särskilda mönstret av celldöd som den utlöser fungerar som ett vaccin inifrån tumören och lär immunsystemet att känna igen och minnas cancern. Om dessa fynd kan översättas till människor kan sådana kemo‑fototermiska system hjälpa till att omvandla resistenta ”kalla” tumörer till ”heta” tumörer som svarar mycket bättre på immunbaserade behandlingar, potentiellt minska återfall och förbättra långsiktig kontroll.
Citering: Lin, J., Yang, H., Zou, Z. et al. Chemo-photothermal synergy ignites antitumor immunity via ferroptosis. Sig Transduct Target Ther 11, 98 (2026). https://doi.org/10.1038/s41392-026-02608-5
Nyckelord: cancernanomedicin, fototermisk terapi, ferroptos, cancerimmunterapi, docetaxelleverans