Clear Sky Science · sv
Frigöra potentialen i bimetalliska nanobomber som medierar STING‑vägen för att förbättra bispecifika T‑cellsengagerare mot fototerapi‑immunterapi för kolorektal cancer
Vända immunförsvaret mot koloncancer
Kolon‑ och rektalcancer är vanligt förekommande och ofta dödliga, delvis därför att tumörer lär sig gömma sig för immunförsvaret. Denna studie undersöker en ny strategi som packar flera cancerbekämpande funktioner i en enda liten ”nanobomb” för att väcka kroppens försvar, hjälpa immunceller att hitta tumören och förhindra att cancern återkommer eller sprider sig.
Varför dagens immundroger behöver förbättras
En lovande klass av cancerläkemedel, kallade bispecifika T‑cellsengagerare, fungerar som biologiska matchmakers: ena änden fångar upp en T‑cell (en central immuncell) och den andra fäster vid en markör på en tumörcell, vilket tvingar dem samman så att T‑cellen kan döda. Även om de är kraftfulla vid blodcancer har dessa läkemedel svårt att fungera i solida tumörer som kolorektal cancer. De elimineras snabbt från kroppen, kan angripa friska vävnader som delar samma markör och stöter ofta på ”kalla” tumörer som saknar tillräckligt med immunceller för att behandlingen ska fungera. Läkare och forskare letar därför efter sätt att leverera dessa läkemedel säkrare och att förvandla kalla tumörer till ”heta” tumörer fulla av aktiva immunceller.
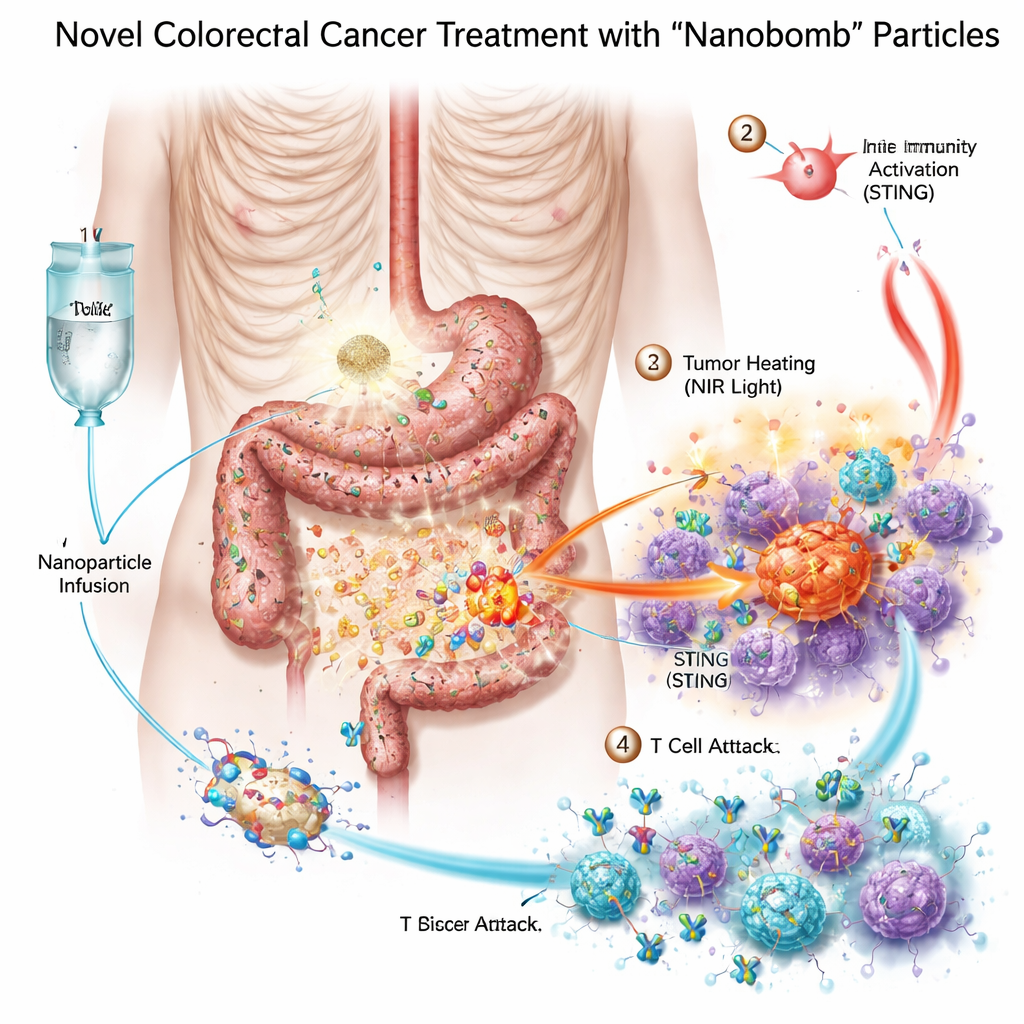
Packa tre vapen i en liten ”nanobomb”
Forskarna konstruerade en bimetallisk nanobomb — vetenskapligt benämnd MnO2/Co‑DA@BiTE/HPT — som kombinerar tre behandlingssätt i en och samma partikel. För det första innehåller kärnan mangan och kobolt, metaller som kan aktivera ett cellulärt larmsystem kallat STING‑vägen, vilket hjälper kroppen att uppfatta fara och kalla på immunceller. För det andra är partikelns yta belagd med en bispecifik T‑cellsengagerare som förbinder T‑celler med cancerceller. För det tredje absorberar materialet nära‑infrarött ljus, vilket gör det möjligt för läkare att värma tumören från utsidan i en form av fototermisk terapi. För att säkerställa att nanobomberna söker sig till kolorektala cancerceller tillsatte teamet en kort DNA‑sekvens, en aptamer, som känner igen PD‑L1, ett vanligt förekommande molekylärt kännetecken på dessa tumörer. När partiklarna når tumören hjälper naturliga enzymer i tumörvävnaden till att bryta ned dem och frigöra deras last precis där den behövs.
Värma upp, larma och rekrytera immens armé
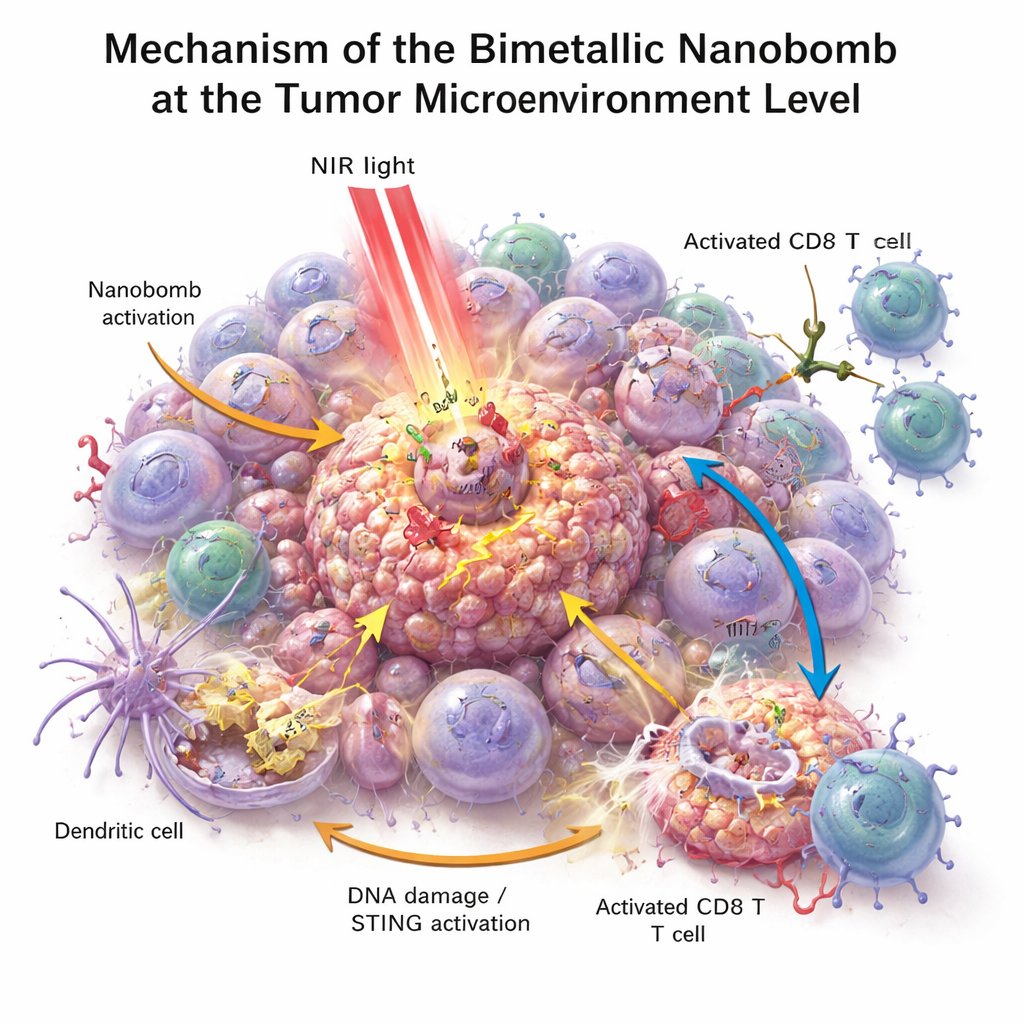
I laboratoriediskar dödade nanobomberna kolorektala cancerceller mer effektivt än någon enskild komponent för sig. När partiklarna belystes med nära‑infrarött ljus värmdes de upp, stressade och skadade cancercellerna och bidrog till att generera reaktiva syreföreningar — mycket reaktiva molekyler som ytterligare skadar tumörceller. Denna stress bröt ner cellernas DNA och drev dem in i en särskilt tydlig form av celldöd som sänder ut ”faran”‑signaler. Närliggande immunceller, särskilt dendritiska celler, tog upp det döende tumörmaterialet och aktiverade STING‑vägen med hjälp av det frigjorda manganet och koboltet. De producerade då interferoner och andra inflammatoriska budbärare som mognar och attraherar T‑celler. Samtidigt kopplade den bispecifika engageraren på nanobomben fysiskt T‑celler till PD‑L1‑positiva tumörceller, vilket förbättrade T‑cellsaktivering och tumördöd även i tidigare kalla tumörer.
Från tumörinvolution till bestående immunminne
I flera musmodeller — inklusive subkutana kolorektala tumörer, tumörer på båda sidor av kroppen, lungmetastaser och en modell för återfall efter operation — bromsade nanobomberna tillsammans med ljus tumorutvecklingen kraftigt eller stoppade den nästan helt. Behandlade tumörer innehöll avsevärt fler cancer‑dödande CD8‑T‑celler och färre regulatoriska T‑celler som normalt dämpar immunsvaret. Dendritiska celler i tumörer och lymfkörtlar visade tecken på mognad, och blodprover avslöjade förhöjda nivåer av immunstimulerande cytokiner. Viktigt var att möss som rensade sina tumörer efter nanobombehandlingen hade bättre skydd när cancern återintroducerades, och de utvecklade färre lungmetastaser, vilket visar att terapin hjälpte till att bygga ett långvarigt immunminne snarare än bara att orsaka engångsminskning av tumörer.
Vad detta kan betyda för framtidens cancervård
Detta arbete introducerar en ”triple‑hit” nanomedicin som värmer tumörer, aktiverar ett internt larm och styr T‑celler direkt till cancerceller, allt i en enda riktad partikel. I musmodeller förvandlade denna strategi inte bara kalla kolorektala tumörer till varma, inflammerade sådana utan hjälpte också till att förhindra återfall och spridning. Även om tekniken fortfarande ligger långt från klinisk användning — uppskalning, långtidssäkerhet och prövningar på människor återstår som stora utmaningar — erbjuder den en ritning för framtida behandlingar som förenar smarta material med immunläkemedel för att ge patienter ett starkare och mer hållbart antitumörsvar.
Citering: Mu, M., Li, H., Chen, B. et al. Unleashing the potential of bimetallic nanobomb-mediated STING pathway to enhance bispecific T-cell engager against colorectal cancer photo-immunotherapy. Sig Transduct Target Ther 11, 80 (2026). https://doi.org/10.1038/s41392-026-02596-6
Nyckelord: kolorektal cancer, immunterapi, nanopartiklar, STING‑vägen, bispecifik T‑cellsengagerare