Clear Sky Science · sv
Personligt farmakokinetik–farmakodynamikstyrd terapi via en iPSC‑deriverad multi‑organoidplattform vid NF1‑mutant bröstcancer
Varför denna forskning är viktig för patienter
Många som har cancer får läkemedel som fungerar bra för vissa patienter men inte för andra, och som ofta ger svåra biverkningar. Denna studie beskriver ett nytt sätt att testa cancerbehandlingar utanför kroppen med hjälp av labbodlade mini‑organ skapade från en patients egna celler. Arbetet fokuserar på en svårbehandlad form av bröstcancer som drivs av förändringar i genen NF1 och visar hur en kombination av en genkorrigerande strategi och ett målinriktat läkemedel kan leda till säkrare, mer effektiva och verkligt personliga behandlingar.
Att bygga en mini‑version av patientens kropp
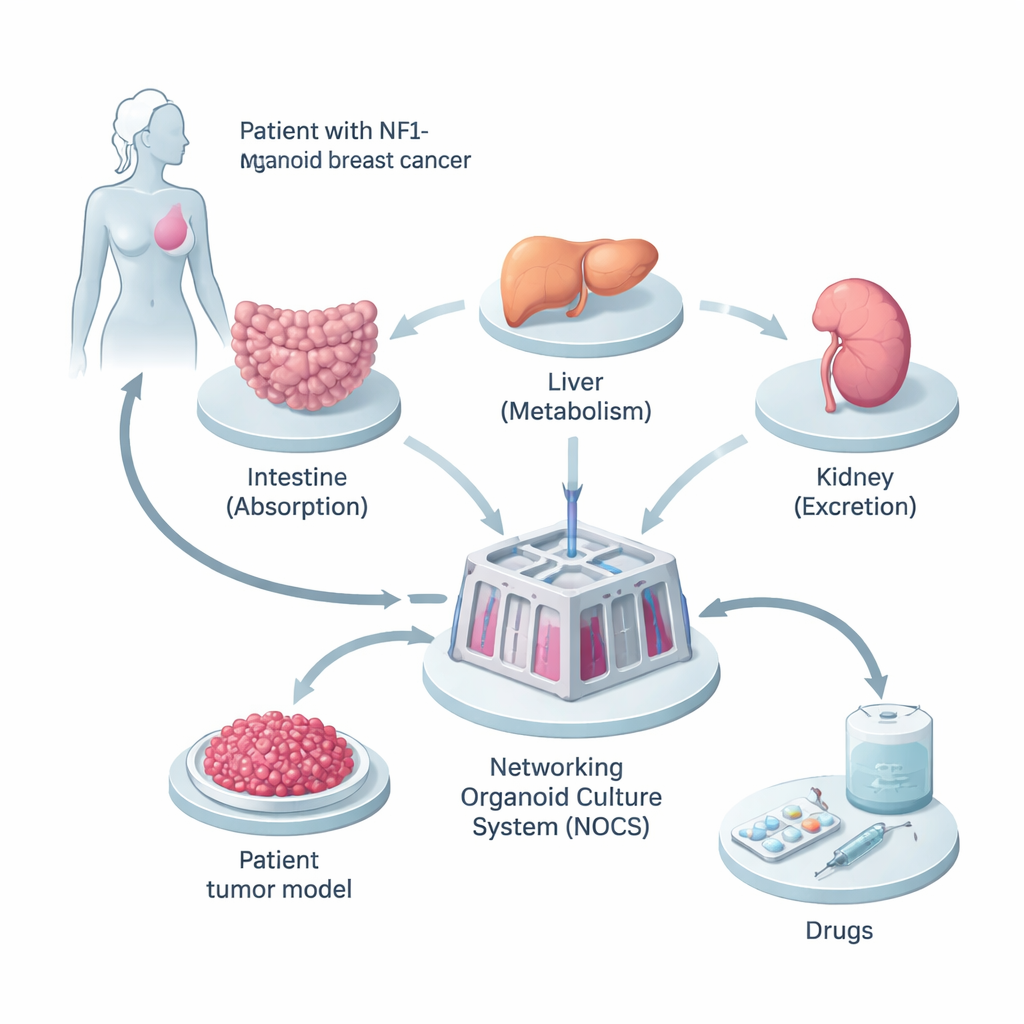
Forskarna började med vävnad från en kvinna vars bröstcancer bar på en ärftlig mutation i NF1‑genen. De omprogrammerade hennes normala hudliknande celler till inducerade pluripotenta stamceller, som kan bli nästan vilken celltyp som helst i kroppen. Från dessa odlade de tre typer av mini‑organ—tunntarm, lever och njure—eftersom dessa är nyckelplatser där läkemedel tas upp, bearbetas och utsöndras. Parallellt skapade de tredimensionella tumörspheroider från hennes cancerceller, och bevarade den blandning av celltyper och genetiska förändringar som fanns i den ursprungliga tumören.
En levande krets för läkemedelstestning
För att få dessa mini‑organ att bete sig mer som en riktig kropp kopplade teamet ihop dem i en vätskefylld enhet kallad Networking Organoid Culture System, eller NOCS. I denna uppsättning flödar ett medium mellan tunntarms-, lever‑, njur‑ och tumörkompartimenten och efterliknar blodcirkulationen. Läkemedel kan tillföras på ett sätt som liknar att svälja en tablett eller få en injektion, och sensorer och pumpar styr hur snabbt ”blodet” rör sig och hur ofta det förnyas. Detta gjorde det möjligt för forskarna att följa hur mycket läkemedel som tas upp, hur snabbt det bryts ner och hur starkt det verkar på tumören—allt i en patient‑specifik, människobaserad modell.
Att laga en trasig gen med exon‑skipping
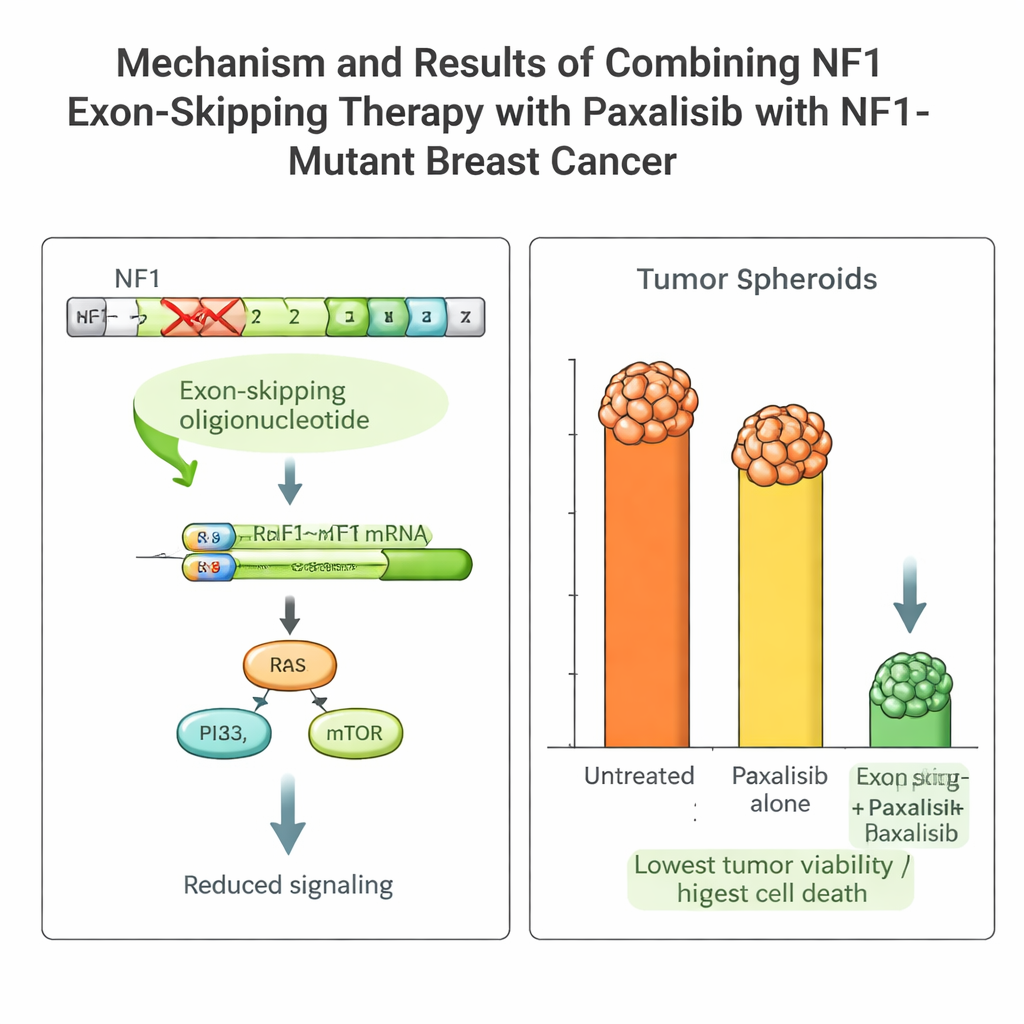
Patientens tumör bar på en skadlig NF1‑mutation som håller tillväxtsignalerna aktiva och gör många standardläkemedel ineffektiva. Teamet designade korta bitar av genetiskt material, så kallade antisens‑oligonukleotider, för att få cellens RNA‑bearbetningsmaskineri att hoppa över den felaktiga delen (exon 2) av NF1‑genen. Med hjälp av ett virusbaserat leveranssystem som verkar under flera dagar inducerade de stabil ”exon skipping” i patientens cancerceller. Detta gav ett kortare men funktionellt NF1‑protein, dämpade de överaktiva tillväxtsignalerna och gjorde tumörcellerna mer känsliga för behandling.
Att välja rätt målinriktat läkemedel med PK/PD‑vägledning
Med denna plattform jämförde teamet flera avancerade läkemedel som blockerar PI3K–mTOR‑vägen, vilken ligger nedströms om NF1. De mätte farmakokinetik (hur kroppen hanterar läkemedlet) och farmakodynamik (hur läkemedlet påverkar tumören) både i möss och i NOCS. Ett läkemedel, Paxalisib, stack ut: det absorberades väl i tarmen, hölls kvar i systemet på användbara nivåer och visade liknande beteende i djur och i organoidenheten. När det kombinerades med NF1 exon‑skipping ökade Paxalisibs cytotoxiska effekt mot patientens tumörceller dramatiskt, med kraftiga minskningar i tillväxt och tydliga tecken på programmerad celldöd, både i NOCS och i möss som bar patientens tumör.
Att väga nytta mot risk över organ
Eftersom tunntarms‑, lever‑ och njurmodellerna var del av samma krets kunde forskarna också iaktta tidiga tecken på organskada. Paxalisib orsakade stressreaktioner och subtil försvagning av barriären i tarm‑ och njurmodellerna samt tecken på påfrestning i levern, men utan större förlust av cellviabilitet vid den testade dosen. Denna typ av helkroppssyn, med mänsklig vävnad, ger ett sätt att jämföra behandlingsalternativ inte bara utifrån hur väl de krymper tumörer, utan också utifrån hur de kan påverka friska organ innan ett läkemedel någonsin når en patient.
Vad detta kan betyda för framtida cancerbehandling
Enkelt uttryckt visar denna studie att det nu är möjligt att odla en förenklad, patient‑specifik ”mini‑kropp på en chip” som kan testa hur olika läkemedel—och till och med genkorrigerande tillvägagångssätt—kommer att bete sig och samspela. För denna patient med NF1‑mutant bröstcancer var den optimala strategin en kombination av NF1 exon‑skipping‑terapi och det orala läkemedlet Paxalisib, som tillsammans bromsade tumörtillväxten mycket mer än någon av åtgärderna ensam. Om dessa plattformar utvecklas vidare och testas på fler patienter kan de hjälpa läkare att välja behandlingsplaner anpassade till varje persons gener och biologi, vilket ökar chanserna till framgång samtidigt som onödig toxicitet minskas.
Citering: Lim, J.H., Mun, S.J., Kang, H.M. et al. Personalized pharmacokinetic–pharmacodynamic guided therapy via an induced pluripotent stem cell–derived multi-organoid platform in NF1-mutant breast cancer. Sig Transduct Target Ther 11, 79 (2026). https://doi.org/10.1038/s41392-026-02595-7
Nyckelord: personlig onkologi, bröstcancer, organoider, NF1‑mutation, målinriktad terapi