Clear Sky Science · sv
Att utnyttja lipiddrivna immunometabola vägar i omentala metastaser för att förbättra immunterapi hos patienter med äggstockscancer
Varför fettet runt buken spelar roll för äggstockscancer
Äggstockscancer sprider sig ofta till ett fettlager i buken som kallas omentum. Detta område är rikt på fettceller och immunceller, och visar sig vara mycket mer än en passiv åskådare. Studien som sammanfattas här visar att hur immunceller använder och hanterar fett i dessa omentala avlagringar kan bidra till att förklara varför endast en liten andel patienter har nytta av moderna immunterapier. Den pekar också på nya läkemedelskombinationer och bilddiagnostiska tester som skulle kunna få dessa behandlingar att fungera för fler människor.
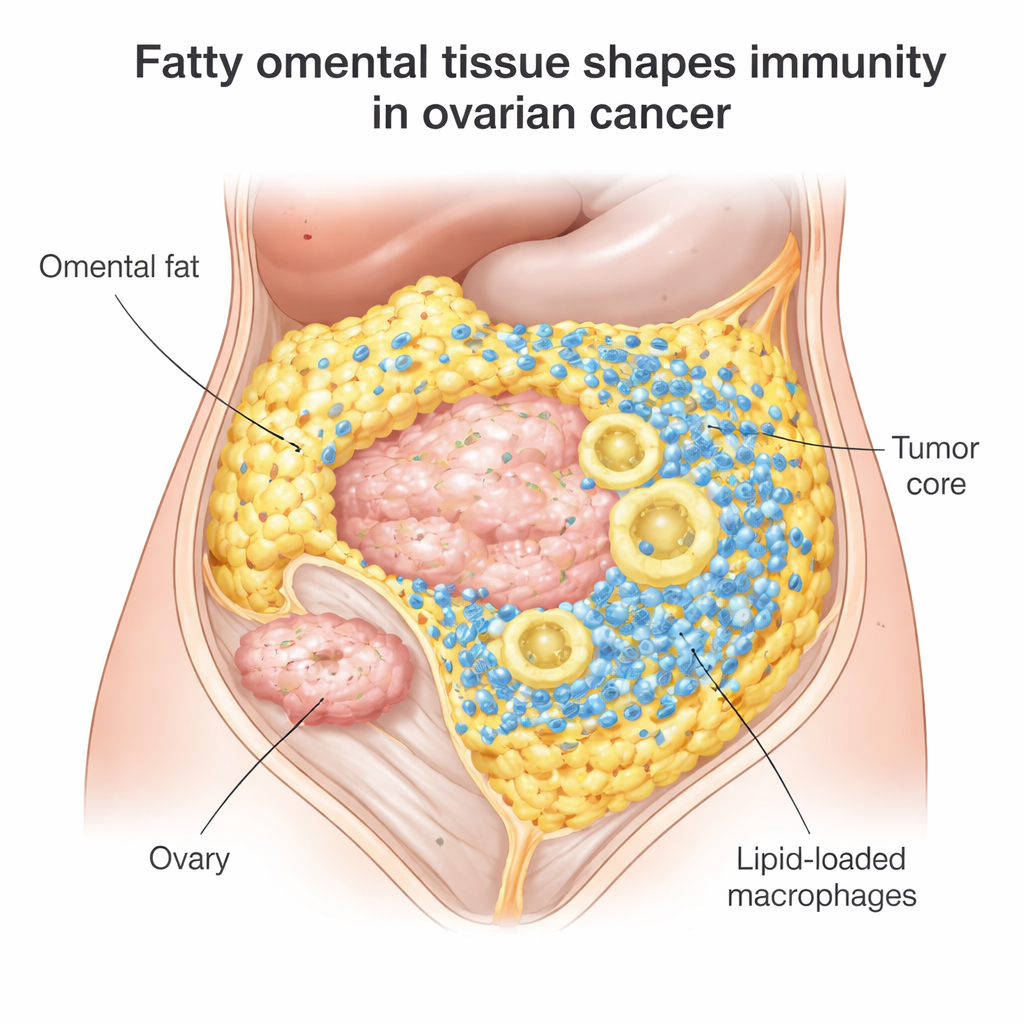
En dold stridszon i bukfettet
De flesta kvinnor med epitelial äggstockscancer svarar initialt på kirurgi och cytostatikabehandling, men 70–80 % får återfall och immuncheckpoint-läkemedel som nivolumab eller pembrolizumab hjälper bara cirka 10–15 %. Forskarna fokuserade på omentala metastaser, en vanlig plats där äggstockscancer sätter sig bland fettcellerna. När de undersökte mer än 100 tumörprover fann de att omentala tumörer var fyllda med immunceller: mördande T-celler som kan angripa cancer och stora städande celler kallade makrofager. Men det fanns en hake. Dessa T‑celler tenderade att klustra vid gränsen där tumör möter fett, istället för att tränga in i tumörens kärna där de behövs som mest.
Fett som gynnar vissa immunceller men överväldigar andra
När de gick djupare visade forskarna att T‑celler i dessa fettiga tumörer anpassar sig till den lokala miljön genom att ta upp lipider, eller fetter, från närliggande fettceller. Det verkar hålla dem metabolt ”välmående”: deras genaktivitet och laboratorietester visade att de kunde känna igen och döda patientens egna tumörceller. Samtidigt var många tumörassocierade makrofager i omentum kraftigt laddade med fettkroppar. Dessa lipidfyllda makrofager visade tecken på hög oxidativ stress — kemiskt slitage kopplat till reaktiva syreföreningar — och skiftade mot ett immunsuppressivt, tumörfrämjande tillstånd. Med andra ord, samma fattsrika miljö som kan gynna effektiva T‑celler pressar också makrofagerna in i ett skadligt läge som dämpar den övergripande immunattacken.
Omprogrammera övermätta makrofager med befintliga läkemedel
Forskarna frågade sig sedan om de kunde vända dessa stressade makrofager tillbaka till allierade. Med hjälp av färska tumörfragment odlade i labb testade de två angreppssätt. Det ena involverade maraviroc, ett HIV-läkemedel som blockerar CCR5, en receptor för immunsignalen CCL5 som är riklig vid tumör–fett‑gränsen. Det andra blockerade CD36, en viktig ”städar”-receptor som tillåter makrofager att importera fettsyror. Båda behandlingarna minskade fettmängden inne i makrofagerna, sänkte markörer för oxidativ stress och skadlig lipidperoxidation, och frigjorde vågor av inflammatoriska signaler. Avgörande var att de gjorde det möjligt för mördande T‑celler att föröka sig och röra sig från det feta skiktet in i tumörkärnan, vilket ökade den lokala immuaktiviteten utan att tillföra några extra immunceller utifrån.
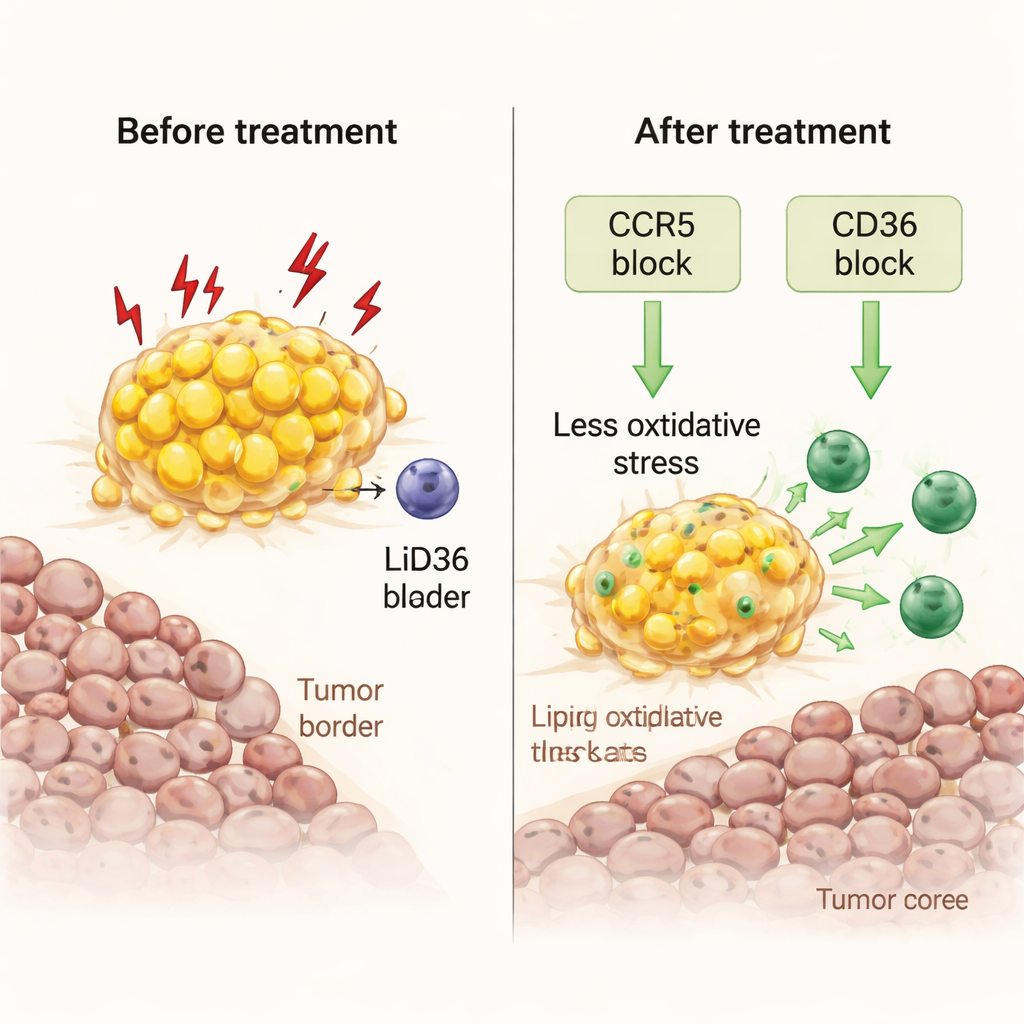
Från cellvägar till verkliga modeller och patienter
För att pröva dessa idéer i en mer realistisk miljö använde teamet humaniserade möss som var konstruerade för att ha ett människoliknande immunsystem och implanterade dem med mänsklig bröstcancer i fettfattig vävnad. Maraviroc-behandling omprogrammerade mänskliga makrofager i dessa djur på ett sätt som speglade patient‑proverna: minskade lipid‑ och stresssignaturer, ökad cytokinproduktion och starkare stöd för T‑cellrelaterade vägar. Kliniskt gick forskarna tillbaka till en japansk studie av nivolumab för kemoterapiresistent äggstockscancer. Varje patient som hade nytta av läkemedlet hade omentala metastaser synliga i operationsproverna. Genom att använda CT- eller MRT‑skanningar kombinerade med maskininlärningsanalys av kroppsfördelning av fett byggde de ett beslutsträd som icke-invasivt kunde flagga patienter vars tumörer sannolikt sitter nära visceralt fett — och i ett prospektivt fall förutsåg denna metod korrekt en patient som senare svarade på nivolumab.
Vad detta kan betyda för framtida behandling
För en icke-specialist är budskapet att ”var” äggstockscancer växer i kroppen, och hur närliggande fett omformar immunceller, kan starkt påverka om immunterapi fungerar. Fettfyllda omentala avlagringar verkar hysa livskraftiga T‑celler men också övermatade, stressade makrofager som dämpar angreppet. Genom att lätta på lipidbördan i dessa makrofager och minska deras oxidativa stress — med CCR5‑blockerare som maraviroc, CD36‑riktade medel eller relaterade strategier — kan det bli möjligt att omvandla ett delvis blockerat immunsvar till ett fullskaligt angrepp på tumören. Samtidigt kan bilddiagnostiska mått på omentalt engagemang hjälpa läkare att välja vilka patienter som mest sannolikt gynnas av immuncheckpoint‑läkemedel, vilket ger en mer personlig och potentiellt mer effektiv strategi för att behandla äggstockscancer.
Citering: Suarez-Carmona, M., Hampel, M., Zhang, XW. et al. Harnessing lipid-driven immunometabolic pathways in omental metastases to enhance immunotherapy in patients with ovarian cancer. Sig Transduct Target Ther 11, 78 (2026). https://doi.org/10.1038/s41392-026-02594-8
Nyckelord: äggstockscancer, omentumfett, immunterapi, tumörassocierade makrofager, lipidmetabolism