Clear Sky Science · sv
GPR54 reglerar utvecklingen av icke-småcellig lungcancer via dopa-dekarboxylas
Varför den här lungcancerhistorien är viktig
Lungcancer är fortfarande en av de dödligaste cancerformerna, och de flesta fall utgörs av en typ som kallas icke-småcellig lungcancer (NSCLC). Många patienter får så småningom slut på effektiva behandlingsalternativ eftersom tumörer anpassar sig eller blir resistenta mot dagens läkemedel. Denna studie avslöjar ett tidigare underskattat kontrollsystem inne i lungcancerceller, centrerat kring en receptor kallad GPR54 och ett enzym kallat dopa-dekarboxylas (DDC). Genom att förstå hur dessa molekyler hjälper tumörer att växa och driva sin metabolism pekar forskarna på nya sätt att bromsa eller till och med krympa NSCLC.
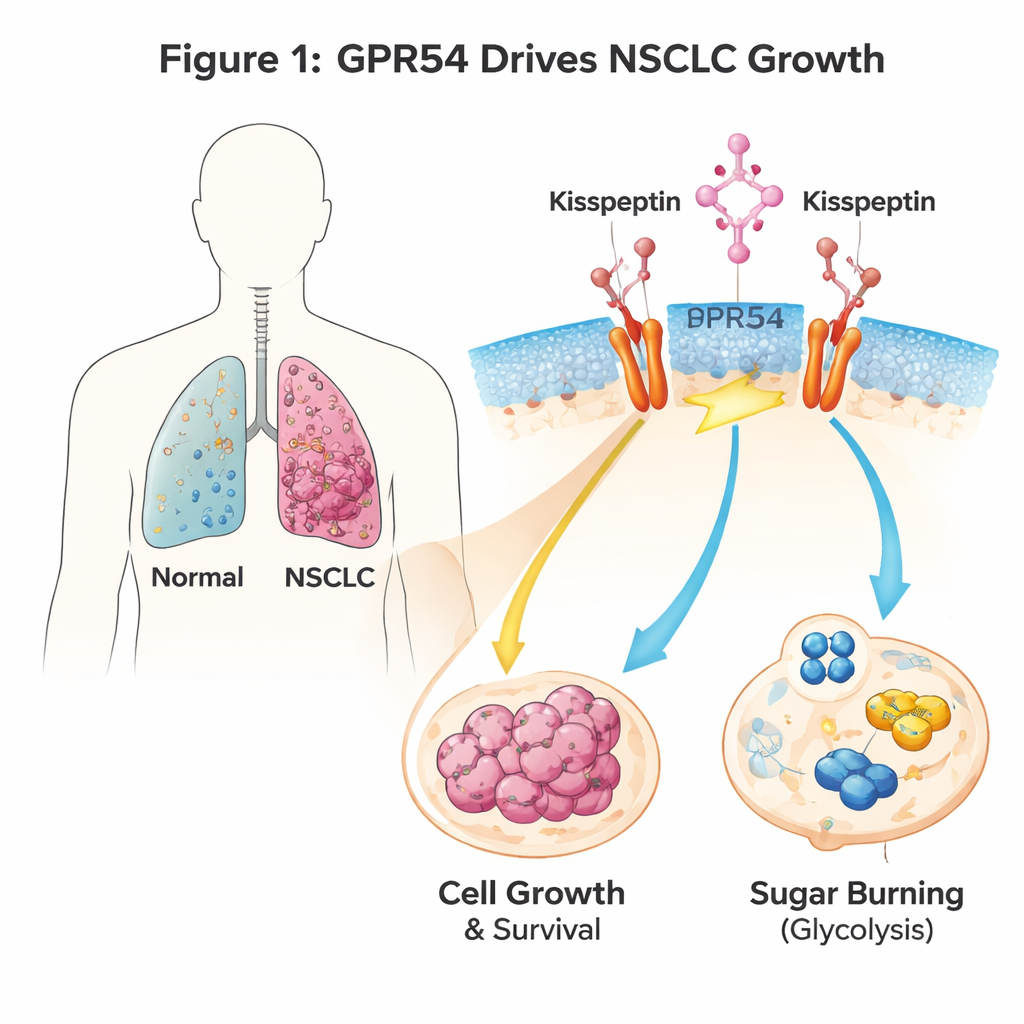
En signalswitch på lungcancerceller
GPR54 är en sensor som sitter på cellernas yta och reagerar på en naturlig signal kallad kisspeptin. Den är mest känd för roller i pubertet och reproduktion, men förekommer också i många cancerformer. Författarna använde genetiskt modifierade möss som utvecklar NSCLC när en cancerskapande gen kallad Kras aktiveras i lungceller. När de tog bort Gpr54-genen i dessa möss levde djuren längre, utvecklade färre och mindre lungtumörer, och deras cancerceller visade tydliga tecken på självdöd (apoptos). Mänskliga NSCLC-cellinjer berättade samma historia: när GPR54-nivåerna sänktes växte tumörcellerna långsammare, bildade färre kolonier och dog lättare, oberoende av deras specifika genetiska mutationer.
Hur GPR54 håller tumörceller vid liv
För att undersöka vidare frågade forskarna vilka interna kretsar GPR54 använder. De fann att GPR54 kopplar in två större tillväxtvägar i cellen, kända som AKT och ERK. Båda är vanliga ”kopplingsnav” som får cancerceller att dela sig och motstå celldöd. När GPR54 blockerades eller togs bort minskade aktiviteten i AKT och ERK, och cellerna blev mer benägna att genomgå apoptos. Återställande av starka AKT- eller ERK-signaler kunde delvis rädda cellerna, vilket bekräftar att GPR54 hjälper NSCLC-celler att överleva genom att stödja dessa tillväxtkretsar.
Omkoppling av hur cancer använder socker
Cancerceller omprogrammerar ofta hur de använder näringsämnen och föredrar snabb nedbrytning av socker (glykolys) för att driva tillväxt. Genuttrycksanalyser av mösstumörer utan Gpr54 visade att många gener som är involverade i sockerhantering och energiproduktion dämpades. I lungcancerceller behandlade med kisspeptin för att aktivera GPR54 visade mätningar av syreförbrukning och syraproduktion — proxyer för energimetabolism — att GPR54 ökar glykolysen. Blockering av GPR54-vägen i olika steg (Gαq/11-omkopplaren, PI3K, AKT eller mTOR) minskade glukosförbrukning och laktatproduktion och drev cellerna mot apoptos. Enkelt uttryckt hjälper GPR54 NSCLC-celler att förbränna socker snabbare och effektivare, vilket stödjer deras snabba tillväxt.
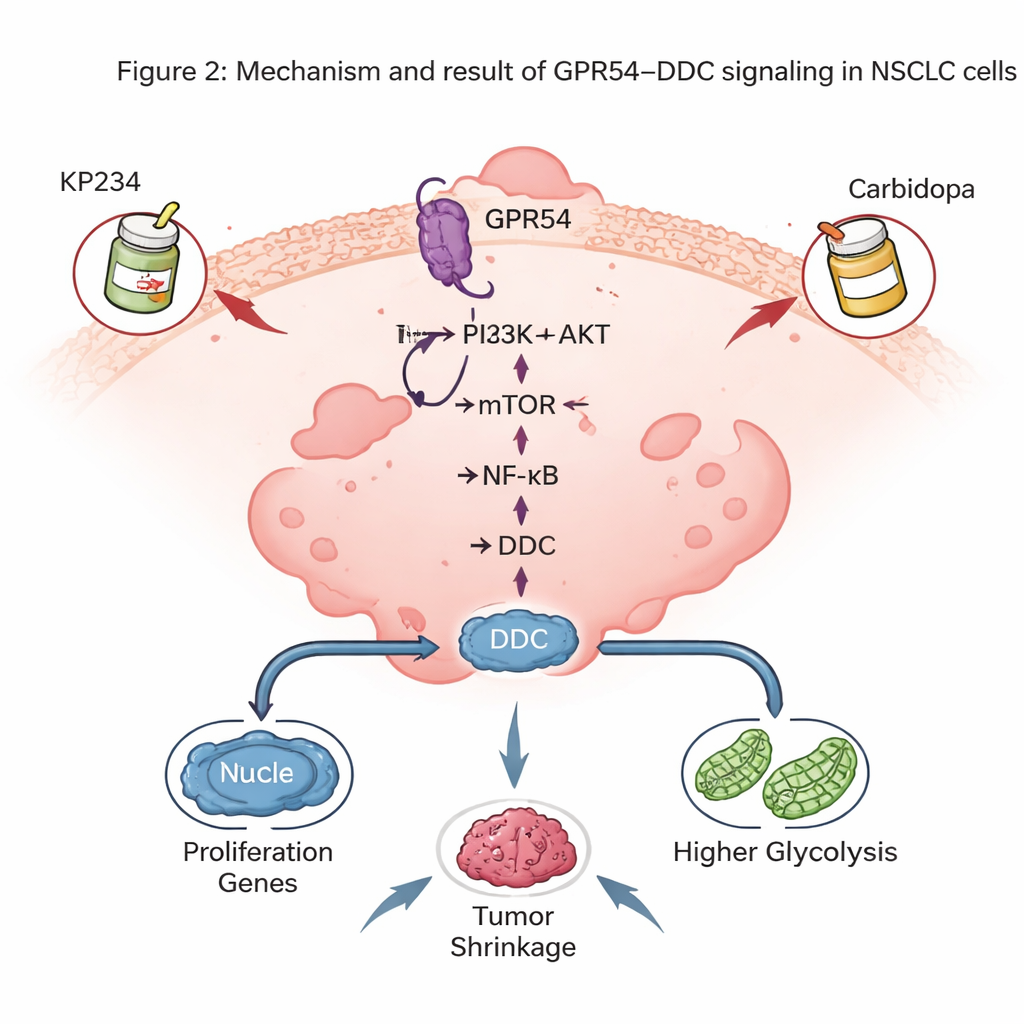
Den överraskande rollen för ett hjärnrelaterat enzym
En av de mest anmärkningsvärda upptäckterna var att GPR54 reglerar nivåerna av DDC, ett enzym mest känt för att tillverka hjärnkemikalierna dopamin och serotonin. I mösstumörer följde DDC-nivåerna noggrant mängden GPR54: mindre GPR54 betydde mindre DDC. Mänskliga NSCLC-tumörer och cellinjer visade också högre DDC än normala lungceller, och patienter med mer DDC hade sämre överlevnad. Nedreglering av DDC i lungcancerceller bromsade tumörtillväxt i möss, minskade celldelning i odlingar och utlöste mer apoptos. På molekylär nivå hjälpte DDC till att bibehålla aktivitet i NF-κB-vägen, en huvudregulator som främjar cancercellers överlevnad och inflammation, och stödde också tumörcellernas högglykolytiska tillstånd.
Test av en läkemedelsparningsstrategi
Eftersom DDC redan riktas mot i Parkinsons sjukdom av ett läkemedel som heter karbidopa, undersökte författarna om kombinationen av en GPR54-blockerare (KP234) med karbidopa kunde slå mot NSCLC från två håll. I cellodlingar och i musmodeller där mänskliga NSCLC-celler odlats i lungan minskade den dubbla behandlingen tumörtillväxten mer än något av läkemedlen ensamt och ökade cancercelldöd, utan påtaglig viktminskning hos djuren. Dessa kombinationer visade också lovande resultat tillsammans med vissa moderna riktade läkemedel mot muterade RAS-gener, vilket tyder på att GPR54–DDC-signalering kan byggas ovanpå befintliga precisionsterapier.
Vad detta betyder för framtida lungcancervård
För en lekmannapublik är huvudbudskapet att NSCLC-celler förlitar sig på ett tidigare underskattat samspel mellan en ytswitch (GPR54) och ett metabolt enzym (DDC) för att hålla sig vid liv och för att bränna bränsle snabbt. Att störa detta samspel försvagar tumörer, gör att de växer långsammare och dör lättare i experimentella modeller. Även om mycket arbete återstår innan sådana strategier når kliniken positionerar denna studie GPR54 och DDC som potentiella biomarkörer för att identifiera aggressiv NSCLC och som lovande mål för nya kombinationsbehandlingar som skulle kunna förbättra utfallen för patienter vars tumörer i dag undviker standardbehandlingar.
Citering: Hwang, HH., Lee, S.Y., Lee, C. et al. GPR54 regulates non-small cell lung cancer development via dopa decarboxylase. Sig Transduct Target Ther 11, 74 (2026). https://doi.org/10.1038/s41392-026-02591-x
Nyckelord: icke-småcellig lungcancer, GPR54, dopa-dekarboxylas, cancermetabolism, målinriktad behandling