Clear Sky Science · sv
Reaktiva syreföreningar (ROS) i cancer: från mekanism till terapeutiska implikationer
När hjälpsamma molekyler blir farliga
Inuti varje cell bildas ständigt små kemiska gnistor kallade reaktiva syreföreningar, eller ROS, som en del av normal cellfunktion. I rätt mängder hjälper de celler att växa, kommunicera och försvara sig mot mikrober. Men den här översikten förklarar hur samma molekyler också kan skada DNA, vrida cellernas signalering ur led och driva cancer att växa, sprida sig och stå emot behandling. Att förstå ROS:s ”dubbelliv” hjälper forskare att utforma nya cancerterapier som antingen dämpar skadlig oxidativ stress eller medvetet skjuter den över gränsen för att döda tumörceller.
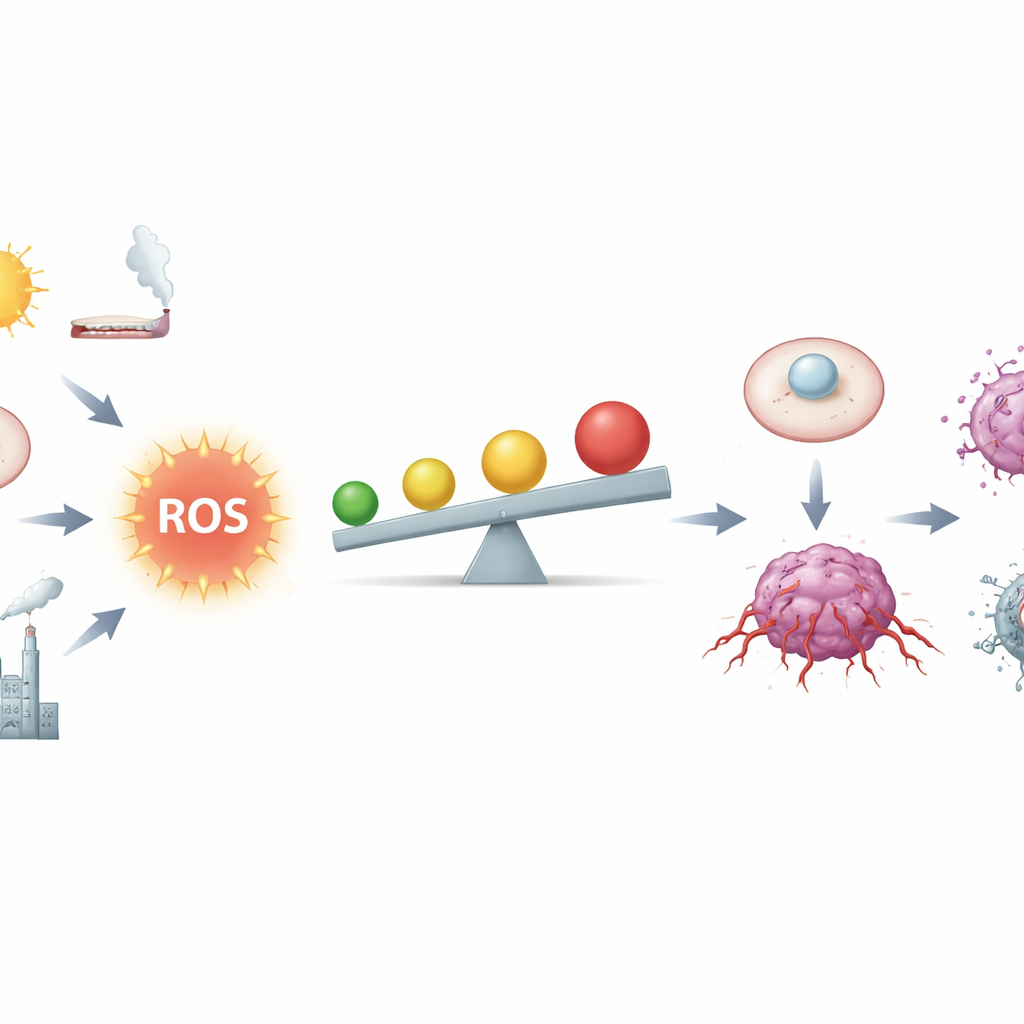
Den tunna linjen mellan bränsle och brand
Författarna beskriver ROS som kemiska biprodukter av andning och metabolism, men också som kraftfulla budbärare. I friska vävnader hjälper låga nivåer ROS att styra cellcykeln, reparera skador och finjustera immunförsvaret. Celler håller dessa signaler i schack med ett invecklat antioxidantnätverk, inklusive molekyler som glutation och enzymer kontrollerade av en huvudregulator kallad Nrf2. Cancerceller lever däremot närmare farozonen: felaktiga gener, överbelastade mitokondrier, kronisk inflammation, tobaksrök, strålning och vissa metaller ökar alla ROS. Vid måttligt förhöjda nivåer kan ROS nypa DNA, destabilisera kromosomer och kroniskt slå på tillväxt- och överlevnadskretsar, vilket gör det lättare för en normal cell att bli en cancercell.
Hur oxidativ stress formar tumörbeteende
När en tumör väl etablerats fortsätter ROS att forma dess biologi. Måttlig oxidativ stress aktiverar många tillväxtvägar som uppmuntrar celler att dela sig, bilda nya blodkärl, invadera närliggande vävnad och motstå cytostatika. ROS kan omprogrammera hur cancerceller använder socker, fetter och aminosyror och styra bränslet in i banor som skapar extra antioxidantkapacitet och byggstenar för nya celler. De påverkar också cellens ödesbeslut: beroende på intensitet och kontext kan ROS välta balansen mot överlevnadssignaler eller mot en av flera former av programmerad celldöd, inklusive klassisk apoptos och nyare former såsom ferroptos, nekroptos och cuproptos. Det gör ROS både till medhjälpare i tumörutveckling och potentiella utlösare av tumörens självförstörelse.
Omskapande av immunitet och läkemedelsrespons
Översikten framhäver att ROS inte bara verkar inom cancerceller—de omformar tumörens omgivning. Hög oxidativ stress kan utarma eller döda cancerbekämpande T‑celler och natural killer‑celler, samtidigt som den gynnar suppressiva celler som skyddar tumören från angrepp. ROS hjälper också tumörer att uppreglera ”döda-mig-inte”-signaler såsom checkpoint‑proteiner, vilket dämpar effekten av immunterapi. Samtidigt kan måttlig ROS driva läkemedelsresistens genom att öka läkemedelsspumpning och stressresponser, så att cancerceller spottar ut cytostatika eller reparerar den skada behandlingen orsakar. Under andra förhållanden kan det dock räcka att driva ROS över en kritisk tröskel för att montera ner dessa försvar och återkänsliggöra tumörer för behandling.
Att göra redoxsvaghet till behandlingsstrategi
Eftersom cancerceller balanserar på en knivsegg mellan att nyttja ROS och att förgiftas av dem, ser författarna redoxbalansen som ett terapeutiskt spak. En bred strategi är att sänka skadliga ROS eller stärka antioxidantsystemen, i första hand för prevention eller för att skydda frisk vävnad under behandling. En annan är att göra tvärtom i tumörer: hämma antioxidantmekanismer eller öka ROS‑produktion tills cancercellerna korsar en dödlig gräns, särskilt i kombination med strålning, riktade läkemedel eller immunterapi. En tredje ansats är att lämna ROS‑nivåerna i fred men blockera de specifika ROS‑känsliga brytarna—signalkomponenter, metabola enzymer eller dödsvägar—som tumörer är beroende av. Genom dessa idéer löper temat om personalisering: olika cancerformer bär olika ”redoxsignaturer”, så framtida terapier kan behöva blod‑ eller vävnadstester av oxidativ skada, antioxidantkapacitet och ROS‑kopplade gener för att välja rätt redoxinriktade behandling för varje patient.
Vad detta betyder för patienter
Enkelt uttryckt hävdar artikeln att ROS varken är entydigt dåliga eller entydigt bra; de är kraftfulla verktyg som celler — och cancer — använder. Cancerceller tenderar att operera närmare en tipping point för oxidativ stress än friska celler, vilket kan skapa ett terapeutiskt fönster. Eftersom både antioxidanter och pro‑oxidanter kan hjälpa eller skada beroende på dos, timing och tumörtyp är dock generell användning av kosttillskott eller ROS‑ökande läkemedel riskabelt. Författarna slutsatser är att framtiden ligger i noggrant konstruerade terapier och diagnostik som avläser varje tumörs redoxstatus och sedan finjusterar ROS och antioxidantsystemen precis lagom—antingen ned för att skydda normala vävnader, eller upp för att pressa cancerceller över deras brytpunkt.
Citering: Akter, S., Madhuvilakku, R., Kar, A.K. et al. Reactive oxygen species (ROS) in cancer: from mechanism to therapeutic implications. Sig Transduct Target Ther 11, 111 (2026). https://doi.org/10.1038/s41392-026-02583-x
Nyckelord: reaktiva syreföreningar, oxidativ stress, cancermetabolism, redoxterapi, tumörmikromiljö