Clear Sky Science · sv
Parathyreoideahormon–relaterat protein är ett terapeutiskt mål vid idiopatisk lungfibros
Varför ärrbildning i lungorna spelar roll
Idiopatisk lungfibros (IPF) är en förödande lungsjukdom där de fina luftblåsorna gradvis förvandlas till stel ärrvävnad, vilket gör varje andetag ansträngande. Nuvarande läkemedel kan sakta ner denna ärrbildning men kan inte stoppa eller återställa den. Denna studie identifierar en tidigare underskattad mekanism i processen: ett litet hormonliknande protein som produceras av luftvägarnas slemhinneceller, kallat parathyreoideahormon‑relaterat protein (PTHrP), och visar att blockering av dess verkan skulle kunna erbjuda en ny behandlingsväg för IPF.
En dold budbärare i luftvägarna
IPF har länge kopplats till överaktiva fibroblaster—celler som normalt hjälper till att reparera vävnad men som i denna sjukdom går på övervarv och deponerar för mycket kollagen, ärrvävnadens huvudkomponent. Många studier har fokuserat på signaler från immunceller och de djupaste alveolära cellerna, men detta arbete ser högre upp i bronkträdet, vid rören som leder luft in i lungorna. Genom att återanalysera stora genetiska dataset från personer med och utan IPF fann forskarna att en gen kallad PTHLH, som kodar för PTHrP, konsekvent var uppreglerad i IPF-lungor. Mikroskopisk avbildning av mänskliga lungprover bekräftade att PTHrP-proteinet var mycket vanligare hos patienter med IPF och koncentrerades i de bronkiella epitelcellerna som bekläder luftvägarna.
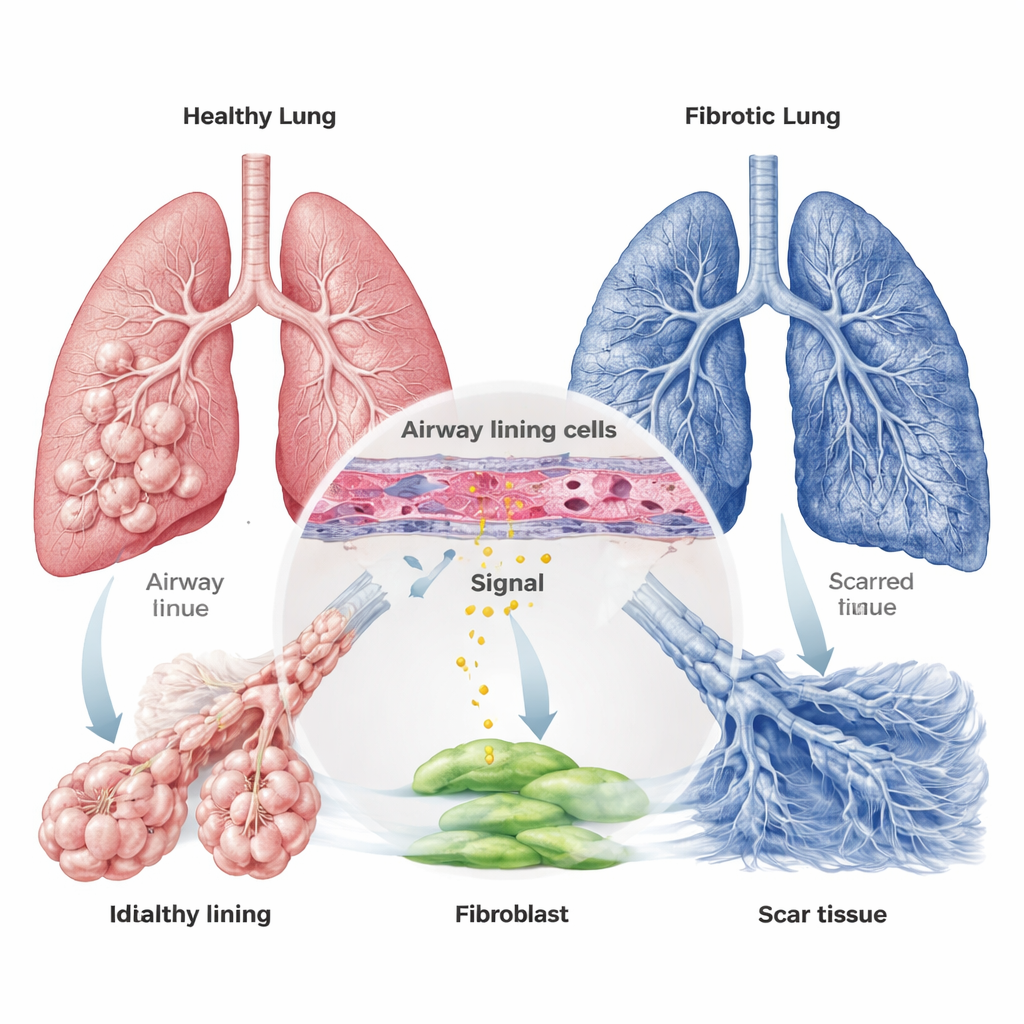
Från luftvägssignal till ärrbildande celler
PTHrP bildas som ett större föregångarprotein som kan klyvas till flera mindre fragment. Teamet fokuserade på ett fragment, PTHrP1‑34, känt för att aktivera en receptor på vissa celler. De visade att bronkiella epitelceller under stress—såsom låg syretillgång eller exponering för det bleomycinliknande läkemedlet, som ofta används för att modellera lungskada hos djur—frigör mer PTHrP1‑34 i sin omgivning. Samtidigt fann de att den matchande receptorn, kallad PTH1R, främst finns inte på alveolära epitelceller utan på fibroblaster och glattmuskelceller. Detta upprättar en kommunikationslinje: skadade luftvägsceller skickar ut PTHrP1‑34 och närliggande fibroblaster är inställda för att ta emot signalen.
Hur signalen gör fibroblaster aggressiva
I laboratorieodlingar gjorde tillsats av PTHrP1‑34 till mänskliga och musläderens fibroblaster att de antog ett mer aggressivt, ärrbildande tillstånd. De ökade produktionen av alfa‑smooth muscle actin (en markör för så kallade myofibroblaster) och viktiga kollagengener, och de rörde sig mer—egenskaper kopplade till progressiv ärrbildning. Molekylära tester visade att detta sker via en specifik intern väg: PTHrP1‑34 binder PTH1R på fibroblastens yta, ökar en budbärarmolekyl kallad cAMP och aktiverar ett enzym benämnt PKA, vilket sedan slår på ”fibrosgener” i cellkärnan. Att blockera receptorn eller hämma PKA minskade starkt denna respons. Viktigt är att luftvägs‑ och alveolära epitelceller inte reagerade på samma sätt, vilket understryker att detta hormonfragment verkar mycket selektivt på fibroblaster.
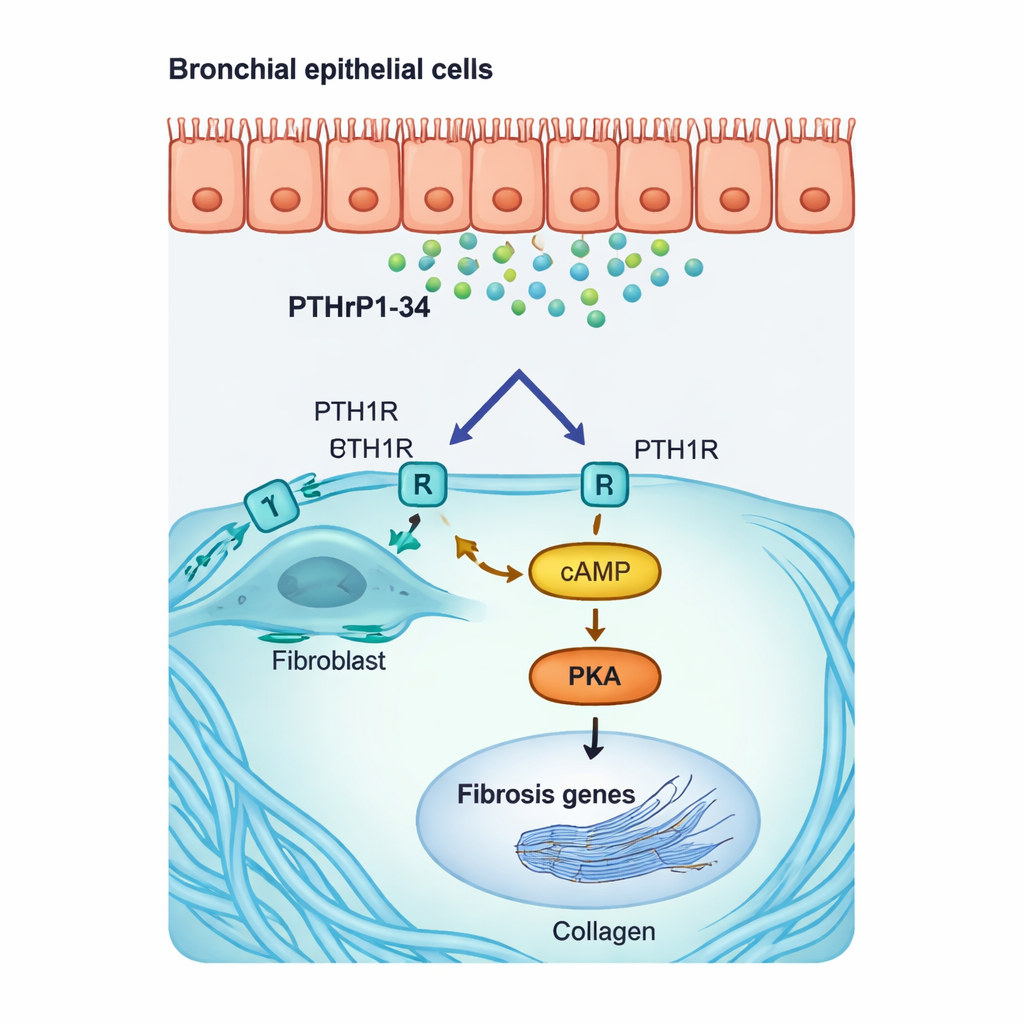
Bevis i sjuka lungor och nya behandlingsvägar
För att se om denna väg spelar roll i hela lungor vände forskarna sig till musmodeller av lungskada orsakad av bleomycin. När djurens lungor utvecklades från tidig inflammation till tät ärrbildning ökade nivåerna av PTHrP1‑34 markant i luftvägar och lungvävnad men inte i blodomloppet, vilket tyder på en lokal, lungspecifik uppgång. Direkt tillförsel av PTHrP1‑34 i luftvägarna drev lungorna mot ett fibrotiskt tillstånd och, när det kombinerades med bleomycin, förvärrade det i hög grad ärrbildningen och kollagenansamlingen. Teamet prövade därefter tre sätt att avbryta denna skadliga signal: en neutraliserande antikropp som fångar upp PTHrP1‑34, ett kort peptidfragment som blockerar dess receptor (PTHrP7‑34) och en gen‑tystande metod som sänker PTHrP‑produktionen i luftvägsceller. I samtliga fall utvecklade mössen mindre lungsfibros, hade lägre kollagennivåer och bibehöll bättre kroppsvikt, med effekter som motsvarade eller överträffade de hos nintedanib, ett godkänt läkemedel mot IPF.
Vad detta innebär för framtida vård
För icke‑specialister är huvudbudskapet att bronkiell slemhinna inte bara är en passiv luftledning; den kan aktivt driva lungsfibros genom att sända ut kraftfulla kemiska budskap. Denna studie identifierar PTHrP1‑34 som ett av dessa budskap och visar att blockering av dess kommunikation med fibroblasterna kan bromsa eller till och med vända fibros i djurmodeller. Även om ytterligare arbete krävs för att bekräfta säkerhet och effekt hos människor, kan inriktning på PTHrP1‑34/PTH1R‑vägen tillföra en helt ny klass av behandling för IPF, med målet att inte bara sakta sjukdomsprogressen utan att angripa en av dess grundläggande drivkrafter.
Citering: Fang, XQ., Lim, S., Lee, YM. et al. Parathyroid hormone–related protein is a therapeutic target in idiopathic pulmonary fibrosis. Sig Transduct Target Ther 11, 67 (2026). https://doi.org/10.1038/s41392-026-02578-8
Nyckelord: idiopatisk lungfibros, lungsfibros, parathyreoideahormon-relaterat protein, fibroblastaktivering, bronkiell epitel