Clear Sky Science · sv
Exogen Epstein–Barr-viralt nukleärt antigen 1 orsakar ADAR1-driven tumörresistens mot immunterapi
Varför ett vanligt virus spelar roll för cancerbehandling
Många cancerformer behandlas i dag med immunterapidroger som frigör kroppens eget immunsystem. Ändå drar de flesta patienter fortfarande inte nytta, eftersom deras tumörer lär sig att gömma sig för immunsystemet. Denna studie avslöjar hur ett mycket vanligt virus, Epstein–Barr-virus (EBV), hjälper tumörer att stänga av immunförsvaret och bli motståndskraftiga mot dessa kraftfulla läkemedel — och hur en ny typ av designad molekyl kan slå på försvaren igen.
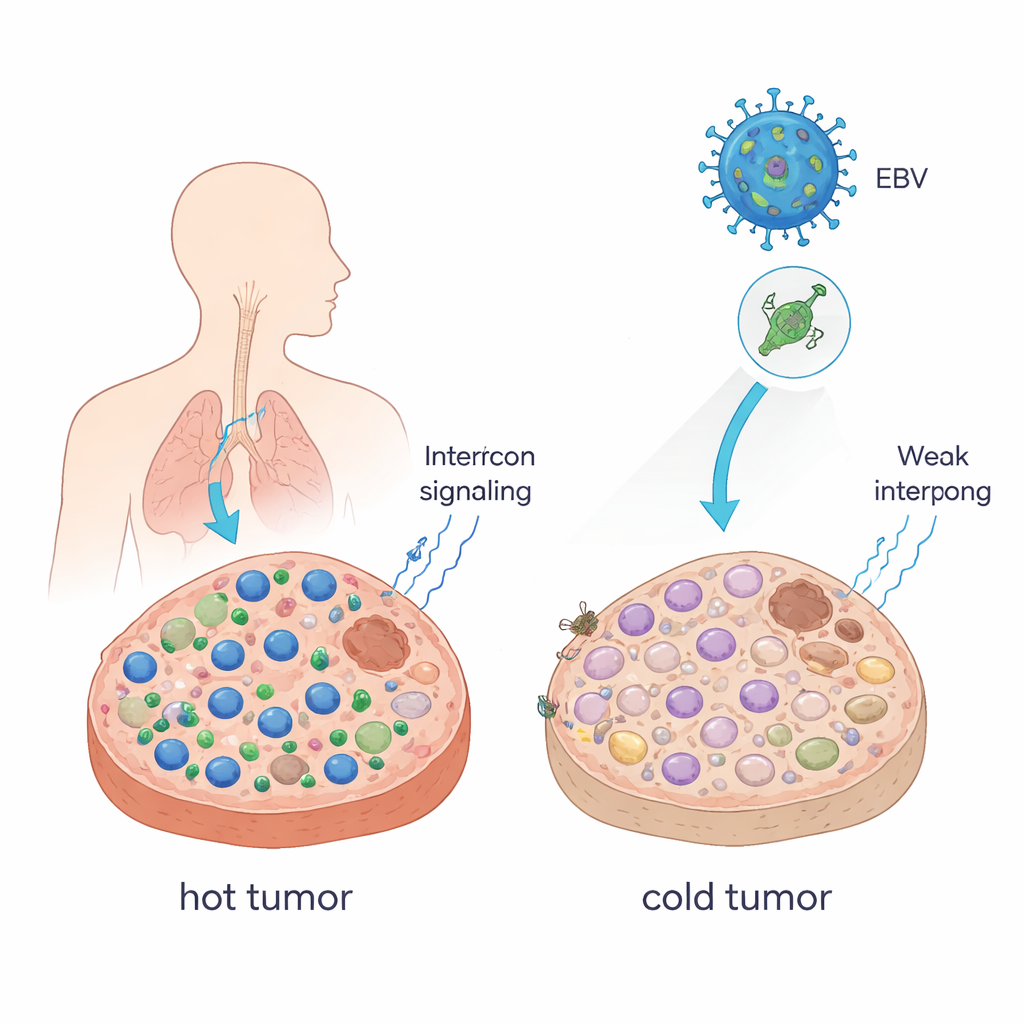
Att förvandla varma tumörer till kalla
Läkare beskriver ofta tumörer som ”varma” när de är fulla av cancer‑dödande T‑celler, och ”kalla” när dessa celler är sällsynta. Varma tumörer svarar vanligtvis väl på immuncheckpoint‑blockad (ICB)‑läkemedel som anti–PD‑1‑antikroppar; kalla tumörer gör det oftare inte. Författarna visade att ett enda EBV‑protein, kallat EBNA1, kan driva tumörer mot detta kallare, mer undvikande tillstånd. När de tvingade musstumörceller att producera EBNA1 och odlade dem i möss med intakt immunsystem blev tumörerna större, innehöll färre CD8+ T‑celler och natural killer‑celler, och hade fler immunsuppressiva makrofager. Signaler kallade interferoner — viktiga budbärare som hjälper till att mobilisera immunceller — var också starkt reducerade. I patientprover av nasofarynxkarcinom, en cancerform starkt kopplad till EBV, visade tumörer som uttryckte EBNA1 liknande minskningar av CD8+ T‑celler jämfört med normalt vävnad.
En viral genväg in i cellens RNA‑styrningsmekanism
För att förstå hur EBNA1 omformar tumörmiljön sökte forskarna efter humana proteiner som fysiskt interagerar med det. De fokuserade på ett protein kallat IGF2BP3, som läser små kemiska märken (m6A) på budbärar‑RNA och kan öka deras stabilitet eller översättning till protein. EBNA1 band tätt till IGF2BP3 i flera celltyper, inklusive EBV‑positiva cancerceller. Data från patienttumörer visade att höga nivåer av IGF2BP3 gick hand i hand med svag interferon‑relaterad genaktivitet och lägre infiltration av CD8+ T‑celler, vilket antyder att denna virus–värd‑allians kan dämpa anti‑tumörimmunitet.
Förstärkning av en RNA‑redigerare som tystar farosignaler
Djupare analyser framhöll ett nyckelmål för denna interaktion: ADAR1, ett enzym som redigerar dubbelsträngat RNA genom att omvandla vissa ”A”‑bokstäver till ”I”. Denna redigering kan få viralliknande RNA inuti celler att verka mindre farligt för interna sensorer och därigenom minska interferon‑svar. Författarna fann att EBNA1, IGF2BP3 och en translationsfaktor kallad EIF4G1 bildar ett tredelat komplex på ADAR1‑mRNA. Detta komplex ökar m6A‑märkningen, rekryterar translationsmaskineriet och ökar selektivt ADAR1‑proteinproduktionen utan att höja dess RNA‑nivåer. Som ett resultat utför tumörceller mer RNA‑redigering i upprepade genetiska element nära interferon‑relaterade gener. Dessa redigeringar minskar mängden oredigerat dubbelsträngat RNA som normalt skulle varna sensorer som MDA5 och PKR, dämpar interferonproduktionen och hjälper tumörer att gömma sig från immunsystemet.
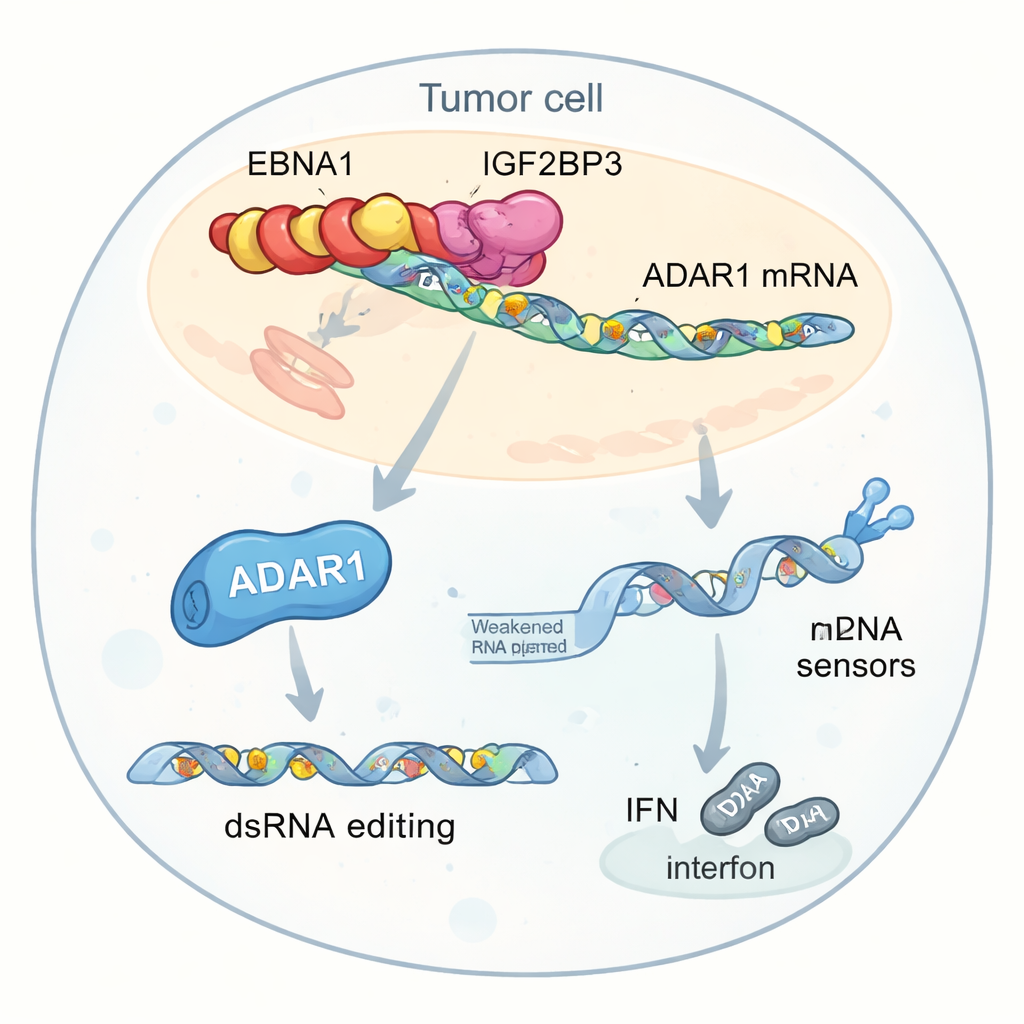
Mindre interferon, svagare immunterapi
När tumörceller som uttrycker EBNA1 utsattes för T‑celler och anti–PD‑1‑antikroppar i laboratoriet var de svårare att döda än kontrollceller och frisatte mindre interferon. Även när de behandlades direkt med interferon var EBNA1‑bärande celler mindre känsliga, och deras interna RNA‑sensorer aktiverades i mindre grad. Att minska nivåerna av ADAR1 återställde delvis dessa effekter, och återupplivade sensoraktivitet och interferonsignalering. Genetiska och sekvenseringsexperiment bekräftade att EBNA1‑uttryckande celler visade fler A‑till‑I‑redigeringshändelser i specifika RNA‑regioner, särskilt efter interferonstimulering, vilket ytterligare stöder idén att viral förstärkning av ADAR1 hjälper till att neutralisera farosignaler som annars skulle utlösa starka immunrespons.
En designad degrader som återväcker immunsvaret
Teamet frågade sig sedan om avlägsnande av EBNA1 från tumörer skulle kunna återställa deras sårbarhet för immunterapi. De designade en PROTAC‑molekyl, EP‑1215, som märker EBNA1 för nedbrytning av cellens eget avfallssystem. Vid låga doser degraderade EP‑1215 effektivt EBNA1 och minskade ADAR1‑proteinnivåer. I musexperiment hade EP‑1215 ensam begränsad effekt på EBNA1‑positiva tumörer, och anti–PD‑1 ensam var också svag. Men i kombination krympte de två behandlingarna tumörerna kraftigt, ökade CD8+ T‑cellsinfiltrationen och förstärkte interferonproducerande T‑celler. I humaniserade musmodeller med mänskliga immunceller och EBV‑relaterade tumörer överträffade kombinationen återigen enstaka behandlingar, utan uppenbar lever‑ eller njurtoxicitet.
Vad detta betyder för framtida cancervård
För icke‑specialister är budskapet att ett vanligt virus kan tyst omkoppla cancerceller för att dämpa interna alarmsystem, och stänga av kemiska signaler som annars skulle locka och aktivera immunceller. EBNA1 gör detta genom att kapa en värd‑RNA‑läsare (IGF2BP3) och en translationsfaktor (EIF4G1) för att överproducera RNA‑redigeraren ADAR1, som redigerar bort just de RNA‑strukturer som immunsensorer är byggda för att känna igen. Genom att degradera EBNA1 med en skräddarsydd PROTAC som EP‑1215 kunde författarna återställa dessa farosignaler och göra resistenta tumörer mottagliga igen för befintliga checkpoint‑läkemedel. Om liknande strategier visar sig vara säkra och effektiva hos människor kan det bli en ny väg att omvandla kalla, EBV‑kopplade tumörer till varma mål som moderna immunterapier äntligen kan träffa.
Citering: Liu, C., Sun, Z., Li, C. et al. Exogenous Epstein–Barr virus nuclear antigen 1 induces ADAR1-driven tumor resistance against immunotherapy. Sig Transduct Target Ther 11, 63 (2026). https://doi.org/10.1038/s41392-026-02574-y
Nyckelord: Epstein-Barr-virus, immunterapiresistens, ADAR1, RNA-redigering, nasofarynxkarcinom