Clear Sky Science · sv
Molekylär mekanism för kolesterolberoende membransammansmältning vid SARS-CoV-2-inträde
Varför kolesterol spelar roll för ett luftvägsvirus
Viruset som orsakar COVID-19, SARS-CoV-2, tar sig in i våra celler genom att slå samman sitt yttre hölje med våra cellmembran. Denna artikel ställer en bedrägligt enkel fråga med stora följder: hur mycket påverkar kolesterol — ett fettämne som oftast förknippas med hjärtsjukdom — det steget i sammansmältningen? Författarna visar att kolesterol i virusmembranet inte bara finjusterar infektionseffektiviteten; det hjälper faktiskt till att organisera virusets spike-proteiner till kraftfulla dockningsplattformar som gör inträdet både lättare och mer pålitligt.
Att bygga en minimal modell för virusinträde
För att dissekera denna process återskapade forskarna mötet mellan virus och cell i ett provrör med hjälp av små fettbubblor kallade liposomer. Ena uppsättningen liposomer bar SARS-CoV-2-spike och stod för virusmembranet; den andra bar ACE2-receptorn och efterliknade värdcellens yta. När de blandades och aktiverades av särskilda enzymer som "klipper" spike till dess sammansmältningberedda form, sammansmälte dessa artificiella membran och ett fluorescerande färgämne kunde flytta från en bubbla till en annan. Detta avskalade system gjorde det möjligt för teamet att exakt justera lipidsammansättningen — inklusive kolesterolnivåerna — på varje sida och iaktta hur sammansmältningen utvecklades steg för steg. 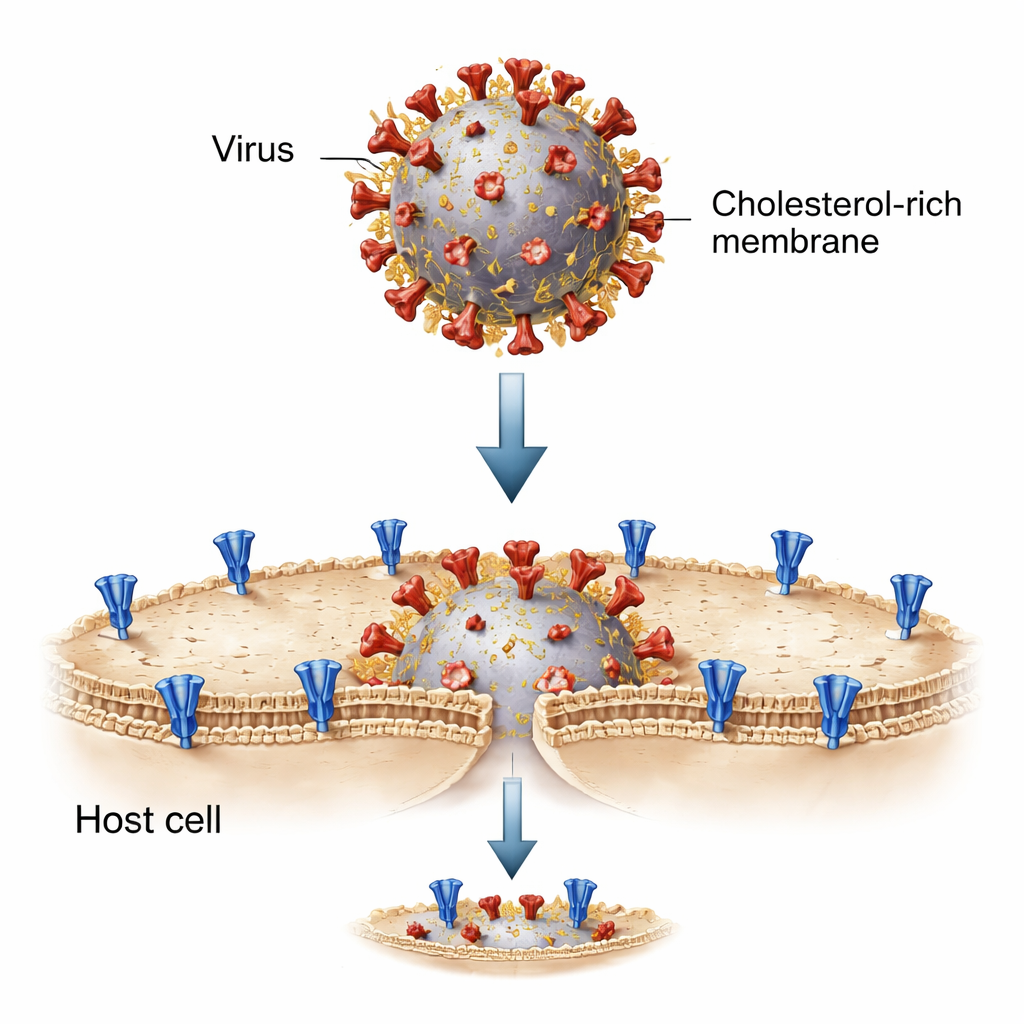
Kolesterol ökar dockning mer än sammansmältning
Genom att variera kolesterolmängden upptäckte gruppen att tillsats av kolesterol i det spike-bärande membranet gjorde sammansmältning vanligare, men inte på det sätt man kanske förväntar sig. Hög kolesterolhalt ändrade inte dramatiskt sannolikheten för att två redan fästa membran faktiskt skulle smälta samman. I stället ökade den kraftigt hur ofta vesiklar som bar spike först dockade vid vesiklar som bar ACE2. Enpartikel-avbildning visade många fler framgångsrika dockningstillfällen när spike satt i kolesterolrika membran, medan sannolikheten att ett dockat par gick vidare till fullständig sammansmältning förblev ungefär konstant. Intressant nog gav kolesterol på ACE2-sidan liten nytta och vid mycket höga nivåer hindrade det till och med sammansmältning, vilket pekar på virusets — snarare än värdens — kolesterol som huvuddrivkraft.
Från modellmembran till levande celler
Forskarna frågade sedan om samma mönster gällde i levande celler. De konstruerade mänskliga celler att uttrycka antingen spike eller ACE2 och såg dem bilda stora sammansmälta strukturer, så kallade syncytier, när de blandades. Att ta bort kolesterol från spike-exprimerande celler nästan eliminerade bildningen av syncytier, medan återställning av kolesterol räddade sammansmältningen. I parallella experiment med SARS-CoV-2 "pseudovirus" (ofarliga partikel som använder coronaviruspiken för att komma in i celler) minskade avstrippning av kolesterol från virusmembranet kraftigt infektionen, och att återföra kolesterol ökade infektionen i dosberoende grad. Däremot gav ändringar av kolesterol enbart på ACE2-exprimerande celler liten förändring. I samtliga tester var budskapet tydligt: kolesterol i det spike-innehållande membranet är avgörande för effektivt inträde.
Spike-kluster: kolesterolets hemliga vapen
Varför skulle kolesterol på virussidan spela så stor roll? Högupplöst membranavbildning visade att spike-proteiner tenderar att bilda täta kluster när kolesterol är rikligt, men förblir mer utspridda när kolesterol saknas. Enkeltmolekylmätningar gick längre och visade att dessa kluster innehåller fler kopior av spike under kolesterolrika förhållanden. Författarna spårade denna effekt till en cysteinrik region (CRR) i spikens svansända, inne i virusmembranet. Detta segment modifieras genom palmitoylering — en typ av fet "ankare" som favoriserar kolesterolrika områden. När teamet förkortade spikens svans eller muterade alla tio cysteiner för att blockera palmitoylering, klustrade spike inte längre med kolesterol och den kolesteroldrivna ökningen i dockning och sammansmältning försvann. 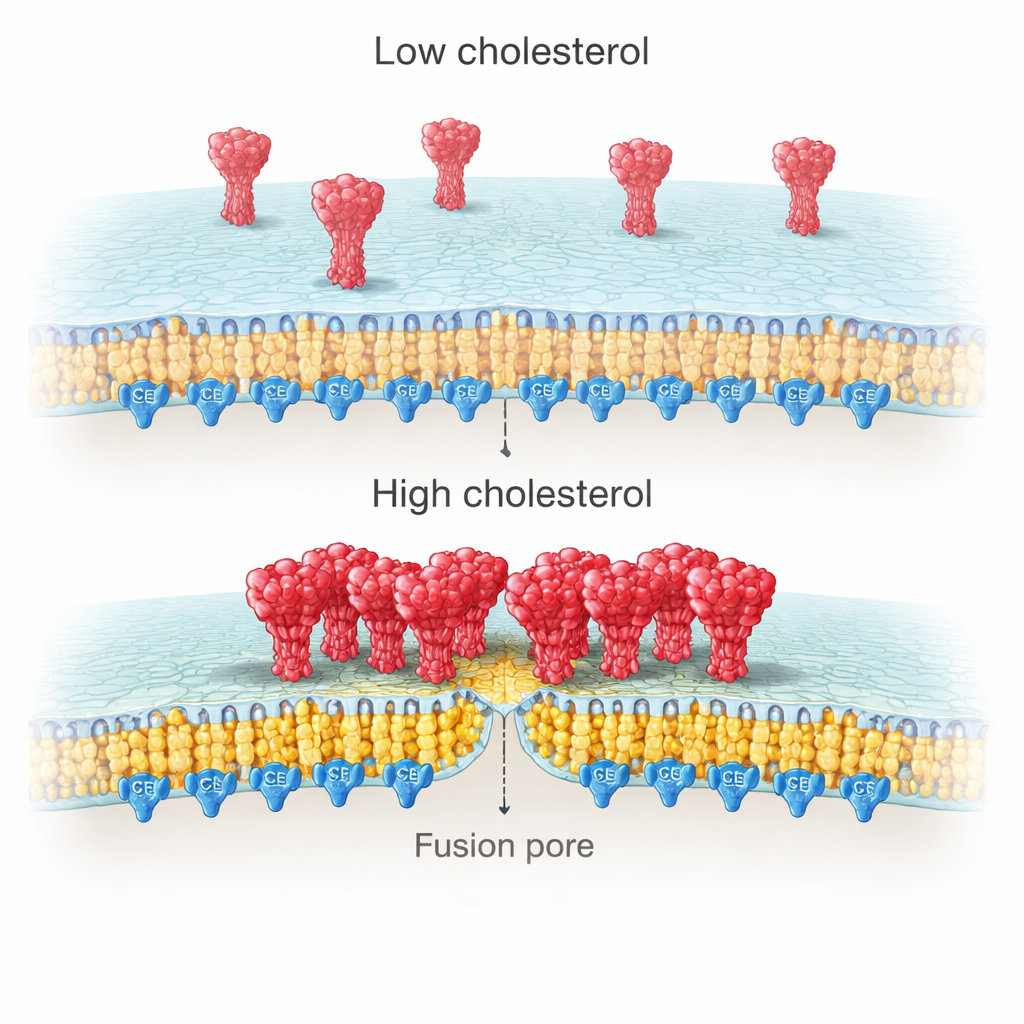
Hur detta kan hjälpa framtida behandlingar
Enkelt uttryckt drar studien slutsatsen att kolesterol förvandlar virusmembranet till en sammansmältplattform genom att samla många spike-proteiner i täta kluster via deras palmitoylerade svansregion. Dessa kluster dockar mer effektivt mot ACE2 på värdceller, vilket ökar chansen att varje enskilt möte leder till lyckad sammansmältning och infektion. För icke-specialister är huvudpoängen att kolesterol inte bara är en passiv ingrediens i virusets hölje; det är en aktiv organisatör av spikens maskineri. Det gör spikens cysteinrika, kolesterolkänsliga svans — och de enzymer som palmitoylerar den — till lovande mål för breda antivirala strategier som skulle kunna fungera mot olika coronavirusvarianter.
Citering: Li, W., Wu, M., Feng, S. et al. Molecular mechanism of cholesterol-dependent membrane fusion in SARS-CoV-2 entry. Sig Transduct Target Ther 11, 57 (2026). https://doi.org/10.1038/s41392-026-02573-z
Nyckelord: kolesterol, SARS-CoV-2 spike, membransammansmältning, virusinträde, palmitoylering