Clear Sky Science · sv
PKC-eta främjar bröstcancermetastasering genom att reglera Hippo–YAP‑signalvägen
Varför denna forskning är viktig
Trippelnegativ bröstcancer (TNBC) är en av de farligaste formerna av bröstcancer eftersom den sprider sig tidigt och saknar riktade behandlingar. Denna studie avslöjar hur ett specifikt enzym inne i cancerceller, kallat PKC‑eta (PKCη), fungerar som en huvudströmbrytare som hjälper tumörer att släppa taget, resa genom kroppen och anläggas som nya tumörer. Genom att förstå denna strömbrytare identifierar forskarna också en liten naturlig peptid som kan slå av den, vilket pekar på en potentiell ny behandlingsväg för denna aggressiva sjukdom. 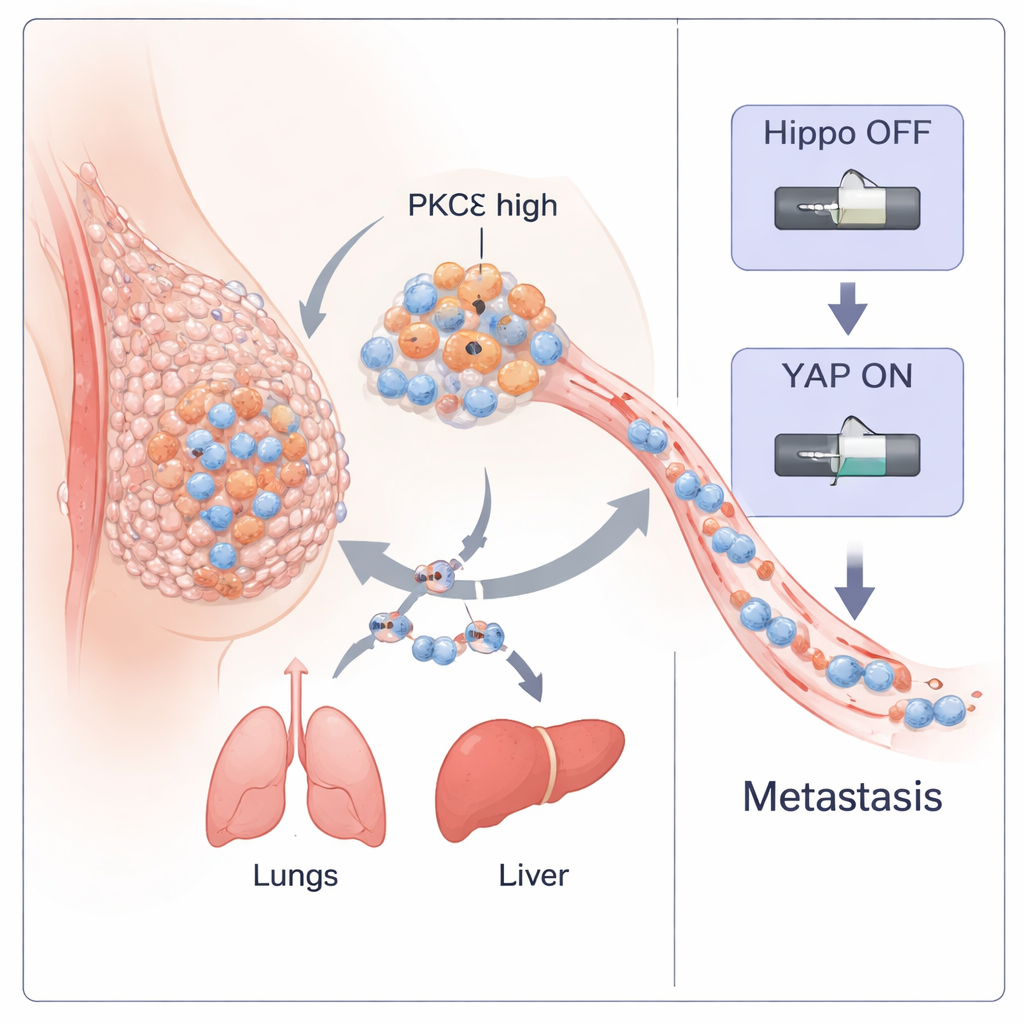
En dold drivkraft i aggressiva brösttumörer
Teamet började med att bearbeta stora samlingar av patientdata för bröstcancer. De fann att genen som kodar PKCη (PRKCH) är särskilt hög i en tumörsubtyp kallad ”claudin‑low”, som starkt överlappar med TNBC och är rik på stamliknande, mycket rörliga celler. I flera patientkohorter visade tumörer med höga nivåer av PRKCH tydliga signaturer av epitelial–mesenkymal övergång (EMT)—en process där tidigare ordnade celler luckrar upp sina fästen, ändrar form och blir mer invasiva. PRKCH‑nivåerna var också högre i metastatiska prover än i de ursprungliga primärtumörerna, och proteinfärgning av humana TNBC‑vävnader visade mer aktiv, perinukleär PKCη i högre grad och mer avancerade cancerformer. Tillsammans pekade dessa fynd på att PKCη är nära kopplat till tumöraggressivitet och spridning.
Från petriskål till mus: visa att PKCη driver spridning
För att testa kausalitet använde forskarna CRISPR‑genredigering för att ta bort PKCη från två starkt metastatiska TNBC‑cellinjer, en från mus (4T1) och en human (MDA‑MB‑231). Utan PKCη skiftade cellerna mot ett mer ”epitelialt” tillstånd: de ökade adhesionsproteiner som E‑cadherin och EpCAM, och minskade klassiska mesenkymala markörer inklusive vimentin och N‑cadherin. Dessa PKCη‑bristande celler bildade färre och mindre kolonier, migrerade och invaderade mindre effektivt, var mer känsliga för celldöd vid avlossning, och visade en kraftig minskning av cancerstamcellsegenskaper, inklusive färre CD44high/CD24low och ALDH‑positiva celler samt minskad sfärbildande kapacitet. När de injicerades i möss gav celler utan PKCη mindre primärtumörer och avsevärt färre metastaser till lungor, lever, hjärna och andra organ; mössen överlevde också längre. Återställande av PKCη vände dessa förändringar, vilket bekräftar att enzymet aktivt främjar TNBC‑progression och spridning.
Hur PKCη kapar en tillväxtkontrollväg
Studien fördjupade sig sedan i hur PKCη utövar denna prometastatiska effekt. Patientdata visade att PKCη‑nivåer stiger och faller i takt med YAP, ett kraftfullt genreglerande protein som kontrolleras av Hippo‑vägen—en cellulär ”säkerhetsbroms” som normalt begränsar tillväxt. Höga nivåer av antingen PRKCH eller YAP1 förutspådde sämre patientutfall, och höga nivåer av båda tillsammans kopplades till särskilt dålig metastasfri överlevnad. I TNBC‑celler sänkte borttagning av PKCη totala YAP‑nivåer och försköt YAP från nukleus till cytoplasma, där det är inaktivt. Biokemiska experiment visade att PKCη fysiskt binder YAP och specifikt fosforylerar Ser128. Denna modifiering stabiliserar YAP och hjälper det att gå in i kärnan för att slå på gener som driver EMT, stamcellsegenskaper och metastasering. När PKCη saknas fosforyleras YAP istället på andra ställen (Ser127 och Ser397) vilket får det att binda 14‑3‑3‑proteiner, fastna i cytoplasman och slutligen brytas ner. PKCη ökar också PTEN—en naturlig broms på AKT‑enzymet—och håller därmed AKT‑aktiviteten låg och undertrycker de uppströms Hippo‑kinaser som annars skulle inaktivera YAP. På så sätt aktiverar PKCη både YAP direkt och håller indirekt Hippo‑"bromsen" avstängd. 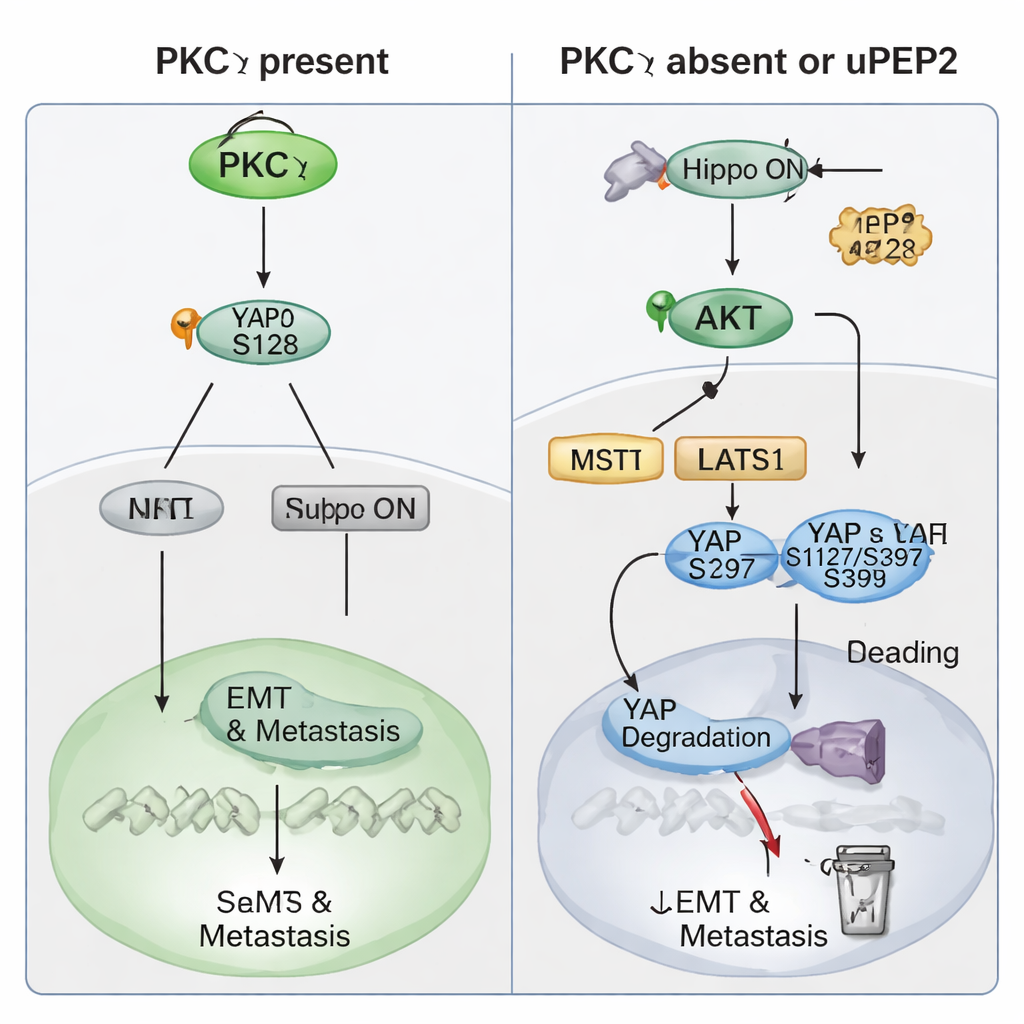
En liten peptid som avväpnar cancerns strömbrytare
Intressant nog bär PKCη‑genen ett kort upstream open reading frame (uORF) som kodar för en mikropeptid kallad uPEP2. Tidigare arbete visade att uPEP2 kan binda och hämma PKCη och närliggande enzymer. Här efterliknade behandling av TNBC‑celler med syntetisk uPEP2 effekterna av PKCη‑utslag: migration, invasion och stamlikt beteende minskade, EMT‑markörer skiftade mot en mindre aggressiv profil, och YAP‑nivåerna föll samtidigt som dess fosforyleringsmarkörer för inaktivering ökade. I musstumörer minskade uPEP2 PKCη och YAP i primärtumörerna, ökade YAP‑inaktivering och associerades med färre mikrometastaser i levern och lungorna. Mekanistiskt främjar uPEP2 degradation av PKCη, slår på Hippo‑vägen igen och driver YAP mot cytoplasmisk retention och nedbrytning.
Vad detta betyder för framtida behandlingar
För en lekmannaläsare är huvudbudskapet att forskarna har identifierat PKCη som en navpunkt som hjälper de mest aggressiva bröstcancerformerna att lossa, röra sig och kolonisera avlägsna organ genom att inaktivera ett naturligt tillväxtkontrollsystem och aktivera YAP‑"gaspedalen." Genom att slå ut PKCη eller använda den lilla naturliga peptiden uPEP2 för att degradera den kunde de återställa Hippo‑säkerhetsbromsen, tysta YAP och kraftigt minska metastaser i prekliniska modeller. Även om detta arbete fortfarande är på experimentstadiet och utfördes i cellinjer och immundefekta möss, lyfter det fram PKCη och dess interaktion med YAP som lovande mål för nya TNBC‑terapier och antyder att uPEP2‑lika läkemedel en dag skulle kunna hjälpa till att förebygga eller begränsa spridningen av denna svårbehandlade cancer.
Citering: Liju, V.B., Waidha, K., Muraleedharan, A. et al. PKC-eta promotes breast cancer metastasis by regulating the Hippo–YAP signaling pathway. Sig Transduct Target Ther 11, 58 (2026). https://doi.org/10.1038/s41392-026-02572-0
Nyckelord: trippelnegativ bröstcancer, PKC-eta, Hippo‑YAP‑väg, epitelial-mesenkymal övergång, cancermetastaser