Clear Sky Science · sv
Serpina3c skyddar mot metaboliskt dysfunktionsassocierad steatotisk leversjukdom hos avkomma inducerad av prenatalt prednisonexponering
Varför denna forskning betyder något för framtida barn
Många kvinnor behöver prednison under graviditeten för att kontrollera allvarliga autoimmuna och inflammatoriska sjukdomar. Läkare vet att det kan rädda mödrars liv, men mycket mindre är känt om hur det påverkar deras barns långsiktiga hälsa. Denna studie ställer en brännande fråga: kan prednison som tas under graviditet tyst förbereda barnets lever för att senare i livet utveckla fettleversjukdom, särskilt i kombination med en ohälsosam kost? Och om så är fallet, finns det ett sätt att vända den risken?
Ett växande leverproblem världen över
Metaboliskt dysfunktionsassocierad steatotisk leversjukdom, eller MASLD, är nu ett av de vanligaste kroniska leversjukdomarna och drabbar ungefär en tredjedel av världens befolkning med förväntad fortsatt ökning. Den omfattar enkel fettansamling i levern, inflammerad ”fettig hepatit”, ärrbildning, skrumplever och till och med levercancer. MASLD är starkt kopplat till fetma, högt blodtryck och typ 2‑diabetes. Allt fler forskare har insett att fröna till denna sjukdom kan sås före födseln, när det utvecklande fostret exponeras för påfrestningar som dålig näring, föroreningar eller läkemedel. Denna idé — att tidiga livsmiljöer formar livslång sjukdomsrisk — är känd som ”utvecklingsursprunget för hälsa och sjukdom.” 
Prednison före födseln som det första anfallet
För att undersöka hur prenatalt prednison påverkar levern behandlade forskarna dräktiga råttor och möss med doser valda för att efterlikna låga kliniska doser som används hos människor. De följde sedan avkommorna före födseln och in i ung vuxen ålder. På egen hand var de nyfödda djuren som exponerats för prednison i livmodern mindre och visade redan tecken på onormalt fettupplägg i levern: fler fettkroppar, högre triglycerider i levern och sämre användning av fetter som energi. När avkommorna växte lagrade deras lever fortfarande mer fett än normalt, även vid vanlig kost. När djuren senare utsattes för en högfettkost — motsvarande ett västerländskt snabbmönster — blev skillnaderna dramatiska. Prednison‑exponerade avkommor utvecklade mer allvarlig fettleversjukdom, inflammation och hos hanarna tydliga tecken på ärrbildning. Deras blodsockerkontroll försämrades också, vilket indikerar bredare metabol problematik.
En skyddande leverprotein försvinner
Genom att gå djupare använde teamet storskalig genprofilering för att leta efter gemensamma molekylära förändringar i levern hos han‑ och honavkommor. En gen framträdde: Serpina3c, som kodar för ett utsöndrat protein tillhörande en familj av naturliga enzymhämmare. I båda könen minskade prenatalt prednison kraftigt och beständigt Serpina3c i levern och i blodet, från sen fosterstadium in i vuxen ålder. När forskarna avsiktligt sänkte Serpina3c endast i levern hos friska möss blev även dessa djur benägna att utveckla fettleversjukdom och dålig sockerhantering, särskilt vid högfettkost. Omvänt, att öka Serpina3c i levern hos prednison‑exponerade avkommor efter födseln återställde i stor utsträckning deras tillstånd: deras lever lagrade mindre fett, hanterade glukos bättre och visade mindre inflammation och ärrbildning.
Hur prednison omkopplar leverns kontrollknappar
Forskarna frågade sedan hur prenatalt prednison sänker Serpina3c. De fann att prednisonets aktiva form, prednisolon, överaktiverar glukokortikoidreceptorn — ett läkemedelssensoriskt protein som finns i leverceller. Denna receptor samarbetar sedan med ett annat protein, HDAC3, som stramar åt DNA‑paketeringen genom att ta bort små ”acetyl”‑märken från histonproteiner. I både djurlever och odlade leverceller ökade prednisolon glukokortikoidreceptor‑ och HDAC3‑aktivitet precis vid Serpina3c‑genen, vilket avlägsnade acetylmärken vid en nyckelplats kallad H3K27. När dessa markörer försvann sjönk genens aktivitet och Serpina3c‑proteinnivåerna föll. Blockering av receptorn eller HDAC3, eller hämning av deacetylering, återställde dessa acetylmärken, ökade Serpina3c och förbättrade fett‑ och sockerhanteringen i leverceller.
En skadlig kedjereaktion inne i levern
Låga nivåer av Serpina3c utlöste en sekundär skadlig kaskad. Under normala förhållanden hjälper Serpina3c till att dämpa enzymer som chymas som genererar hormonet angiotensin II direkt i vävnader. När Serpina3c var bristfällig ökade chymasnivåerna och aktiviteten, vilket producerade mer angiotensin II i levern och överaktiverade dess receptor, AT1R, på leverceller. Denna lokala hormonskov är känd för att driva oxidativ stress, insulinresistens, fettansamling, inflammation och ärrbildning. I både prednison‑exponerade djur och möss med lever‑specifik Serpina3c‑nedreglering var chymas–angiotensin II–AT1R‑vägen påslagen, och nyckelgener som normalt stödjer fettförbränning och glukosupptag var nedtryckta. Att återställa Serpina3c efter födseln tystade denna väg och återupplivade en sundare metabolism. 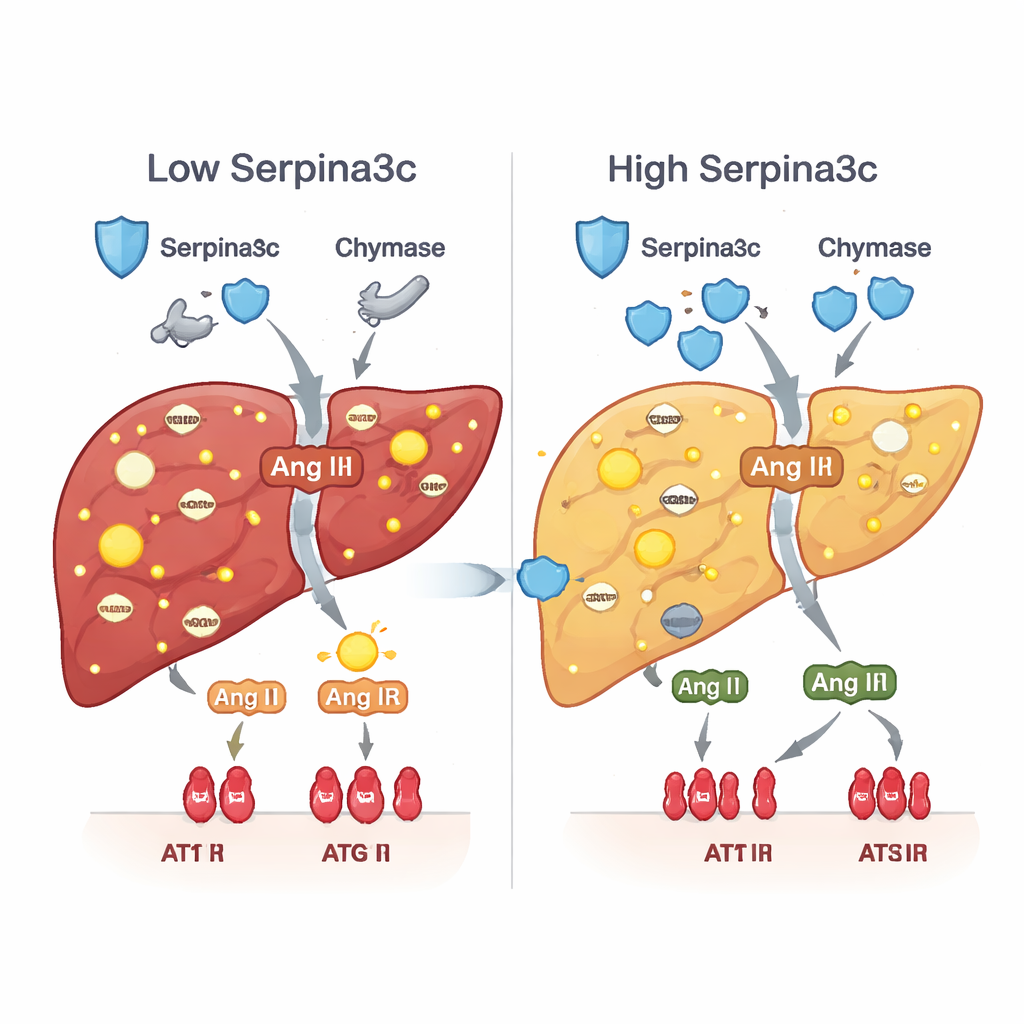
Vad detta innebär för patienter och familjer
För lekmän är huvudbudskapet att läkemedel som tas under graviditet kan lämna ett molekylärt fingeravtryck på den utvecklande levern som varar in i vuxen ålder. I denna studie fungerade prednison som ett ”första slag” och sänkte ett skyddande protein (Serpina3c) via epigenetiska förändringar — kemiska märken på DNA‑paketerande proteiner — så att ett senare ”andra slag” som en högfettkost lättare utlöste fettleversjukdom. Den uppmuntrande sidan är att denna risk inte var oföränderlig: att återhöja Serpina3c i levern efter födseln minskade leverbesvären markant. Även om dessa resultat kommer från gnagare väcker de viktiga frågor om hur vi övervakar och stödjer barn vars mödrar behövde prednison under graviditeten, och pekar på Serpina3c och chymas–angiotensin II‑systemet som lovande framtida måltavlor för att förebygga eller behandla fettleversjukdom som börjar före födseln.
Citering: Dai, Y., Lu, Z., Peng, Y. et al. Serpina3c protects against metabolic dysfunction-associated steatotic liver disease in offspring induced by prenatal prednisone exposure. Sig Transduct Target Ther 11, 71 (2026). https://doi.org/10.1038/s41392-025-02569-1
Nyckelord: prenatal prednison, fettleversjukdom, epigenetik, Serpina3c, utvecklingsursprung