Clear Sky Science · sv
Artros: molekylär patogenes och potentiella terapeutiska alternativ
När vardaglig ledvärk blir en helkroppshistoria
Ömma knän eller stela fingrar avfärdas ofta som en oundviklig del av åldrandet. Men artros — världens vanligaste ledsjukdom — är inte bara ”slitage”. Den här översiktsartikeln drar undan ridån och visar vad som verkligen pågår i smärtande leder, från felaktigt fungerande smärtnervceller till överbelastade cellulära maskiner, och undersöker en ny generation behandlingar som går långt utöver enkla smärtstillande medel.
En vanlig sjukdom med stora personliga kostnader
Artros drabbar nästan 8 % av världens befolkning, med hundratals miljoner människor som lever med kronisk smärta och försämrad rörlighet. Sjukdomen är vanligare hos kvinnor, hos personer över 55 år och hos dem som är överviktiga eller har jobb eller idrotter som utsätter lederna för tunga, upprepade belastningar. Dagens standardvård — träning, viktminskning, ortoser, antiinflammatoriska tabletter, ledinjektioner och i svåra fall ledprotes — kan lindra symtomen men stoppar sällan sjukdomens gradvisa förlopp. Denna klyfta mellan behov och tillgänglig behandling har fått forskare att undersöka mycket djupare hur artros startar och varför det gör så ont.
Varför leden gör ont: ledningar, kemikalier och signaler
Smärta vid artros förklaras inte av röntgenbilder ensam: vissa med måttliga förändringar har stark smärta, medan andra med svåra förändringar rapporterar lite smärta. Artikeln följer smärtans väg från knäleden upp genom ryggmärgen till hjärnan. Nervändar i leden — särskilt tunna Aδ- och C-fibrer — badar i en soppa av inflammatoriska kemikalier, inklusive interleukiner och tumörnekrosfaktor, samt nervtillväxtfaktor. Dessa substanser slår på speciella kanaler i nervändarna som släpper igenom natrium och kalcium, vilket gör att nerverna avfyrar lättare och oftare. Med tiden kan smärtbanor i ryggmärgen och hjärnan bli överkänsliga, så att normal rörelse eller måttlig kyla känns skarp och brännande.
Den dolda arbetsbelastningen inne i ledcellernas inre
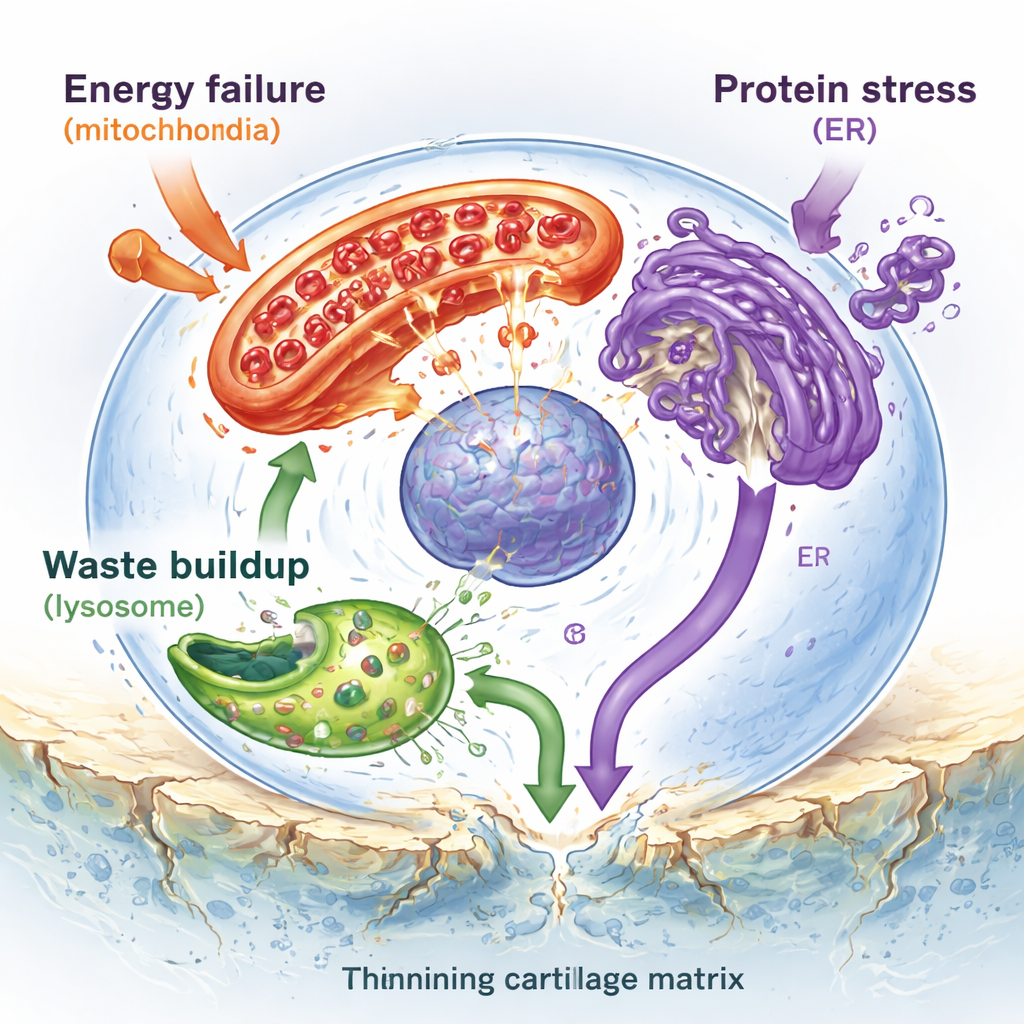
Långt inne i brosket försöker de enda invånarna — kondrocyterna — upprätthålla en slät, fjädrande matrix som låter benen glida. Författarna visar att dessa celler utsätts för angrepp på flera fronter. Mitokondrierna, cellens små kraftverk, blir skadade och mindre effektiva, producerar för lite energi och för många reaktiva syrearter som skadar DNA och proteiner. Lysosomerna, cellens återvinningscentraler, överbelastas av hårda mineraliska kristaller, vilket försvagar deras membran så att destruktiva enzymer läcker ut i cellen och utlöser celldöd. Det endoplasmatiska retiklet, ett membranlabyrint där nya proteiner viks, blir blockerat av felvikta molekyler och sätter igång en kronisk ”stressrespons” som så småningom driver cellerna mot självdestruktion. Tillsammans matar dessa stressade organeller inflammation och accelererar förlusten och förkalkningen av brosk.
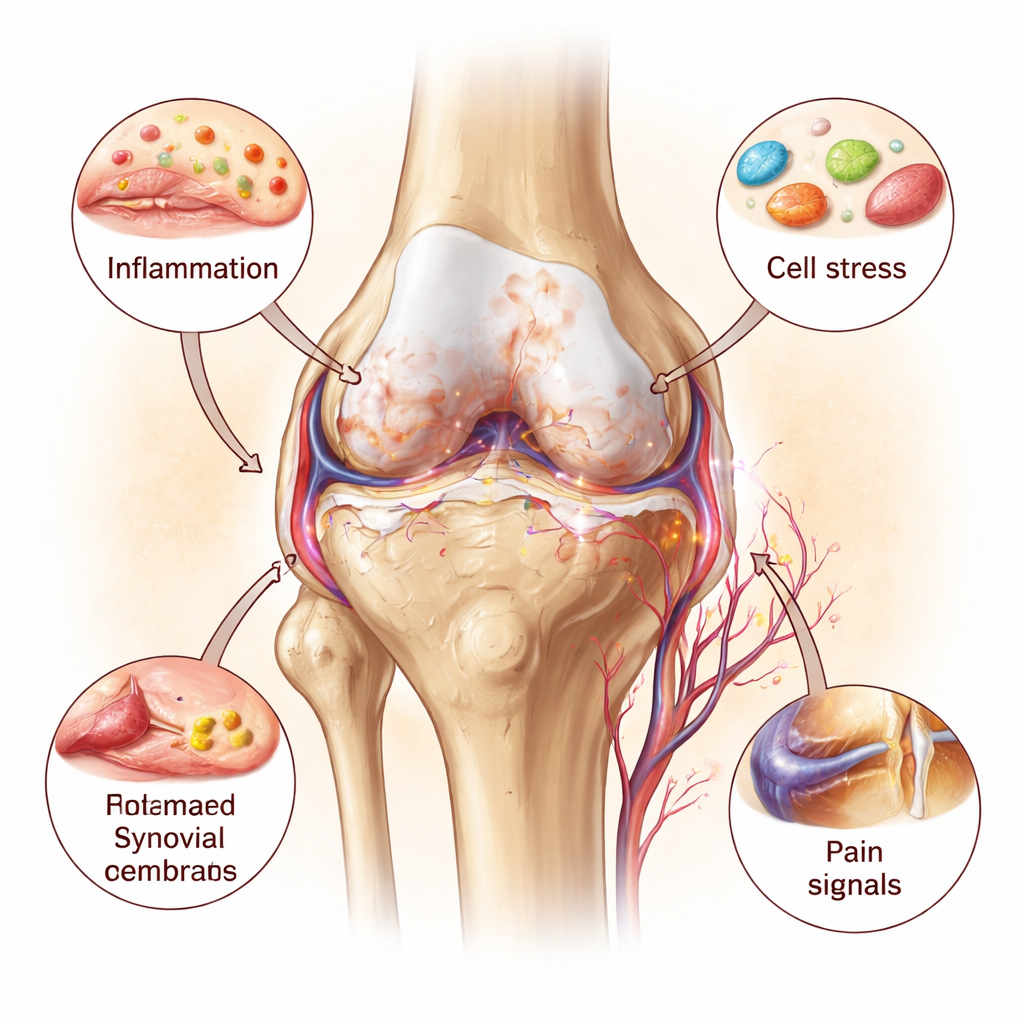
Inflammation: bränsle på elden
Inflammatoriska budbärarmolekyler är denna process megafoner. Tre i synnerhet — interleukin‑1, interleukin‑6 och tumörnekrosfaktor‑alfa — bildar en ond cirkel med organellskador. De driver kondrocyterna att producera enzymer som bryter ned brosk och uppmuntrar onormal benbildning under ledytan. Samtidigt släpper skadade mitokondrier och läckande lysosomer ut sina egna nödsignaler, vilka ytterligare aktiverar immunsensorer inne i leden. Blodkärl och smärtfibrer växer in i områden av brosk som normalt är tysta och utan nerver, vilket höjer smärtkänsligheten. Denna helledsbild skildrar artros som en långsamt framryckande men självförstärkande inflammatorisk sjukdom, inte som en passiv mekanisk nedslitning av brosk.
Nya behandlingsidéer: från jonkanaler till cellens kraftverk
Beväpnade med denna mekanistiska karta testar forskare nya läkemedel och leveranssystem. På smärtsidan blockerar eller avkänsligar experimentella medel nervkanaler såsom TRPV1 (capsaicinreceptorn), TRPA1, TRPM3/8 och specifika natriumkanaler (Nav1.7 och Nav1.8), eller neutraliserar nervtillväxtfaktor för att förhindra att nerver blir hyperkänsliga. På sjukdomsmodifierande sidan syftar riktade antikroppar till att dämpa nyckelcytokiner, medan småmolekyler och ”senolytiska” medel försöker återställa hälsosammare cellbeteenden. En särskilt spännande front är organellriktad terapi: föreningar som stimulerar mitokondriell städning (mitofagi), stabiliserar lysosomala pH och membran eller mildrar stress i det endoplasmatiska retiklet. Raffinerade nanopartiklar, liposomer och konstruerade exosomer designas för att rikta in sig på kondrocyter och till och med specifika organeller, för att leverera läkemedel exakt där de behövs.
Vad detta betyder för personer som lever med artros
Artikeln avslutar med att artros bör ses och behandlas som en komplex biologisk störning som involverar rubbad cellmetabolism, kronisk låggradig inflammation och maladaptiv smärtmappning. Många av de föreslagna läkemedlen och leveranssystemen befinner sig fortfarande i tidig laboratorie‑ eller djurstudiefas, men de pekar mot en framtid där behandling blir både multimodal och individualiserad: lindra smärta genom att dämpa överaktiva nerver samtidigt som ledens egna celler och deras interna maskineri skyddas eller föryngras. För patienter skulle detta så småningom kunna innebära terapier som inte bara gör rörelse mindre smärtsam, utan också bromsar eller möjligtvis vänder den strukturella skada som i dag ofta anses oundviklig.
Citering: Zhang, Y., Han, Y., Sun, Y. et al. Osteoarthritis: molecular pathogenesis and potential therapeutic options. Sig Transduct Target Ther 11, 81 (2026). https://doi.org/10.1038/s41392-025-02556-6
Nyckelord: artros, ledsmärta, brosk, inflammation, mitokondrier