Clear Sky Science · sv
Upptäckt och utveckling av antivirala läkemedel: utmaningar och framtida riktningar
Varför vi fortfarande behöver bättre virusbekämpande läkemedel
COVID-19-pandemin visade hur snabbt ett nytt virus kan rubba vardagen — och hur mycket vi fortfarande är beroende av effektiva läkemedel när vacciner inte räcker. Denna översiktsartikel ser tillbaka över 60 års utveckling av antivirala läkemedel och ställer frågan: hur kan vi bygga snabbare, smartare och bredare skydd mot framtida virushot? Den förklarar på ett tillgängligt sätt hur forskare upptäcker, designar och levererar antivirala läkemedel, vad man lärde sig av COVID-19, och hur verktyg som artificiell intelligens och nanoteknik kan förändra spelplanen.
Från de första antivirala läkemedlen till dagens arsenal
Antiviral medicin är ett relativt ungt fält. Det första godkända läkemedlet, idoxuridin på 1960‑talet, visade att man genom att förändra DNA:s byggstenar kunde bromsa viral replikation, men det skadade också friska celler och kunde därför bara användas i ögat. Senare kom acyklovir, ett banbrytande läkemedel mot herpes som främst aktiveras inne i infekterade celler, vilket gör det både kraftfullt och säkert. På 1980‑talet blev zidovudin den första behandlingen för HIV, vilket öppnade dörren för moderna kombinationsterapier som idag gör HIV till ett hanterbart kroniskt tillstånd. Under årtiondena har bättre kemi och datorstödd design bidragit till mer precisa läkemedel mot influensa, hepatit B och C, HIV och, senast, SARS‑CoV‑2. Översikten beskriver denna tidslinje och visar hur varje genombrott introducerade ett nytt sätt att överlista virus.
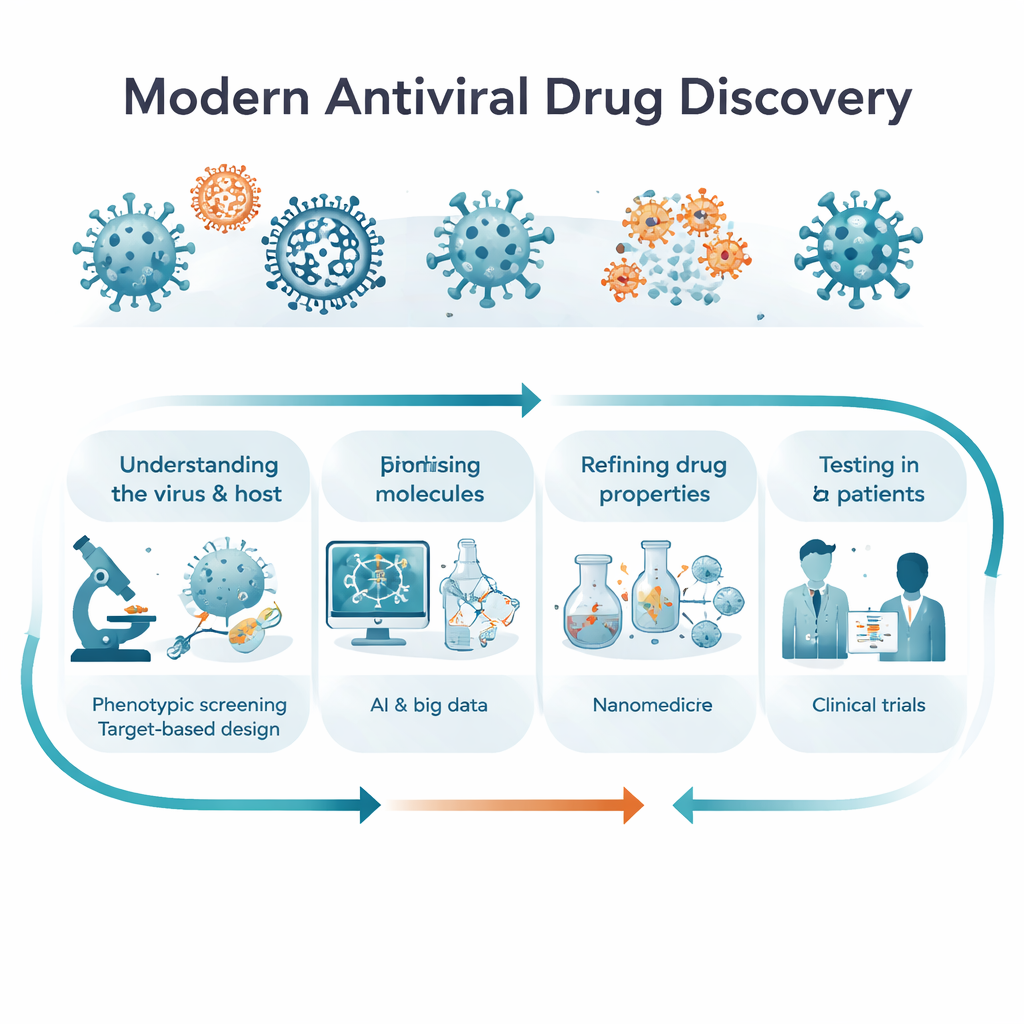
Två sätt att hitta ett bra läkemedel: observera celler kontra sikta på mål
Forskare följer i allmänhet två kompletterande vägar för att hitta nya antivirala medel. I den ”fenotypiska” upptäckten utgår man inte från ett specifikt protein; istället utsätter man infekterade celler eller modellorganismer för tusentals molekyler och frågar helt enkelt: vilka håller viruset i schack och cellerna vid liv? Detta kan avslöja överraskande, först-i-sitt-slag-läkemedel, inklusive sådana som verkar via mer än en väg. I den ”målinriktade” upptäckten identifierar forskare först ett viralt eller mänskligt protein som är avgörande för infektion—till exempel en polymeras, ett proteas eller en immunsignal—och designar sedan molekyler för att blockera eller modulera det målet. Artikeln förklarar hur dessa strategier skiljer sig åt, varför de spelar roll i olika skeden av forskningen, och hur framtida projekt troligen kommer att blanda dem och röra sig smidigt från bred observation till precis molekylär förståelse.
Att träffa viruset — och dess stödsystem — där det gör ont
Moderna antivirala medel gör långt mer än att bara täppa till ett enda viralt enzym. Översikten går igenom virusets livscykel, från inträde i cellen till kopiering av genomet och frisättning, och lyfter fram läkemedelstyper som stör vid varje steg. Vissa föreningar binder direkt till virala enzymer eller strukturella proteiner. Andra verkar genom att rikta in sig på värdfaktorer som virusen är beroende av — såsom cellmembranreceptorer, viktiga metaboliska enzymer eller medfödda immunsignaler som interferoner och toll‑liknande receptorer. Genom att verka på värdens ”hjälpproteiner” kan dessa läkemedel minska risken att snabbt muterande virus undkommer. Författarna beskriver också framväxande idéer som små molekyler som stör membranlösa ”droppar” inne i celler där virus monteras, eller som selektivt bryter ner virala proteiner och RNA istället för att bara blockera dem.
Designa bättre molekyler: form, egenskaper och leverans
Att omvandla ett initialt ”hit” till ett användbart läkemedel handlar om mer än att maximera potens. Kemister justerar molekylers form och laddning så att de passar sina mål som nyckel i lås, ofta med vägledning av högupplösta proteinstrukturer och simuleringar. De finjusterar även vattenslöslighet, stabilitet och metabolism för att säkerställa att läkemedlet når rätt vävnad, förblir aktiv tillräckligt länge och undviker onödig toxicitet. Artikeln ger exempel på hur små förändringar — som att lägga till en sidokedja eller bilda ett salt — kan öka aktiviteten mot resistenta HIV‑ eller koronavirusstammar samtidigt som säkerheten förbättras. Den förklarar också prodrugs, som är inaktiva eller mindre aktiva former designade att omvandlas i kroppen, och målinriktade leveranssystem såsom leverriktade sockertaggning och lipidnanopartiklar som tryggt för fram ömtålig mRNA eller nukleinsyra‑läkemedel in i celler.
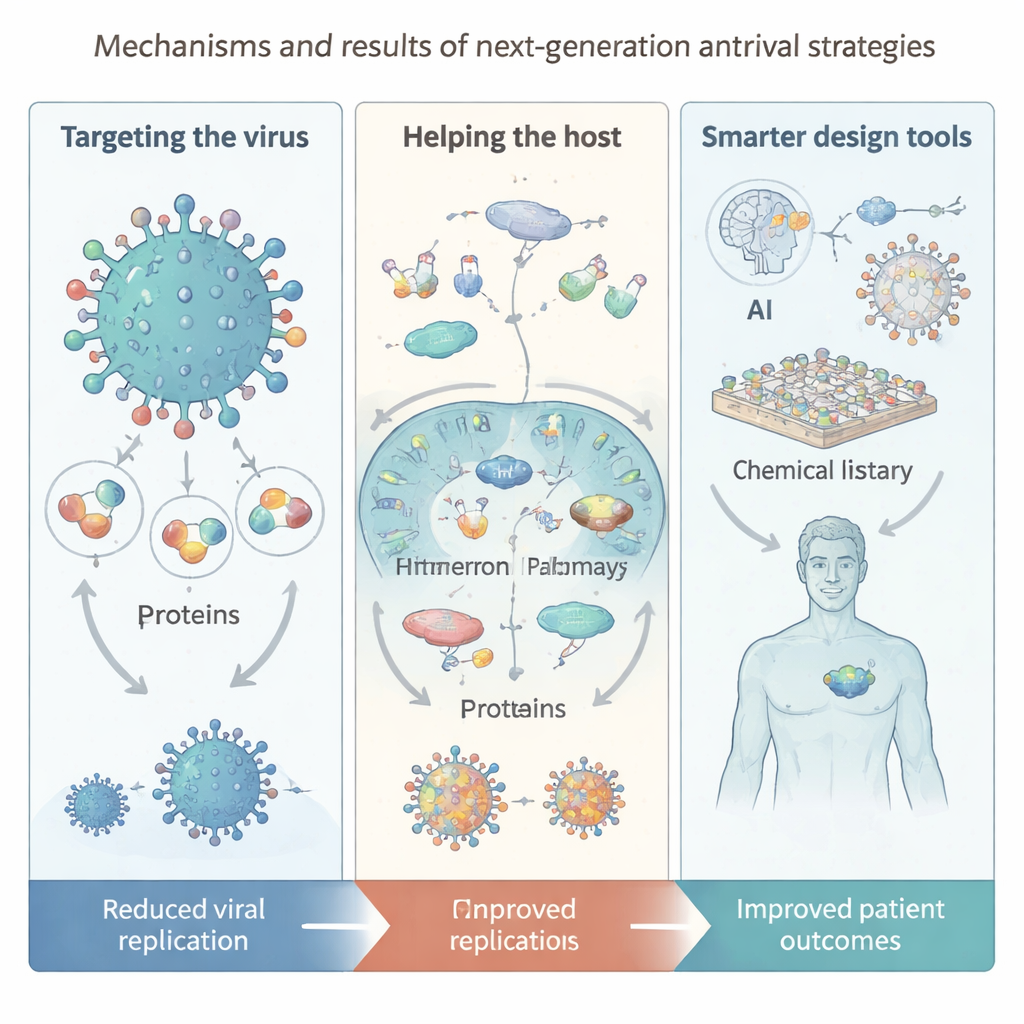
Nya verktyg: artificiell intelligens, enorma bibliotek och nanoteknik
Ett huvudtema i översikten är hur tekniken omformar upptäckten av antivirala medel. Artificiell intelligens hjälper nu till att förutsäga proteinstrukturer, söka i enorma ”virtuella” bibliotek med miljarder möjliga molekyler och föreslå nya föreningar eller läkemedelskombinationer. DNA‑kodade bibliotek och plattformar för makrocykliska peptider möjliggör ultrarapid screening av enorma kemiska rum, medan automatiserade syntes‑ och reningssystem påskyndar bygg‑och‑test‑loopen. På leveranssidan erbjuder nanoteknik virusliknande partiklar, smarta polymerer och ”nanozymes” som kan skada virala höljen direkt eller skärpa immunsvaret. Samtidigt varnar författarna för att AI‑modeller fortfarande är beroende av högkvalitativa data, att många genererade molekyler är svåra att framställa eller testa, och att frågor om säkerhet, rättvisa och integritet måste hanteras i takt med att dessa verktyg blir mer centrala.
Vart upptäckten av antivirala läkemedel är på väg
För en lekmannaläsare är artikelns huvudbudskap både dämpat och hoppfullt. Virus muterar snabbt, och ingen enda tablett kommer att fungera för evigt eller mot varje hot. Men genom att lära av COVID‑19, fördjupa vår förståelse för virus–värd‑interaktioner och kombinera smart kemi, avancerad biologi, AI och nanoteknik bygger forskare ett mer rörligt antiviralt verktygslåda. Framtida behandlingar kommer sannolikt att vara bredare i räckvidd, bättre tolererade och anpassade för att träffa inte bara viruset utan också de sårbara ”svaga punkterna” i infektionsprocessen. Fortsatt samarbete över discipliner, industrier och länder kommer att vara avgörande för att omvandla dessa vetenskapliga framsteg till prisvärda, praktiska läkemedel innan nästa pandemi inträffar.
Citering: Du, S., Hu, X., Li, P. et al. Antiviral drug discovery and development: challenges and future directions. Sig Transduct Target Ther 11, 69 (2026). https://doi.org/10.1038/s41392-025-02539-7
Nyckelord: upptäckt av antivirala läkemedel, COVID-19-terapier, värdriktade antiviraler, artificiell intelligens i läkemedelsdesign, nanoteknik inom medicin