Clear Sky Science · sv
Fototerapisystem baserade på nanopartiklar: molekylära mekanismer och kliniska tillämpningar
Ljus som ett skonsamt medicinskt verktyg
De flesta av oss tänker på ljus som något som låter oss se, värmer huden eller driver solpaneler. Denna översiktsartikel utforskar en mer överraskande roll: att använda noggrant avvägt ljus tillsammans med små konstruerade partiklar för att diagnostisera och behandla sjukdomar inifrån och ut. Författarna beskriver hur ”nanopartikelbaserad fototerapi” kan fokusera skada på cancerceller, dämpa inflammation i hjärta och leder och till och med hjälpa hjärnan att rensa giftiga proteiner vid tillstånd som Alzheimers sjukdom — allt medan större delen av frisk vävnad sparas.
Hur små partiklar förvandlar ljus till medicin
I centrum för denna metod finns nanopartiklar — strukturer tusentals gånger smalare än ett människohårs tjocklek — som kan bära läkemedel, absorbera ljus och omvandla det till antingen värme eller kortlivade kemiska utsläpp. Två huvudstrategier dominerar. I fotodynamisk terapi alstrar ljusaktiverade molekyler på eller inuti nanopartikeln reaktiva syrearter — energirika syreformer som perforerar närliggande cellkomponenter. I fototermisk terapi omvandlar andra partiklar, såsom guld eller svart fosfor, nära-infrarött ljus till värme och ”kokar” därmed kortvarigt tumörceller från insidan. Eftersom ljuset kan riktas och partiklarna kan designas för att ackumulera huvudsakligen i sjuka vävnader får läkare en nivå av rumslig precision som traditionell kemoterapi och strålbehandling saknar. 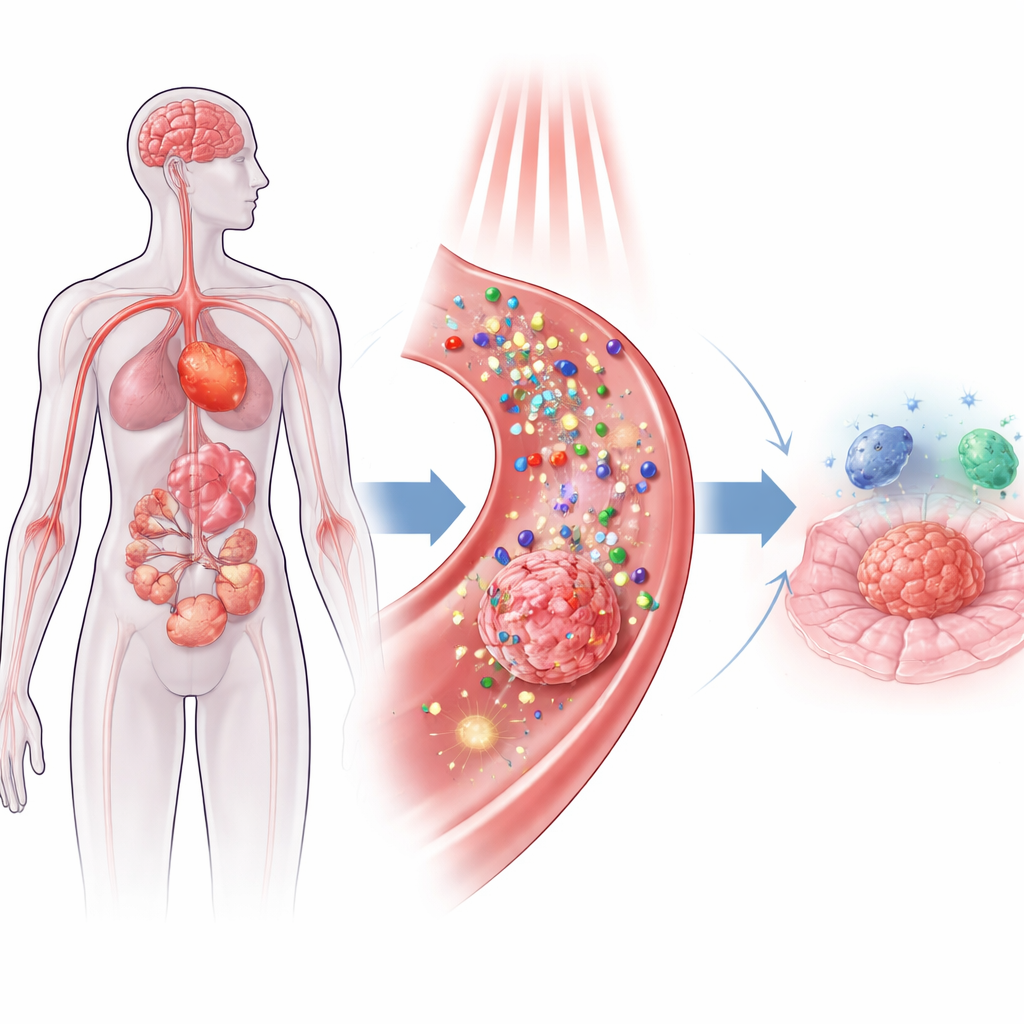
Bygga smartare bärare och leveransvägar
Att bara belysa kroppen räcker inte; utmaningen är att få rätt partiklar till rätt plats och hålla dem där tillräckligt länge för att verka. Översikten katalogiserar ett verktygslåda med leveranssystem, inklusive mjuka bärare såsom liposomer, fasta lipidpartiklar och polymerbaserade sfärer eller miceller, liksom styva stommar gjorda av kiseldioxid, metaller, kol eller metall‑organiska ramverk. Deras ytor kan beläggas med ”stealth”-polymerer för att förlänga cirkulationen, med naturliga cellmembran för att undkomma immunsystemet eller med ”adress-taggar” som känner igen markörer på cancer- eller inflammerade celler. Vissa konstruktioner är ”smarta”: de förblir inerta i blodomloppet men ändrar storlek, laddning eller form som svar på surhet, enzymer eller redoxförhållanden inne i en tumör och släpper ut sitt innehåll endast där det behövs.
Vad som händer inne i celler när ljuset slår till
När ljuset sätts på vecklas en kaskad av molekylära händelser ut. Författarna förklarar hur ljusexciterade partiklar genererar oxidantutbrott som attackerar membran, DNA och vitala strukturer som mitokondrier och lysosomer. Detta kan få celler att gå in i ordnad självdöd (apoptos), eller, när skadan är allvarlig, i mer kaotisk död. Celler kan också öka autofagi, en form av intern återvinningsprocess som antingen hjälper dem överleva mild stress eller påskyndar deras undergång när de överbelastas. Avgörande är att döende tumörceller kan avge ”fara”-signaler som samlar immunsystemet: exponera vissa proteiner på ytan, släppa ut faktorer som attraherar dendritiska celler och omforma tumörassocierade immunceller från en undertryckande till en tumörbekämpande status. I praktiken kan en lokal ljusbehandling fungera som ett personligt cancervaccin. 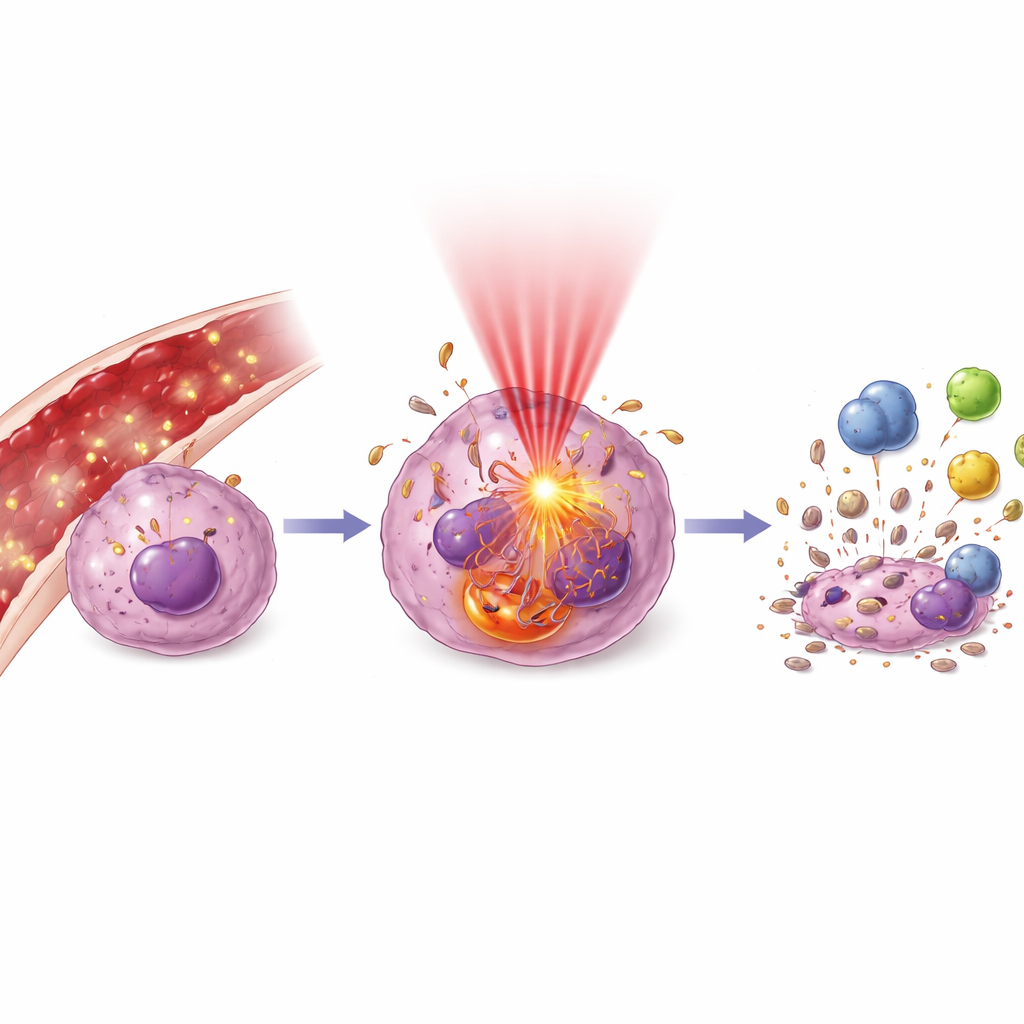
Bortom cancer: hjärta, hjärna och autoimmuna mål
Även om cancer är det mest avancerade fältet, anpassas samma principer till kroniska tillstånd. Vid hjärt‑kärlsjukdom syftar ljusbaserade angreppssätt inte till att döda celler utan att minska oxidativ stress, stabilisera kärlbeklädnadsceller och till och med hjälpa till att krympa eller hårdna farliga plack. I hjärnan, där neuroner är mycket känsliga, syftar mildare ljusregimer — ofta kallade fotobiomodulation — till att öka mitokondriell energiproduktion, minska toxiska proteinansamlingar och dämpa mikroglia‑ och astrocyt‑driven inflammation. Översikten lyfter också fram tidiga arbeten inom metabola och autoimmuna sjukdomar, där noggrant doserat ljus och nanopartiklar kan knuffa immunceller bort från aggressivt, vävnadsskadeframkallande beteende och mot mer reglerande, lugnande roller, samtidigt som insulinkänslighet och signalering i fettväv modest förbättras.
Från labbet till kliniken: löften och hinder
Trots årtionden av forskning är endast ett fåtal ljusaktiverade läkemedel fullt godkända, mest för ögonsjukdomar och vissa tumörer. Författarna menar att nanoteknik börjar låsa upp nästa våg, möjliggör djupare ljuspenetration, bättre målinriktning och inbyggd avbildning för att övervaka behandling i realtid. Ändå återstår stora hinder: att skala upp nanopartikelproduktion med konsekvent kvalitet, bevisa långtidssäkerhet och utsöndring från kroppen, leverera ljus effektivt till djupa organ och uppfylla strikta regulatoriska krav. Översikten slutar med slutsatsen att genom att förena materialvetenskap, optik, biologi och AI‑styrd design står nanopartikelbaserad fototerapi redo att utvecklas från nischade procedurer till en bredare, icke‑invasiv pelare inom precisionsmedicin.
Citering: Chauhan, D.S., Prasad, R., Dhanka, M. et al. Nanoparticles-based phototherapy systems: molecular mechanisms and clinical applications. Sig Transduct Target Ther 11, 95 (2026). https://doi.org/10.1038/s41392-025-02536-w
Nyckelord: nanopartikel-fototerapi, fototermisk terapi, fOTODYNAMISK terapi, cancer-nanomedicin, fotobiomodulation