Clear Sky Science · sv
IFFO1 hämmar bröstcancer genom att samordna mitokondriell fission och fettsyrasyntes via LaminA/C–PGC1α-axeln
Varför denna forskning är viktig
Bröstcancer är fortfarande en av de ledande orsakerna till cancerrelaterad död bland kvinnor, i stor utsträckning eftersom vissa tumörer fortsätter växa, sprida sig och överlista nuvarande behandlingar. Denna studie avslöjar en tidigare underskattad cellulär “broms” kallad IFFO1 som saktar ner bröstcancer genom att tygla två centrala motorer för tumörtillväxt: cellens energifabriker, mitokondrierna, och dess förmåga att tillverka och lagra fetter. Att förstå denna broms ger en ny ingång för terapier som kan fungera över flera subtyper av bröstcancer.
En dold väktare i bröstceller
Forskarna började med att undersöka prover från 30 kvinnor med bröstcancer samt stora offentliga cancer-databaser. De fann att nivåerna av proteinet IFFO1 konsekvent var lägre i tumörvävnad än i närliggande normal bröstvävnad. Ju mer avancerad cancerscenen var, desto mindre IFFO1 fanns, och patienter vars tumörer hade högre IFFO1 tenderade att leva längre. I odlad bröstcancerceller minskade tvångsuttryck av IFFO1 kraftigt cellernas förmåga att växa, dela sig och migrera — beteenden som krävs för att tumörer ska expandera och sprida sig. IFFO1 dämpade också ett cellulärt program känt som epitelial–mesenkymal omvandling, vilket hjälper cancerceller att lossa och invadera annan vävnad.
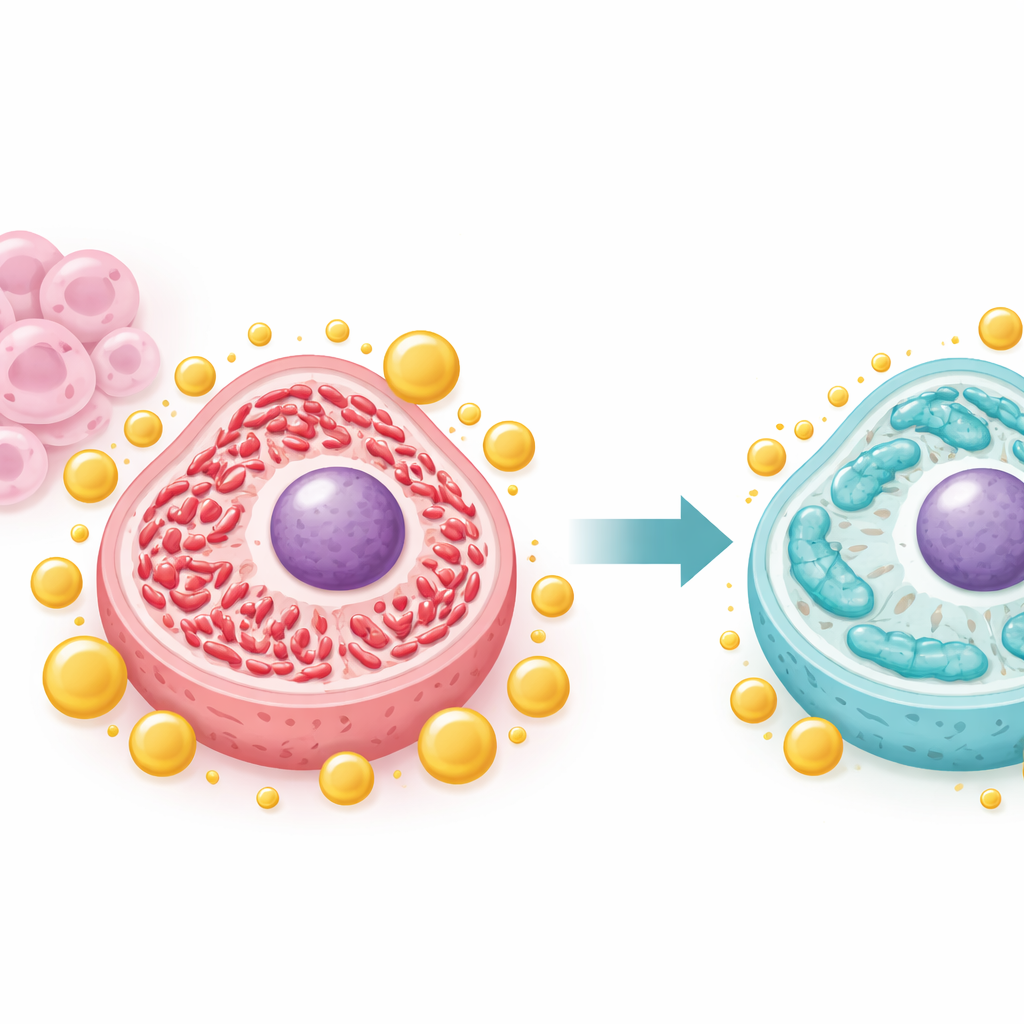
Att lugna överaktiva energifabriker
Cancerceller omformer ofta sina mitokondrier, de små kraftverken i cellerna, för att driva snabb tillväxt. Teamet visade att IFFO1 skjuter balansen bort från ett starkt fragmenterat, ”fissions”-tillstånd mot ett mer förlängt, ”fusions”-tillstånd som generellt sett är förknippat med friskare och mer stabila mitokondrier. När IFFO1 var rikligt minskade viktiga fissionsproteiner som Drp1 och Fis1, medan fusionsproteiner ökade. Mikroskopi visade att mitokondrierna blev längre och mindre fragmenterade, och mått på mitokondriellt DNA och energiutbyte sjönk från de abnormt höga nivåerna som ses i aggressiva celler. Dessa förändringar tyder på att IFFO1 förhindrar att mitokondrier går in i en hyperaktiv konfiguration som stöder okontrollerad tumörtillväxt.
Att kapa fettleveransen
Snabbväxande tumörer behöver inte bara energi; de behöver också en stadig tillgång på fetter för att bygga nya membran och signalsubstanser. Studien fann att IFFO1 också trycker ner denna metabola gaspedal. I celler med extra IFFO1 minskade centrala fettbyggande proteiner — inklusive FASN, SREBP‑1, SCD1 och andra. Enzymtester bekräftade lägre fettsyntetisk aktivitet, och kemiska analyser visade minskningar i fria fettsyror, triglycerider och kolesterol. Färgämnen som markerar fettförråd visade färre lipidkorn och mindre totalt neutralt fett inne i cancercellerna. Omvänt gav ökande av fissionsproteinet Drp1 motsatt effekt och ökade fettproduktionen, medan tystning av Drp1 dämpade den — vilket stödjer en direkt koppling mellan mitokondriernas form och fettillgång i cancer.
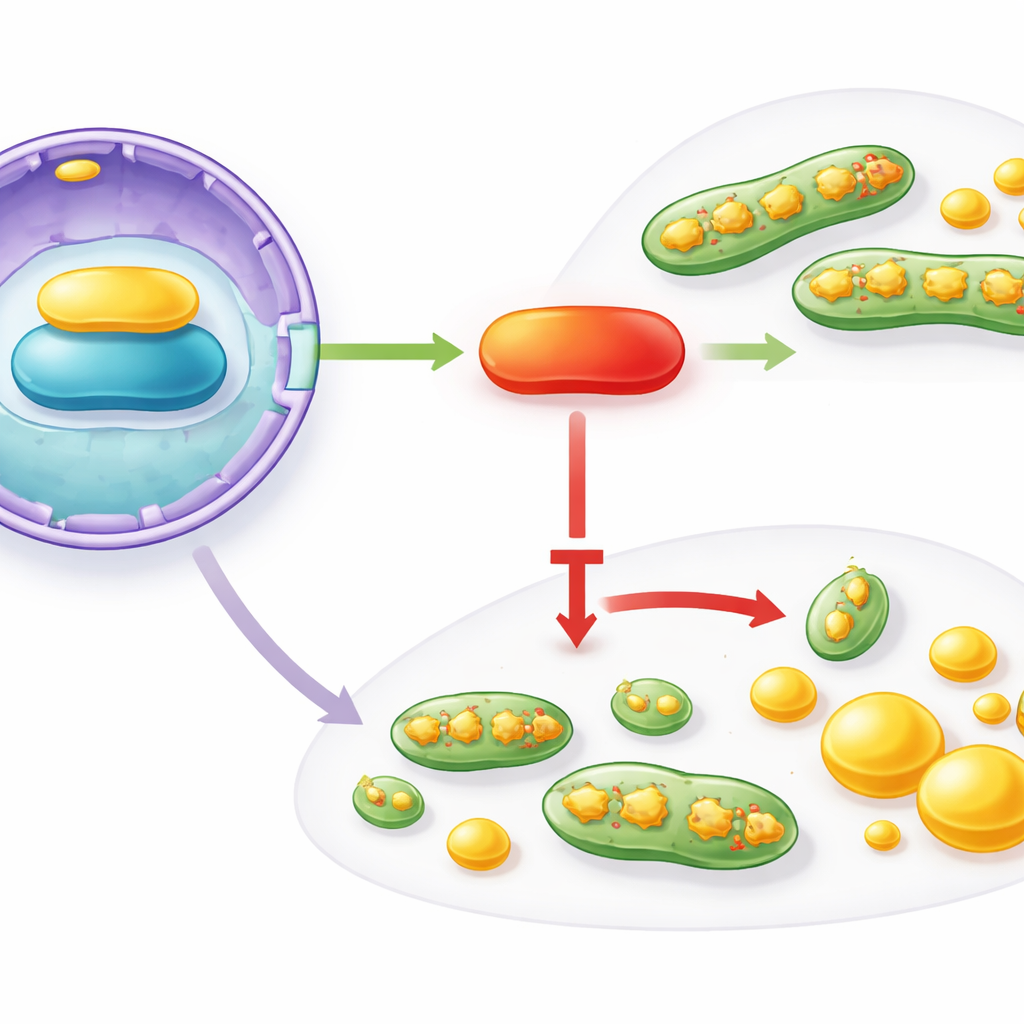
En signaleringskedja från kärnan till mitokondrierna
Hur orkestrerar IFFO1 dessa omfattande förändringar? Författarna följde en kedja av interaktioner som börjar i cellkärnan och slutar vid mitokondrierna och fettbildande maskineriet. IFFO1 binder fysiskt till ett strukturellt protein i kärnans omslag kallat Lamin A/C och ökar dess nivåer. Lamin A/C stödjer i sin tur aktiviteten hos PGC1α, en huvudregulator som övervakar mitokondriell hälsa och metabolism. I bröstcancervävnader och celler fann man att både Lamin A/C och PGC1α var minskade, i linje med förlusten av IFFO1. När forskarna artificiellt ökade IFFO1 steg Lamin A/C och PGC1α, mitokondriell fission minskade och fettsyntesen avtog. Nedreglering av Lamin A/C utsuddade dessa fördelar, men återställande av PGC1α återförde dem, vilket pekar ut en funktionell IFFO1 → Lamin A/C → PGC1α-axel som begränsar tumörfrämjande mitokondriella och lipida förändringar.
Att testa bromsen i levande djur
För att se om dessa cellulära effekter översätts till verkliga tumörer implanterade teamet humana bröstcancerceller med eller utan extra IFFO1 i möss. Tumörer med förstärkt IFFO1 växte långsammare, vägde mindre vid experimentets slutpunkt och visade färre tecken på fettansamling. I en separat modell där cancerceller injicerades i blodomloppet för att etablera lungmetastaser bildade celler som överproducerade IFFO1 avsevärt färre lungtumör-noduli. Vävnadsanalyser från dessa möss upprepade fynden från cellodlingarna: högre Lamin A/C och PGC1α, mindre mitokondriell fission och lägre fettsyntes.
Vad detta betyder för framtida behandlingar
Sammantaget presenterar arbetet IFFO1 som en flerskiktad tumörsuppressor som kopplar cellens strukturella skelett, dess energifabriker och dess fettbildande maskineri. Genom att stabilisera Lamin A/C och öka PGC1α håller IFFO1 mitokondrierna från att fragmenteras överdrivet och kapar överproduktionen av fetter som cancerceller är beroende av. För icke-specialister är huvudbudskapet att detta protein fungerar som en intern broms på både kraften och byggstenarna som driver bröstcancer tillväxt och spridning. Läkemedel som höjer IFFO1-nivåer eller efterliknar dess effekter på Lamin A/C–PGC1α-vägen skulle en dag kunna erbjuda nya alternativ, särskilt för aggressiva eller behandlingsresistenta former av bröstcancer.
Citering: Cai, H., He, J. IFFO1 inhibits breast cancer by coordinating mitochondrial fission and fatty acid synthesis via the LaminA/C-PGC1α axis. Oncogenesis 15, 16 (2026). https://doi.org/10.1038/s41389-026-00609-1
Nyckelord: bröstcancer, mitokondriell dynamik, fettsyrasyntes, tumörmetabolism, PGC1α-vägen