Clear Sky Science · sv
Onkogentisk kontroll av nukleotidsyntes
Varför cancerceller bryr sig om byggstenarna
Cancer beskrivs ofta som celler som inte slutar dela sig. Men för att kopiera sig själva behöver dessa celler en ständig tillförsel av små byggstenar kallade nukleotider, som bygger upp DNA och RNA och också driver många cellulära processer. Denna översikt förklarar hur cancerframkallande gener omskapar cellens kemi för att hålla nukleotidproduktionen hög, hur tumörer växlar mellan olika sätt att skaffa dessa molekyler, och hur läkare kan utnyttja dessa knep med gamla och nya läkemedel.
Två vägar till samma byggstenar
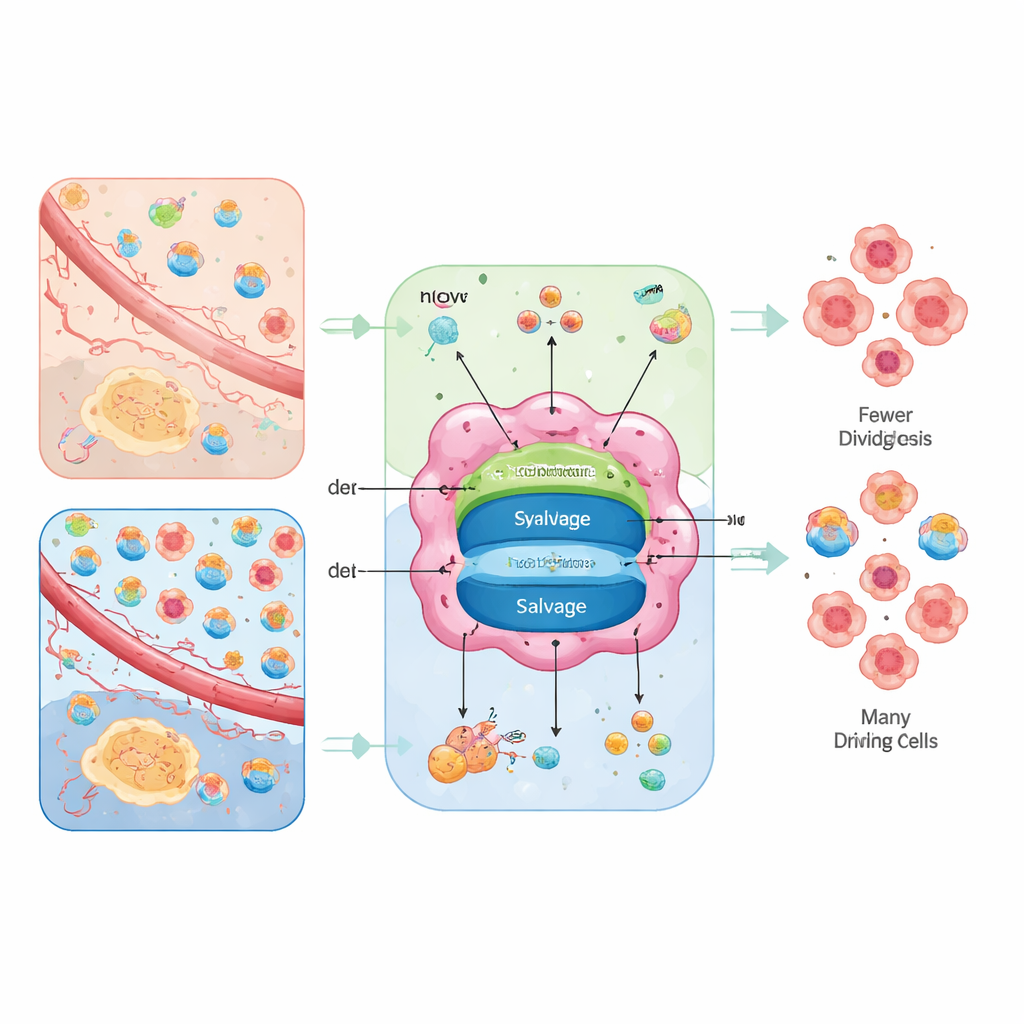
Celler kan tillverka nukleotider från grunden eller återvinna dem. "Från grunden"-vägen, kallad de novo-syntes, bygger ringarna från grundläggande näringsämnen som glukos, aminosyror, koldioxid och bikarbonat, med energiintensiva, flerstegsreaktioner. Återvinningsvägen, kallad salvage, tar sönderdelade baser och nukleosider från omgivningen eller från cellens avfall och sätter tillbaka dem till användbara nukleotider med mycket lägre energikostnad. Tumörer använder båda alternativen, men balansen mellan dem beror på deras interna energitillgång och vad den omgivande vävnaden förser dem med.
Hur tumörmiljön styr valet
Författarna ramar in nukleotidförsörjningen som ett "miljöformt ruttnings"-problem. I dåligt försörjda regioner där aminosyror finns men fria nukleosider är knappa, lutar cancerceller starkt mot de novo‑vägar och blir sårbara för läkemedel som blockerar dessa steg. I bättre perfunderade områden, där blodet levererar gott om nukleosider eller där mitokondrier är svaga, kan tumörer förlita sig mer på salvage och blir istället känsliga för transportörhämmare som förhindrar nukleosidupptag. När båda alternativen är öppna uppvisar tumörer metabol flexibilitet och kan undvika enkla läkemedel; när båda är stängda stannar cellerna i DNA-replikation, ackumulerar skador och kan dö eller omvandla sig till mer mogna, mindre aggressiva tillstånd.
Dolda stödlänkar som matar nukleotidförsörjningen
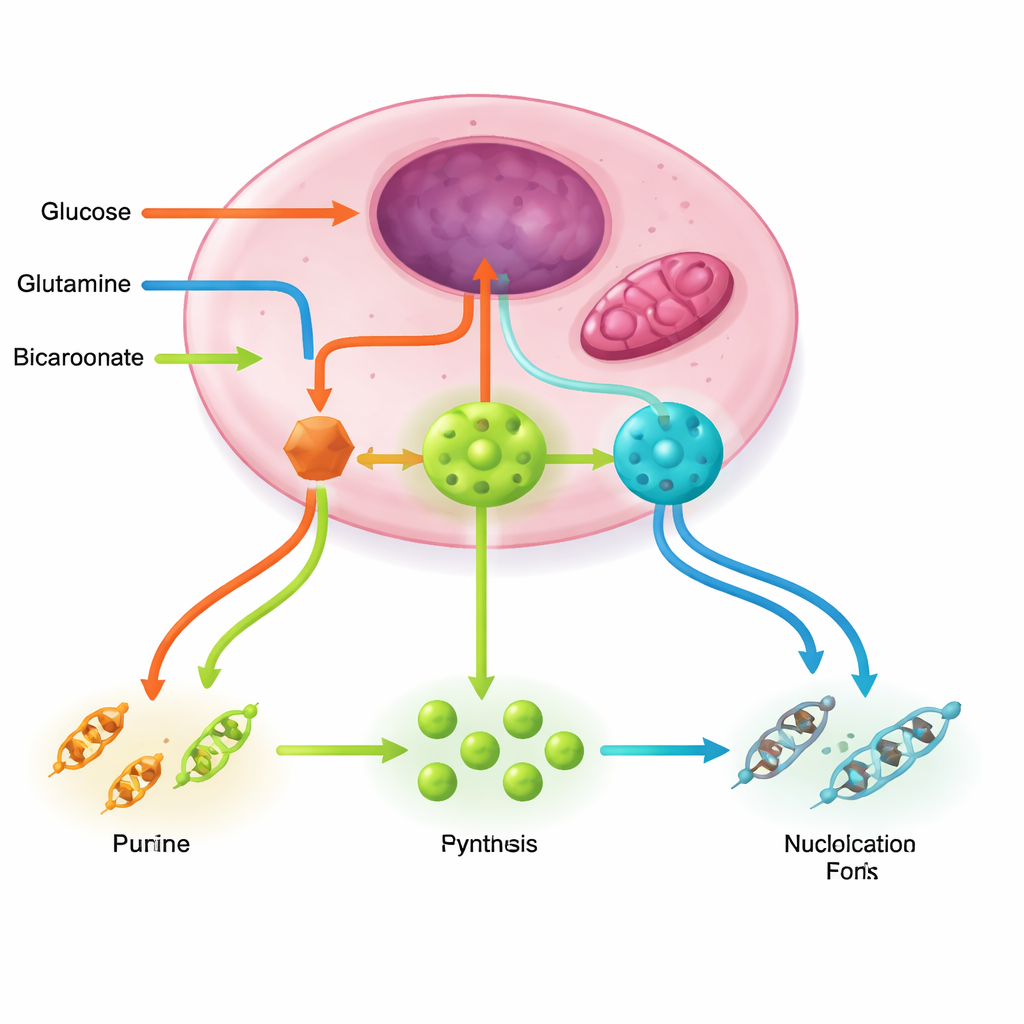
Att hålla nukleotidfabriker igång kräver flera stödkretsar. Pentosfosfatvägen förser sockerstommen och reducerande kraft; glutamin och den energiproducerande cykeln i mitokondrierna tillhandahåller kväve och aspartat; serin-, glycin- och folatkemi donerar enkolsenheter som färdigställer ringarna; bikarbonat bidrar med väsentliga kolatomer. Cancer‑drivare såsom PI3K–AKT–mTORC1, RAS–MAPK och MYC skruvar upp dessa banor tillsammans, ökar nyckelenzymer och bygger till och med multi‑enzymkomplex som kanaliserar instabila intermediärer effektivt. I kontrast fungerar stressensorer som LKB1–AMPK och p53 normalt som bromsar, vilket minskar nukleotidproduktionen när energi eller DNA‑integritet hotas — bromsar som många tumörer inaktiverar.
Gammal cytostatika, ny metabol logik
Eftersom snabbväxande celler är så beroende av nukleotider, riktade några av de tidigaste cytostatikumen in sig på denna svaghet. Klassiska läkemedel såsom metotrexat, 5‑fluorouracil, cytarabin, gemcitabin och olika purinanalogar blockerar antingen folatanvändning, hämmar specifika enzymer eller utger sig för att vara felaktiga byggstenar som förgiftar DNA och RNA. Översikten omprövar dessa mediciner genom ruttningsmodellen och förklarar varför biverkningar och resistens är vanliga: icke‑cancerösa vävnader behöver också nukleotider, och tumörer kan ofta omdirigera flödet genom salvage eller parallella vägar när en nod blockeras.
Nästa generations strategier och öppna frågor
Nya angreppssätt syftar till att vara mer selektiva genom att slå mot de mest cancer‑snedvridna delarna av nätverket. Experimentella läkemedel utvecklas mot mitokondriella enkols‑enzymer som MTHFD2, pyrimidinenzymer som DHODH, och purinenzymer som IMPDH och PAICS, ofta i kombinationer som också blockerar salvage‑transportörer. Författarna föreslår praktiska markörer — såsom transportörnivåer, blodkärlstäthet, mitokondriell funktion och uttryck av specifika metabola enzymer — för att avgöra vilka tumörer som förlitar sig mer på de novo eller salvage och för att matcha patienter med väg‑riktade terapier. Framåtblickande lyfter de fram viktiga frågor, inklusive hur dessa vägar förändras över rum och tid inne i riktiga tumörer, hur omgivande immun‑ och stromaceller formar nukleotidtillgången, och hur man designar tolerabla läkemedelsscheman som utnyttjar replikationsstress utan att överväldiga normala vävnader. Tillsammans argumenterar arbetet för att förståelse och riktade insatser mot nukleotidmetabolism kan förvandla ett grundläggande krav för celldelning till en kraftfull, personlig hävstång mot cancer.
Citering: Vidal-Cruchez, O., Ben-Sahra, I. The oncogenic control of nucleotide synthesis. Oncogenesis 15, 17 (2026). https://doi.org/10.1038/s41389-026-00608-2
Nyckelord: nukleotidmetabolism, cancermetabolism, de novo-syntes, salvage-vägar, metabola terapier